Aluminiumacetat (Al (CH3CO) 3) Struktur, Eigenschaften, verwendet
- 2077
- 181
- Nick Laurén
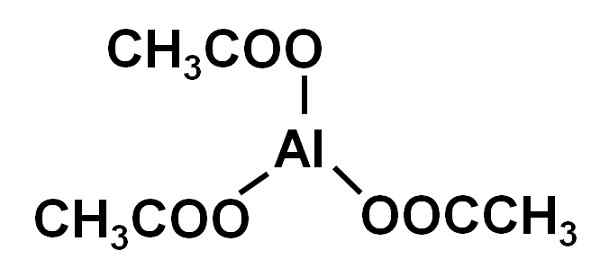
Er Aluminiumacetat Es handelt3+ und drei Acetationen Cho3Gurren-. Seine chemische Formel ist AL (Cho3Gurren)3. Es ist auch als Aluminium Triacetate bekannt. Es ist ein leicht hygroskopisches und lösliches Wasser fest im Wasser.
Um diese Verbindung zu erhalten, müssen völlig wasserfreie Bedingungen verwendet werden, dh frei von Wasser, sonst bilden sich die Aluminiumdiaceate bei (OH) (CH)3Gurren)2.
 Aluminium Triacetate AL (CH3Gurren)3. Autor: Marilú Stea.
Aluminium Triacetate AL (CH3Gurren)3. Autor: Marilú Stea. Aluminiumacetatlösungen haben antibakterielle und antimykotische Eigenschaften, so dass sie seit dem neunzehnten Jahrhundert zur Behandlung von Infektionen insbesondere der Ohren eingesetzt wurden.
Am bekanntesten ist Burows Lösung, die von einem deutschen Arzt entworfen wurde. Die Verwendung ist jedoch manchmal dazu geführt, das Mittelohr zu beschädigen.
Diese Lösung wurde auch zur Behandlung von Hautproblemen wie Juckreiz und Ausbruch verwendet. Es wird sogar als Sonnenbrand genutzt.
Aluminiumacetat und seine Derivate werden verwendet, um sehr kleine Strukturen oder Partikel von Aluminiumoxid an die2ENTWEDER3. Diese Strukturen oder Nanopartikel können in Form von Blättern, Blüten oder Nanoröhren sein.
[TOC]
Struktur
Aluminium Triacate wird durch ein Aluminiumkation zum3+ und drei Acetatanionen Cho3Gurren-. Es ist das Aluminiumsalz von Essigsäure ch3Cooh.
Aluminium ist mit Acetatanionen durch den Sauerstoff verbunden. Mit anderen Worten, es ist mit drei Sauerstoff verbunden. Diese Gewerkschaften sind ionisch.
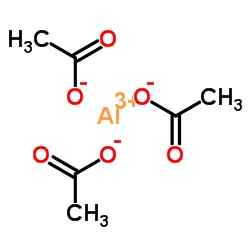 Ionenstruktur von Aluminiumacetat. N4TR!Umbr [CC BY-S (https: // CreePecommons.Org/lizenzen/by-sa/4.0)]]. Quelle: Wikimedia Commons.
Ionenstruktur von Aluminiumacetat. N4TR!Umbr [CC BY-S (https: // CreePecommons.Org/lizenzen/by-sa/4.0)]]. Quelle: Wikimedia Commons. Nomenklatur
- Aluminiumacetat
- Aluminium Triacetat
- Aluminiumethanoat
- Burow -Lösung (englische Übersetzung Burows Lösung): Es ist eine Aluminiumacetatlösung.
Eigenschaften
Körperlicher Status
Weiß feste.
Molekulargewicht
204.11 g/mol
Löslichkeit
In Wasser löslich.
Chemische Eigenschaften
In wässriger Lösung wird Aluminium Triacate gelöst und bildet das (OH) Diacetat (CH) tendenziell (OH) Diacetat (CH)3COO) und manchmal Monoacetat bei (OH)2(CH3Gurren). Es hängt alles vom pH und der Menge an Essigsäure CH ab3Cooh in der Lösung vorhanden.
Kann Ihnen dienen: Oberflächenspannung: Ursachen, Beispiele, Anwendungen und ExperimenteAl (Ch3Gurren)3 + H2Oder ⇔ al (oh) (Cho3Gurren)2 + CH3Cooh
Al (Ch3Gurren)3 + 2 h2Oder ⇔ al (OH)2(CH3COO) + 2 CH3Cooh
Andere Eigenschaften
Aluminiumacetat ist leicht hygroskopisch, dh es neigt dazu, Luftwasser zu absorbieren.
Erhalten
Aluminiumacetat wird vorzugsweise unter streng wasserfreien Bedingungen erhalten, dh bei totaler Wasser Abwesenheit. Dies beinhaltet auch das Fehlen von Luft, da dies Feuchtigkeit enthalten kann.
Eine Mischung aus Gletscher Essigsäure CH wird erhitzt3Cooh und Essigsäureanhydrid (CH3CO)2Oder unter solchen Bedingungen, die es ermöglichen, das gesamte gegenwärtige Wasser zu beseitigen. Zu dieser heißen Mischung wird Aluminiumchlorid Alcl zugegeben3 Ashidro fest (ohne Wasser).
Ein weißer Feststoff von AL (CH3Gurren)3.
Alcl3 + 3 Ch3Cooh → al (ch3Gurren)3 + 3 HCl
Das gesamte Fehlen von Wasser ist wichtig, um die Bildung von Aluminiummonoacetatsalzen bei (OH) zu vermeiden2(CH3COO) und Aluminiumdiacetat bei (OH) (Cho3Gurren)2.
Es kann auch durch Reaktion von Aluminiumhydroxid auf (OH) erhalten werden3 und Essigsäure ch3Cooh.
Verwendung in der Medizin
Ohr-Infektion
Aluminiumacetat wurde seit dem neunzehnten Jahrhundert zur Behandlung von Otitis verwendet, bei der eine Entzündung des äußeren oder mittleren Ohrs im Allgemeinen von Infektionen begleitet wird. Seine Verwendung ist auf seine antibakterielle und antimykotische Wirkung zurückzuführen.
Es wurde in Form einer 13%igen Aluminiumacetat -Lösung verwendet, die ursprünglich vom deutschen Arzt Karl August von Burow entwickelt wurde. Es heißt also Burow -Lösung.
Es wurde festgestellt Pseudomonas aeruginosa, Er Staphylococcus aureus und das Proteus mirabilis.
 Ohrenentzündungen werden seit vielen Jahren mit Aluminiumacetat behandelt. Autor: Ulrike Mai. Quelle: Pixabay.
Ohrenentzündungen werden seit vielen Jahren mit Aluminiumacetat behandelt. Autor: Ulrike Mai. Quelle: Pixabay. Es gibt jedoch diejenigen, die berichten, dass diese Lösungen für das Ohr schädlich sein können. Einige Studien an Tieren untersuchen ihre toxischen Wirkungen für das Ohr, haben jedoch widersprüchliche Ergebnisse berichtet.
Es kann Ihnen dienen: Zinkhydroxid (Zn (OH) 2)Bestimmte Forscher empfehlen, Aluminiumacetat nicht zu verwenden, wenn die Trommelmembran perforiert ist, da beobachtet wurde, dass sie eine entzündliche Wirkung auf das Mittelohr ausübt.
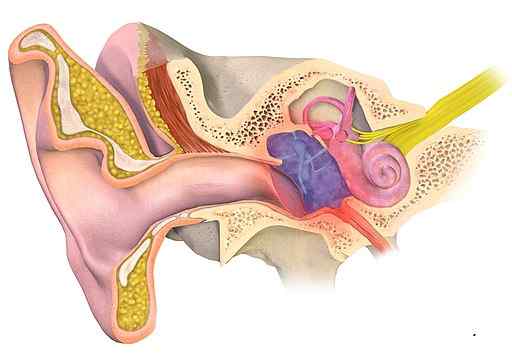 Es ist nicht bequem, Otitis -Medien (bläuliche Zone in der Abbildung) mit Aluminiumacetat zu behandeln. Bruceblaus [CC BY-SA (https: // creativecommons.Org/lizenzen/by-sa/4.0)]]. Quelle: Wikimedia Commons.
Es ist nicht bequem, Otitis -Medien (bläuliche Zone in der Abbildung) mit Aluminiumacetat zu behandeln. Bruceblaus [CC BY-SA (https: // creativecommons.Org/lizenzen/by-sa/4.0)]]. Quelle: Wikimedia Commons. Hautkrankheiten
Die Lösung von Burow wird als antiseptisches, adstringierendes und als topische Lösung zur Behandlung schwerer Eruptionen, Dermatitis, Entzündung, Juckreiz, Verbrennung und Sonnenbrand verwendet. Übt eine beruhigende und reduzierende Wirkung von Reizungen aus.
 Manchmal können Sonnenbrände mit einer Aluminiumacetatlösung behandelt werden. Autor: Tumisu. Quelle: Pixabay.
Manchmal können Sonnenbrände mit einer Aluminiumacetatlösung behandelt werden. Autor: Tumisu. Quelle: Pixabay. Andere Verwendungen
Aluminium Triacate und seine Derivate werden für viele qualitative und quantitative chemische Experimente verwendet.
Ein Derivat von Aluminium Triacetat, Diacetat bei (OH) (CH3Gurren)2 Auch als Aluminiumhydroxidacetat bezeichnet, wird es als Vorläufer verwendet, um Gamma-Aluminiumoxid-Nanostrukturen (γ-al) zu erhalten2ENTWEDER3).
In diesem Fall bedeutet Vorläufer, dass aus dem Aluminium-Diacetat (auf eine bestimmte Weise erhalten) die γ-Al-Nanostrukturen hergestellt werden2ENTWEDER3, Und dies wird erreicht, indem es bei sehr hohen Temperaturen erhitzt wird.
Nanostrukturen sind sehr kleine Partikel, die nur durch spezielle Mikroskope wie elektronische Mikroskope beobachtet werden können. Mit Aluminiumacetat als Vorläufer wurden Nanostrukturen von γ-to erhalten2ENTWEDER3 Ähnlich wie Blätter, Blüten, Fasern und sogar Nanoröhren.
 Aluminiumoxid -Nanofribos können unter Verwendung eines Aluminiumacetatderivats erhalten werden. Aleksei TR [CC BY-SA (https: // creativecommons.Org/lizenzen/by-sa/4.0)]]. Quelle: Wikimedia Commons.
Aluminiumoxid -Nanofribos können unter Verwendung eines Aluminiumacetatderivats erhalten werden. Aleksei TR [CC BY-SA (https: // creativecommons.Org/lizenzen/by-sa/4.0)]]. Quelle: Wikimedia Commons. Einsatzgebrauch
Zu Beginn des 20. Jahrhunderts wurde Aluminiumacetat als Konservierungsmittel wie Dosen Würste verwendet.
Eine Aluminiumacetatlösung wurde durch Mischen von Aluminiumsulfat an die hergestellt2(SW4)3, Caco Calciumcarbonat3, Essigsäure ch3Cooh und Agua h2Oder, und zu Essen hinzugefügt.
Wenn diese Lösung mit Fleisch in Kontakt kommt, wird Aluminium in den Bestandteilen in Form einer Verbindung fixiert, die in kochendem Wasser unlöslich ist, in Magensäften jedoch um ungefähr 80% auflöst.
Es kann Ihnen dienen: Bromous Säure (Hbro2): physikalische und chemische Eigenschaften und verwendet und verwendetBereits im Jahr 1904 war bekannt, dass Aluminiumsalze die Verdauung im Magen und im Darm verzögern. Daher ist es eine nicht konventionelle Praxis, Aluminiumacetat -Lösungen in Konserven hinzuzufügen.
 In der Vergangenheit wurde Aluminiumacetat als Konservierungsmittel in Konserven verwendet. Es ist derzeit bekannt, dass es schädlich ist und nicht mehr dafür verwendet wird. Autor: Changglc. Quelle: Wikimedia Commons.
In der Vergangenheit wurde Aluminiumacetat als Konservierungsmittel in Konserven verwendet. Es ist derzeit bekannt, dass es schädlich ist und nicht mehr dafür verwendet wird. Autor: Changglc. Quelle: Wikimedia Commons. Schädliche Effekte
Da es Studien gibt, die berichten, dass Aluminiumacetat toxisch sein kann, wurden Tests durchgeführt, bei denen Aluminiumacetat in Labormäuse injiziert wurde.
Die Ergebnisse deuten darauf hin, dass diese Verbindung das Rückgrat dieser Tiere schädigen und die Chromosomen und Spermien der Tiere beschädigt haben. Mit anderen Worten, es ist genotoxisch.
Dies warnt vor möglichen gesundheitlichen Gefahren, die zu einer Überbelichtung von Aluminiumacetat und der Sorgfalt, die während des Gebrauchs angenommen werden muss.
Verweise
- Mac-Kay Chace und. (1904). Die Verwendung von Basis -Aluminiumacetat als Konservierungsmittel in der Wurst. Journla der American Chemical Society 1904, 26, 6: 662-665. Aus Pubs geborgen.ACS.Org.
- Haube, g.C. und ihde, a.J. (1950). Aluminiumacetate und Propionate - die Vorbereitung und Zusammensetzung. Zeitschrift der American Chemical Society 1950, 72, 5: 2094-2095. Aus Pubs geborgen.ACS.Org.
- Pitaro, j. et al. (2013). Ototoxizität von Aluminiumacetat/Benzolethoniumchlorid -Otic -Lösung im Chinchilla -Tiermodell. Laryngoscope, 2013; 123 (10): 2521-5. NCBI erholte sich.NLM.NIH.Regierung.
- Thorp, m.ZU. et al. (2000). Burows Lösung bei der Behandlung von aktivem, viel chronisch supruritivem Mittelohrentzündungsmedium: Bestimmung einer wirksamen Verdünnung. Das Journal of Laryngology & Otology, Juni 2000, vol. 114, pp.432-436. NCBI erholte sich.NLM.NIH.Regierung.
- D'ouza, Mr.P. et al. (2014). Bewertung der Genotoxie von Studienschärfen im Knochenmark, männlichen Keimzellen und fetalen Leberzellen von Schweizer Albino -Mäusen. Mutationsforschung 766 (2014) 16-22. NCBI erholte sich.NLM.NIH.Regierung.
- Basal und. et al. (2015). Die Auswirkungen der Lösungen von Topical Burow und Castellanis auf die Mittelohrschleimhaut der Ratten. J. Int adv otol 2015; 11 (3): 253-6. Von Advancedotology erholt.Org.
- ODER.S. Nationalbibliothek für Medizin. (2019). Acetat still. Aus Pubchem geborgen.NCBI.NLM.NIH.Regierung.
- Buttaravoli, p. Und Leffler, s.M. (2012). Sonnenbrand. Was zu tun ist. In geringem Notfall (dritte Ausgabe). Von Scientedirect erholt.com.
- Thompson, e. und Kalus, zu. (2017). ACTE -Hautreaktionen und bakterielle Infektionen. Behandlung. Im Handbuch für Reise- und Tropenmedizin (fünfte Ausgabe). Von Scientedirect erholt.com.
- Kim, t. et al. (2010). Steuerbare Morphologie-Synthese von Gamma-Alumin. Kristallwachstum & Design, vol.10, nein. 7, 2010, pp.2928-2933. Aus Pubs geborgen.ACS.Org.
- Rajala, j.W. et al. (2015). Core-Shell Electrospun Hohlaluminiumoxid-Keramikfasern. Fasern 2015, 3, 450-462. MDPI erholt sich.com.

