Isoamilico alkoholische Struktur, Eigenschaften, Verwendung und Risiken
- 3390
- 495
- René Riediger
Er Isoamylalkohol Es ist eine organische Verbindung, deren Formel ist (ch3)2CHCH2CH2Oh. Chemisch gesehen ist ein verzweigter primärer Alkohol und bildet eines der Pentanol -Isomere, genannt Amylalkohole (C5H12ENTWEDER).
Wie viele Alkohole mit niedrigem Molekulargewicht ist es eine farblose Flüssigkeit bei Raumtemperatur. Dies ermöglicht und erleichtert, dass es als Lösungsmittel für verschiedene Anwendungen verwendet wird. Darüber hinaus, wenn es nach dem Abwerfen nicht zu viele negative Auswirkungen auf das Ökosystem ausübt.
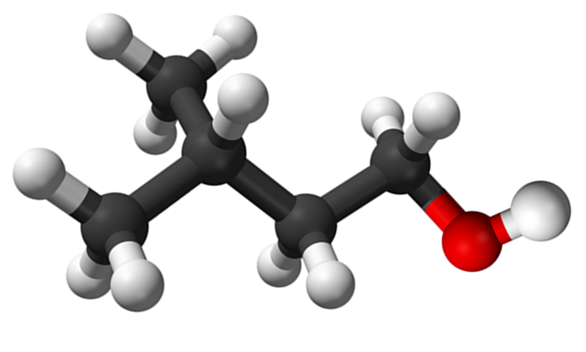
 Isoamilic Alkoholmolekül. Quelle: Claudio Pistilli de Wikipedia.
Isoamilic Alkoholmolekül. Quelle: Claudio Pistilli de Wikipedia. Während es ein Vermittlermaterial in der Synthese von Amiloacetat zur Ausarbeitung von Bananenduftstoffen ist, ist sein eigener Geruch unangenehm und ähnlich wie der von Birnen.
Zusätzlich zum Lösungsmittel mehrerer biologischer Substanzen und als Vermittler bei der Synthese anderer Acetate reduziert es die Oberflächenspannung bestimmter industrieller Formulierungen, wodurch sich die Bildung von Schäumen verhindert. Daher wird es in mikroemulgierten Systemen verwendet.
In Bezug auf seinen natürlichen Ursprung wurde in den Horomonas der Hornissen Isoamilic Alkohol gefunden, und in den schwarzen Trüffeln eine Art Pilz im europäischen Südosten, der sich im europäischen Südosten befindet.
[TOC]
Isoamilico -Struktur
Im oberen Bild wurde das Isoamylalkoholmolekül mit einem Kugeln und Balkenmodell gezeigt. Rechts davon entspricht die rötliche Kugel dem Sauerstoffatom der OH -Gruppe, das für alle Alkohole charakteristisch ist. Auf der linken Seite befindet sich das kohlensäurehaltige Skelett mit einer Methylgruppe, Cho3, Branzt die Struktur.
Aus molekularer Sicht ist diese Verbindung dynamisch für Atome mit SP -Hybridationen3, Erleichterung der Rotation ihrer Verbindungen; Solange es nicht dazu führt3.
Es ist auch erwähnenswert sein, sein amphiphiles Merkmal: Es hat ein apolares oder hydrophobe Ende, das von der Kette besteht3)2CHCH2CH2-, und ein polarer oder hydrophiler Kopf, die OH -Gruppe. Diese Definition von zwei spezifischen Bereichen unterschiedlicher Polaritäten macht diesen Alkohol zu einer Spannung; Und von hier aus ist es an der Anwendung für Mikroemulsionen zurückzuführen.
Kann Ihnen dienen: HebelregelIntermolekulare Wechselwirkungen
Angesichts des Vorhandenseins der OH -Gruppe zeigt das Isoamilic Alkoholmolekül ein dauerhaftes Dipolmoment. Folglich das Dipol-Dipol.
Während der Zweig der Hauptketten wirksame Wechselwirkungen zwischen Molekülen verringert, kompensieren Wasserstoffbrücken in diesem Alkohol diesen Abstieg, wodurch die Flüssigkeit bei 131 ° C kocht.
Es geschieht nicht mit seinem festen oder „Eis“, der auf -117 ° C schmilzt, was darauf hinweist, dass seine intermolekularen Wechselwirkungen nicht stark genug sind, um ihre Moleküle ordentlich zu halten. vor allem, wenn die Cho -Gruppe3 Das Zweifel der Hauptkette verhindert einen besseren Kontakt zwischen Molekülen.
Eigenschaften
Aussehen
Farblose Flüssigkeit.
Riechen und schmecken
Lehnt einen unangenehmen Geruch ab, der dem der Birne ähnelt, und hat einen scharfen Geschmack.
Molmasse
88.148 g/mol.
Dichte
0,8104 g/ml bei 20 ° C. Es ist daher weniger dicht als Wasser.
Wasserdampfdichte
Es ist 3,04 -mal dichter als Luft.
Dampfdruck
2,37 mmHg bei 25 ° C.
Siedepunkt
131,1 ° C.
Schmelzpunkt
-117,2 ° C.
Zündungspunkt
43 ° C (geschlossener Tasse).
Selbstdirektionstemperatur
340 ° C.
Löslichkeit
Es ist relativ löslich in Wasser: 28g/l. Dies liegt daran. Wenn gemischt, würden zwei Phasen beobachtet: eine niedrigere, entsprechend Wasser und ein Vorgesetzter, das von Isoamylalkohol.
Im Gegensatz dazu ist es in weniger polaren Lösungsmitteln wie: Aceton, Ether, Chloroform, Ethanol oder Gletscher Essigsäure viel löslicher; und sogar in Ölether.
Es kann Ihnen dienen: Labor -Thermometer: Eigenschaften, wofür es, für die Verwendung, BeispieleSchmiere
3.738 CP bei 25 ° C.
Oberflächenspannung
24,77 Dins/cm A 15 ° C.
Brechungsindex
1.4075 bis 20 ° C.
Wärmekapazität
2.382 kJ/g · k.
Anwendungen
Rohmaterial
From isoamilic alcohol other esters, thiophene, and drugs such as amilo nitrite, Validol (isavalerate mentile), bromisoval (bromobalerilurea), Corvalol (a callerian tranquanar) and Barbamil (amobarbital) (amobarbital).
Düfte
Zusätzlich zur Verwendung zur Synthese von Amiloacetat, die ein Bananenaroma hat, werden auch andere Fruchtdüfte wie Aprikose, Orangen, Pflaumen, Kirsche und Malz davon erhalten. Daher ist es ein notwendiger Alkohol bei der Ausarbeitung zahlreicher essbarer oder kosmetischer Produkte.
Antispumant
Durch die Reduzierung der Oberflächenspannung fördert es die Verwendung in mikroemulgierten Systemen. Vermeiden Sie praktisch eine beschleunigte Blasenbildung und reduzieren Sie sie in Größe, um sie zu brechen.
Es hilft auch, die Grenzfläche zwischen wässrigen und organischen Phasen während der Extraktionen besser zu definieren. Beispiel. Diese Technik ist für die DNA -Extraktion bestimmt.
Extraktionen
Mit Isoamylalkohol können Sie auch Fette oder Öle aus verschiedenen Proben extrahieren, zum Beispiel Milch. Auch Paraffinwachs, Tinten, Gummi, Lack und Celluloseester auflösen.
Mit Extraktionen können Sie Phosphorsäure aus Eisenphosphat -Minerallösungen erhalten.
Risiken
Lagerung und Reaktivität
Wie jede Flüssigkeit, die Gerüche verleiht, kann sie ein bevorstehendes Feuerrisiko darstellen, wenn der Ort, an dem seine Temperatur zu gespeichert ist, noch mehr, wenn es bereits eine Wärmequelle gibt.
Unter diesen Bedingungen fungiert es einfach als Kraftstoff, füttert die Flammen und nutzt sogar seinen Behälter aus. Lassen Sie beim Verbrennen Dämpfe frei, die die Gesundheit beeinflussen und Erstickung verursachen können.
Kann Ihnen dienen: Quantitative Analyse in der Chemie: Messungen, VorbereitungAndere Ursachen, bei denen Isoamilic Alkohol in Brand gesetzt wird, besteht darin, ihn zu mischen oder mit Substanzen wie Peroxiden, Brome zu reagieren.
Gesundheit
Bei Kontakt mit der Haut können Sie sie reizen und austrocknen. Die Symptome sind jedoch schwerwiegender, wenn es zu lange eingeatmet wird (Husten, Nasenverbrennungen, Hals und Lungen) oder bei Einnahme (Kopfschmerzen, Übelkeit, Durchfall, Erbrechen, Schwindel und Wissensverlust)).
Und schließlich, wenn es in den Augen verschüttet wird, irritiert sie und kann ihnen sogar irreversibel schaden. Glücklicherweise ermöglicht der Geruch von "alkoholischen Birnen", dass Sie es bei Flucht oder Verschütten erkennen können. Darüber hinaus ist es eine Verbindung, die mit Respekt manipuliert werden muss.
Verweise
- Morrison, r. T. und Boyd, r, n. (1987). Organische Chemie. 5. Ausgabe. Editorial Addison-Wesley Interamerikaner.
- Carey f. (2008). Organische Chemie. (Sechste Ausgabe). Mc Graw Hill.
- Graham Solomons t.W., Craig b. Braten. (2011). Organische Chemie. Amine. (10. Ausgabe.). Wiley Plus.
- Wikipedia. (2019). Isoamylalkohol. Abgerufen von: in.Wikipedia.Org
- Nationales Zentrum für Biotechnologie Information. (2019). Isoamylalkohol. Pubchem -Datenbank. CID = 31260. Erholt von: Pubchem.NCBI.NLM.NIH.Regierung
- Zhang Yu & Muhammed Mamoun. (17. September 2008). Extraktion von Phosphorsäure aus Nitratlösungen mit Isoamylalkohol. Lösungsmittelextraktion und Ionenaustausch Band 6, 1988 - Ausgabe 6. doi.org/10.1080/07366298808917973
- Das Gesundheitsministerium in New Jersey. (2008). Isoamylalkohol. [PDF]. Erholt von: NJ.Regierung
- Kat Chem. (2019). Isoamylalkohol. Erholt von: Kat-Chem.Hu
- Chemoxy International Ltd. (S.F.). Isoamylalkohol. Erholt von: Chemoxy.com
- « Triethilaminstruktur, Eigenschaften, Verwendung und Risiken
- Liechtenstein Flagge Geschichte und Bedeutung »

