Alkine
- 817
- 41
- Rieke Scheer
 Alvento -Struktur mit einem dreifachen Link
Alvento -Struktur mit einem dreifachen Link Was sind Alkine?
Der Alkine Sie sind Kohlenwasserstoffe oder organische Verbindungen, die in ihren Strukturen eine dreifache Verbindung zwischen zwei Kohlenstoffen enthalten. Diese dreifache Verbindung (≡) wird als funktionale Gruppe angesehen, wenn sie ein aktives Zentrum des Moleküls darstellt, und ist daher für ihre Reaktivität verantwortlich.
Obwohl Alkines nicht viel von Alko oder Alkenen unterscheiden, weisen sie aufgrund der Art ihrer Verbindungen eine größere Säure und Polarität auf. Der genaue Begriff, um diesen kleinen Unterschied zu beschreiben, ist das, was bekannt ist Unsättigung.
Die Alkane sind gesättigte Kohlenwasserstoffe, während die Alkine in Bezug. Was bedeutet das? Das ein Alkane h3C-ch3 (Ethan) kann Dehydrogen zu H sein2C = Ch2 (Etene) und anschließend HCighCh (etino oder besser bekannt als Acetylen).
Beachten Sie, wie sich bei Kohlenstoffen als zusätzliche Links enthält. Der Kohlenstoff versucht aufgrund seiner elektronischen Eigenschaften, vier einfache Verbindungen zu bilden, desto größer ist die Tendenz zum Reaktieren (mit Ausnahme von aromatischen Verbindungen).
Andererseits ist die dreifache Verbindung viel stärker als die doppelte (=) oder die einfache (-) Bindung, jedoch zu hohen Energiekosten. Daher können die meisten Kohlenwasserstoffe (Alkaner und Alkene) bei hohen Temperaturen dreifache Bindungen bilden.
Als Folge der hohen Energien von diesen ließen sie beim Brechen sehr heiß ab. Ein Beispiel für dieses Phänomen ist zu beobachten, wenn Acetylen mit Sauerstoff verbrennt und die intensive Wärme der Flamme zu Schweißnaht oder Schmelzmetallen verwendet wird.
Acetylen ist das einfachste und kleine Alkin von allen. Andere Kohlenwasserstoffe können aus ihrer chemischen Formel exprimiert werden, indem H durch alquilische Gruppen ersetzt wird (RC≡CR '). Gleiches gilt in der Welt der organischen Synthese durch eine große Anzahl von Reaktionen.
Dieses Alkin erfolgt aus der Reaktion von Calciumoxid des Kalksteins und des Coque, dessen Rohstoff die erforderlichen Kohlenstoffe in einem elektrischen Ofen liefert:
CaO + 3c => CAC2 + CO
Der CAC2 Es ist Calciumcarbid, eine anorganische Verbindung, die schließlich mit Wasser auf Acetylen reagiert:
CAC2 + 2H2O => ca (OH)2 + Hcais
Physikalische und chemische Eigenschaften von Alkinen
Polarität
Die dreifache Verbindung unterscheidet Alkine von Alkanern und Alkenen. Die drei Arten von Kohlenwasserstoffen sind apolar, unlöslich in Wasser und sehr schwache Säuren. Die Elektronegativität der Doppel- und Dreifachbindungskohlenstoff ist jedoch größer als die von einfachen Kohlenstoffen.
Danach ergeben Kohlenstoffe neben der Dreifachbindung die induktive Wirkung negativer Lastdichte. Aus diesem Grund gibt es die CighC- oder C = C -Verbindung, die eine größere elektronische Dichte als im Rest des kohlensäurehaltigen Skeletts gibt. Infolgedessen gibt es ein kleines Dipolmoment, in dem die Moleküle durch Dipol-Dipolo-Kräfte interagieren.
Diese Wechselwirkungen sind sehr schwach, wenn ihre Dipolmomente mit denen des Wassermoleküls oder Alkohols verglichen werden. Dies spiegelt sich in ihren physikalischen Eigenschaften wider: Alkine haben im Allgemeinen höhere Fusions- und Siedepunkte im Vergleich zu denen ihrer weniger ungesättigten Kohlenwasserstoffe.
Kann Ihnen dienen: die 7 wichtigsten Biochemie -AnwendungenEbenso sind sie aufgrund ihrer geringen Polarität weniger unlöslich in Wasser, aber in apolaren organischen Lösungsmitteln wie Benzol löslich.
Säure
Auch diese Elektronegativität verursacht Wasserstoff HC≡CR ist saurer als jeder in anderen Kohlenwasserstoffen vorhanden. Daher sind Alkine Arten saurer als Alkene und viel mehr als Alkane. Seine Säure bleibt jedoch im Vergleich zu Carbonsäuren verabscheuungswürdig.
Da Alkine sehr schwache Säuren sind, reagieren sie nur mit sehr starken Basen wie Natriummasturo:
HCais + nanh2 => Hcigncna + nh3
Aus dieser Reaktion wird eine Lösung von Natriumacetylure erhalten, Rohmaterial für die Synthese anderer Alkine.
Alquinos Reaktivität
Die Reaktivität der Alkine wird durch die Zugabe kleiner Moleküle zu ihrem dreifachen Glied erklärt, wodurch die Ungesättigtheit verringert wird. Dies können Wasserstoffmoleküle, Wasserstoffhillogenide, Wasser oder Halogene sein.
Hydrierung
Das kleine H -Molekül2 Es ist sehr schwer fassbar und schnell, um die Wahrscheinlichkeit zu erhöhen, in die dreifache Verbindung der Alkine hinzugefügt zu werden.
Dies sind normalerweise Metalle (PD, PT, RH oder NI), die fein geteilt sind, um die Oberfläche zu erhöhen; Und auf diese Weise den Kontakt zwischen Wasserstoff und Alquino:
Rcais ' + 2h2 => Rch2CH2R '
Das Ergebnis ist, dass Wasserstoff "Anker" für Kohlenstoffe ist, die eine Bindung brechen, und so weiter2CH2R '. Dies sättigt nicht nur den anfänglichen Kohlenwasserstoff, sondern modifiziert auch seine molekulare Struktur.
Zugabe von Wasserstoffhalogenuros
Hier wird das anorganische Molekül HX hinzugefügt, wobei X eines der Halogene (F, Cl, Br oder I) sein kann:
Rcais ' + hx => rch = cxr'
Flüssigkeitszufuhr
Die Hydratation von Alkinen ist, wenn sie ein Wassermolekül hinzufügen, um einen Aldehyd oder ein Keton zu bilden:
Rcais ' + h2O => rch2Cor '
Wenn R 'ein H ist, ist es ein Aldehyd; Wenn es sich um eine Miete handelt, dann ist es ein Cetona. In der Reaktion wird eine Verbindung, die als Enol (RCH = C (OH) r ') bekannt ist, als Zwischenmediär gebildet.
Dies leidet in einem Gleichgewicht, der als Tautomerisierung bezeichnet wird.
Zugabe von Halogenen
Und in Bezug auf Ergänzungen können die zweigärischen Moleküle von Halogenen auch an Kohlenstücken verankert werden (x x2= F2, Cl2, Br2 I habe gehört2):
Rcais ' + 2x2 => RCX2-CX2R '
Acetylenalkylierung
Aus der Natriumacetylurlösung können andere Alkine durch Verwendung eines Miden -Halogenids hergestellt werden:
HcighNa + rx => hcighcr + nax
Wenn es sich beispielsweise um das Methyljodid handelte, wäre das resultierende Alkin:
HcighNa + ch3I => hcighCch3 + Nax
Hcighcch3 ist der richtige, auch bekannt als MethylAcetylen.
Chemische Struktur von Alkinen
 Chemische Struktur des Alquino
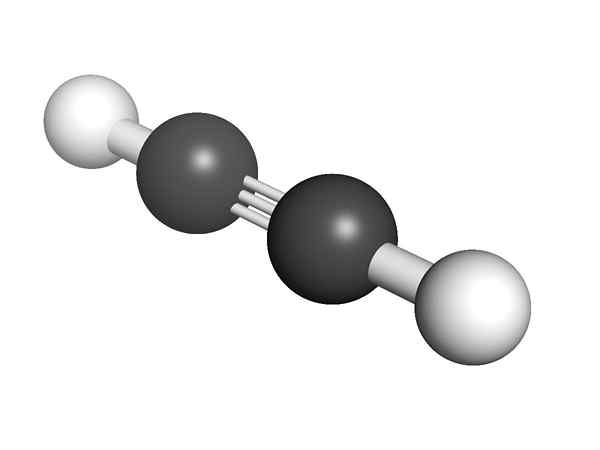
Chemische Struktur des Alquino Was ist die Struktur der Alkine? Im oberen Bild wird ein Acetylenmolekül gezeigt. Die lineare Geometrie der Cwerbs -Verbindung kann daraus klar sein.
Wenn es eine dreifache Bindung gibt, muss die Struktur des Moleküls linear sein. Dies ist ein weiterer der bemerkenswerten Unterschiede zwischen ihnen und dem Rest der Kohlenwasserstoffe.
Es kann Ihnen dienen: Cycopropan (C3H6)Die Alkane werden normalerweise als Zickzack dargestellt, weil sie SP -Hybridisierung haben3 und ihre Links sind getrennt 109º. Sie sind tatsächlich eine kovalent vereinigte Tetraederkette. Während Alkene durch SP -Hybridisierung flach sind2 seiner Kohlenstoffe bilden sich insbesondere eine trigonale Ebene mit getrennten Glieren von 120 °.
In Alkinen ist die Orbitalhybridisierung SP, dh 50% von A S und 50% eines P. Es gibt zwei SP -Hybridorbitale, die in Acetylen- oder Alkingruppen in den Alkinen mit H -Atomen verbunden sind.
Die Entfernung sowohl H als. Aus diesem Grund ist der Link -c≡C- linear. Sehen Sie die Struktur eines beliebigen Moleküls in den Regionen, in denen das Skelett sehr linear ist.
Abstand von den Links und terminalen Almosen
Kohlenstoffe in der Dreifachbindung sind in einem geringeren Abstand als im Doppel oder im einfachen Link. Mit anderen Worten, Cwerbs ist kürzer als C = C und dass C-C. Infolgedessen ist die Verbindung stärker, da die beiden π -Verbindungen dazu beitragen, die einfache Verbindung σ zu stabilisieren.
Wenn sich die dreifache Bindung am Ende einer Kette befindet, ist es ein terminales Alkin. Daher muss die Formel dieser Verbindung HC≡CR sein, wobei das H das Ende oder Beginn der Kette bemerkt.
Wenn es sich im Gegenteil um eine dreifache interne Verbindung handelt, ist die Formel RC≡CR ', wobei R und R die rechte und linke Seite der Kette sind.
Nomenklatur der Alquinos
Wie werden Alkines gemäß den vom IUPAC diktierten Regeln ernannt?? Ebenso wie die Alquenos und Alkene ernannt wurden. Dazu wird das Suffix -ano oder -eno für das Suffix -oino geändert.
Zum Beispiel: hcighCch3 Es sind Tipps ernannt, da es drei Kohlenstoffe hat, wie z. B. Propan (Cho3CH2CH3). Der HC≡CCH2CH3 Es ist der 1-Butino, bei dem es sich um ein terminales Alkin handelt. Aber im Fall von Cho3Cais3 Dies ist der 2-Butino, und darin ist die dreifache Verbindung nicht terminal, sondern intern.
Das CH3Cais2CH2(CH3)2 Es ist 5-Methyl-2-Hexin. Kohlenstoffe beginnt von der Seite, die dem Triple Link am nächsten liegt.
Eine andere Art von Alkinen sind die Cycloalquine. Für sie reicht es aus, das Suffix -ano durch -ino des entsprechenden Cycloalcans zu ersetzen. Somit wird das Cyclopropan mit einer dreifachen Bindung als Cyclopropin bezeichnet (was nicht existiert).
Wenn es zwei dreifache Links gibt, wird das Präfix DI zum Namen hinzugefügt-. Es hat als Beispiele für HCigh-C-Cwerb, Diacetylen oder Propadine; Und zu HCighC-C-Cwerb, Butadiino.
Alquinos verwendet
Acetylen oder Etino
Das kleinste der Alkinnen verdickt die mögliche Anzahl der Verwendungen für diese Kohlenwasserstoffe. Von der Alken können andere organische Verbindungen synthetisiert werden. Es erfährt auch oxidative Reaktionen, um unter anderem Ethanol, Essigsäure und Acrylsäure zu erhalten.
Kann Ihnen dienen: Lithiumhydrid: Struktur, Eigenschaften, erhalten, verwendet, verwendetAndere ihrer Verwendungen bestehen darin, die Wärmequelle zur Anregung der Elektronen von Atomen bereitzustellen. Spezifischer, E von Metallkationen in Bestimmungen durch Atomabsorptionsemission, weit verbreitete spektroskopische Technik.
Naturalkine
Die einzigen vorhandenen Methoden zur Herstellung von Alkinen sind nicht nur synthetisch oder mit Wärmeanwendung in Abwesenheit von Sauerstoff, sondern auch biologisch.
In diesen Enzymen genannt Acetylese, was eine Doppelbindung verweigern kann. Dank dessen werden viele natürliche Alkinquellen erreicht.
Anschließend können diese Quellen Gifte, Gegenmittel, Arzneimittel oder eine andere Verbindung, die einen Nutzen bieten, extrahiert werden. vor allem, wenn es sich um die Gesundheit handelt. Die Alternativen sind viele, wenn sie ihre ursprünglichen Strukturen modifizieren und sie als Unterstützung für neue Alkine haben.
Beispiele für Alkine
Bisher wurden zahlreiche Beispiele für Alkine erwähnt. Einige stammen jedoch aus sehr bestimmten Quellen oder haben bestimmte molekulare Strukturen: Sie sind Polyacetyle.
Dies bedeutet, dass es möglicherweise mehr als eine dreifache Verbindung gibt, die Teil einer sehr großen Struktur ist und nicht nur eine einfache kohlensäurehaltige Kette.
Tarirsäure
 Tarysäurestruktur
Tarysäurestruktur Taririnsäure stammt aus einer Pflanze in Guatemala namens Picramnia Tariri. Es wird speziell aus dem Öl aus seinen Samen extrahiert.
In seiner molekularen Struktur kann eine einzelne dreifache Verbindung beobachtet werden, die einen apolaren Schwanz von einem polaren Kopf trennt; Daher könnte es als amphipatisches Molekül betrachtet werden.
Histrionicotoxin
 Histionikotoxinstruktur
Histionikotoxinstruktur Histionikotoxin ist ein Gift, das von der Haut der Einwohner Kolumbiens, Brasiliens und anderer lateinamerikanischer Länder getrennt ist. Es hat zwei dreifache konjugierte Links mit einer Doppelbindung. Beide sind Terminals und sind durch einen sechs Kohlenstoffring und einen zyklischen Amin getrennt.
Cicutoxin
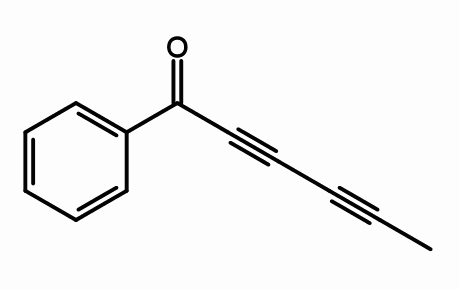 Cicutoxin -Struktur. Von Giorgiogp2 [CC BY-SA 3.0 (https: // creativecommons.Org/lizenzen/by-sa/3.0) oder GFDL (http: // www.Gnu.Org/copyleft/fdl.html)] aus Wikimedia Commons
Cicutoxin -Struktur. Von Giorgiogp2 [CC BY-SA 3.0 (https: // creativecommons.Org/lizenzen/by-sa/3.0) oder GFDL (http: // www.Gnu.Org/copyleft/fdl.html)] aus Wikimedia Commons Aus der molekularen Struktur von Cicutoxin, wo sind die dreifachen Verbindungen? Wenn die doppelten Bindungen flach sind, wie sie richtig gesehen werden und die einfachen Glieder Tetraedralen sind, sind die Dreifachungen linear und sind am Steigungen (\).
Diese Verbindung besteht aus einem Neurotoxin, das hauptsächlich in der Wasserheilpflanze gefunden wurde.
Capillina
 Kapillina -Struktur. Von Klever [CC0] aus Wikimedia Commons
Kapillina -Struktur. Von Klever [CC0] aus Wikimedia Commons Es ist ein Alkin, das im ätherischen Öl von Artemis -Pflanzen vorhanden ist, das als Antimykotikum verwendet wird. Es können zwei drei aufeinanderfolgende Links beobachtet werden, korrekter konjugiert.
Was bedeutet das? Dass die Dreifachbindungen entlang der gesamten Kohlenstoffkette schwingen und beinhalten, dass die Doppelbindung C = o für C-O geöffnet wird-.
Pargilin
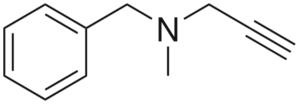 Struktur von Pargilin
Struktur von Pargilin Es ist eine Alty mit blutdrucksenkender Aktivität. Die Analyse seiner Struktur in Teilen ist: eine Bankgruppe nach links, ein tertiäres Amin in der Mitte und eine rechte Wing; das heißt eine terminale Eigenschaftsgruppe.
Verweise
- Francis a. Schildpatt. Organische Chemie. Carbonsäuren. (Sechste Ausgabe., Seite 368-397). Mc Graw Hill.
- Brennan, John. (10. März 2018). Beispiel für Alkine. Wissenschaftlich. Entnommen aus: Wissenschaft.com
- Byju. (2018). Dreifachbindung in Alkinen. Genommen von: Byjus.com
- Enzyklopädie von Beispielen (2017). Alkine. Wiederhergestellt von: Beispiele.CO
- Kevin a. Boudreaux. Alkine. Genommen von: Angelo.Edu
- Robert c. Neuman, jr. Alkene und Alkines. [PDF]. Genommen von: Chem.UCR.Edu

