Kohlenstoff -Alotrope
- 841
- 121
- Ibrahim Steuk
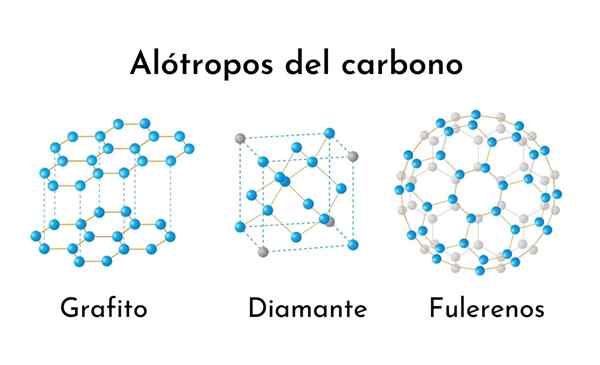 Drei der häufigsten Kohlenstoff -Alotrope
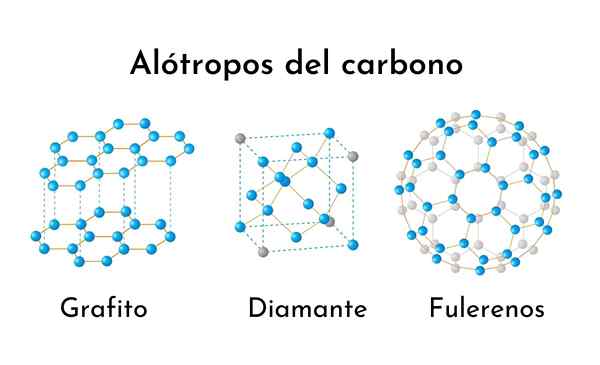
Drei der häufigsten Kohlenstoff -Alotrope Was sind Kohlenstoff Alotrope?
Das alotrope Wort bezieht sich auf die verschiedenen molekularen Formen, in denen ein chemisches Element vorgestellt werden kann. Daher sind Kohlenstoff -Alotrope alle Formen, natürlich oder nicht, da das reine Kohlenstoffelement vorgestellt werden kann.
Trotz genau der gleichen Zusammensetzung können Alotropes völlig unterschiedliche Eigenschaften haben.
Dies ist besonders bei Kohlenstoff Alotropen notorisch berüchtigt. Wie wir später sehen werden werden.
Als nächstes werden bisher alle Kohlenstoff -Alotrops zusammen mit ihren herausragendsten Eigenschaften und ihrer Anwendungen beschrieben:
Diamant
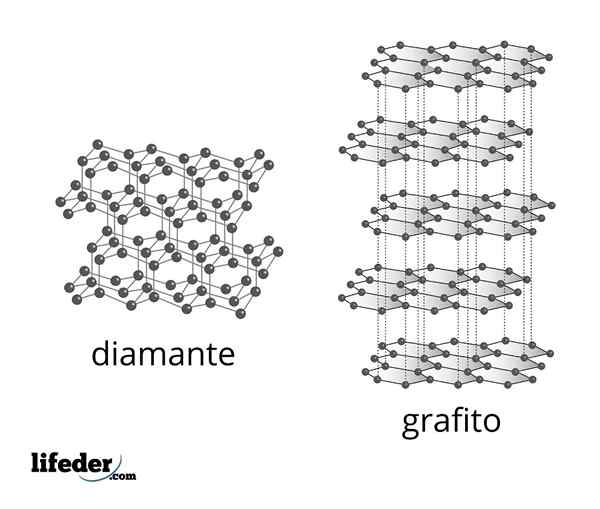 Mikroskopische Struktur von Diamant und Graphit
Mikroskopische Struktur von Diamant und Graphit Der Diamant ist die stabilste Form von Kohlenstoff und einer der zwei bekanntesten Alotrope dieses Elements. Es besteht aus tetraedrischen Kohlenstoffatomen mit SP -Hybridisierung3 mit einfachen c-c kovalenten Bindungen in einem dreidimensionalen kovalenten Netzwerk verknüpft.
Dieses Kohlenstoff -Alotrope ist natürlich oder kann industriell aus Graphit mit hohen Drücken hergestellt werden.
Eigenschaften
- Es besteht aus einem transparenten und farblosen kristallinen Feststoff, der bei hoher Helligkeit poliert werden kann.
- Es ist das härteste Mineral, das vom Menschen bekannt ist. Dies bedeutet, dass ein Diamant in der Lage ist, die Oberfläche eines anderen Materials zu kratzen und nur mit einem anderen Diamanten zerkratzt werden kann.
- Es ist eines der teuersten natürlichen Elemente der Welt.
- Es ist der beste thermische Leiter, der bekannt ist, mit einer thermischen Leitfähigkeit zwischen 1300 und 2300 w/m.K.
- Leitet keinen Strom.
- Es hat einen sehr niedrigen thermischen Expansionskoeffizienten.
- Es hat einen sehr niedrigen Reibungskoeffizienten.
Anwendungen
- Die bekannteste tägliche Verwendung ist im Schmuck.
- Aufgrund seiner Härte ist es ein ausgezeichnetes Schleifmaterial, so dass es auf die Oberfläche des Schneid- und Polierens von Metallen, Steinen usw. hinzugefügt wird.
- Aufgrund seiner thermischen Eigenschaften wird es bei der Herstellung von Wärmedissipatoren verwendet.
- Es wird bei der Herstellung von Mikrolagern mit geringer Reibung verwendet.
Graphit
Es ist ein weiterer der bekanntesten Kohlenstoff -Alotrope. Es handelt.
Alle Kohlenstoffatome in Graphit haben SP -Hybridisierung2, Sie haben also eine flache trigonale Struktur. Jeder Kohlenstoff ist mit drei anderen benachbarten Kohlenstoffen verbunden, die Sechsecke bilden, die Benzol ähneln, wobei ein Elektronensystem PI auf der Oberfläche jedes Blattes demokiert, wodurch Graphit leitende Strom macht.
Eigenschaften
- Es ist ein solides schwarzes Material bei Raumtemperatur.
- Es ist Kraftstoff, sodass Sie in Gegenwart von Sauerstoff verbrennen können.
- Graphit ist ein guter elektrischer Leiter.
- Es hat einen hohen Schmelzpunkt.
- Es ist ein weiches Material, das den Eindruck erweckt, rutschig zu sein.
- Es hat einen niedrigen Reibungskoeffizienten.
- Es ist ein guter thermischer Leiter.
Anwendungen
- Es wird häufig bei der Herstellung von Bleistiften zum Schreiben oder zum Zeichnen verwendet.
- Es wird häufig als trockenes Schmiermittel verwendet.
- Aufgrund seiner elektrischen Leitfähigkeit und der geringen chemischen Reaktivität wird es häufig in elektrischen Kontakten in verschiedenen elektronischen Geräten verwendet.
- Es wird in Elektroden zur chemischen Analyse verwendet.
Graphen
 Graphenstruktur
Graphenstruktur Graphen ist nichts anderes als ein Blatt isoliertes Graphit. Es wird als zweidimensionaler Kristall definiert und wird erhalten, indem die Graphitschichten mit Klebeband getrennt werden. Graphen hat einzigartige Eigenschaften, die es von Graphit unterscheiden, obwohl sie in der Struktur sehr ähnlich sind.
Kann Ihnen dienen: Bier-Lambe-GesetzEigenschaften
- Hohe elektrische und thermische Leitfähigkeit.
- Es ist ein elastisches und flexibles Material, aber gleichzeitig mit hoher Härte und Widerstand.
- Für eine einzelne Kohlenstoffatomdicke ist es ein völlig transparentes Material.
- Es kann Strom durch Sonneneinstrahlung erzeugen.
Anwendungen
- Flexible Bildschirme.
- Flexible elektronische Schaltkreise.
- Antikorrosive Bedeckungen.
- Sehr effiziente Sonnenkollektoren.
- DNA -Sequenzierungssysteme.
- Hochgenauige Biosensoren.
Jungs oder Nanokarbon
Die Jungs sind geschlossene molekulare Strukturen, die nur durch Kohlenstoffatome gebildet werden, in denen Anordnungen in Form von Ringen von 4 bis 7 Mitgliedern vorgestellt werden.
Abhängig von ihrer Größe und Form werden in der Regel verschiedene Arten von Jungs unterschieden:
Buckminsterfulerane (c60)
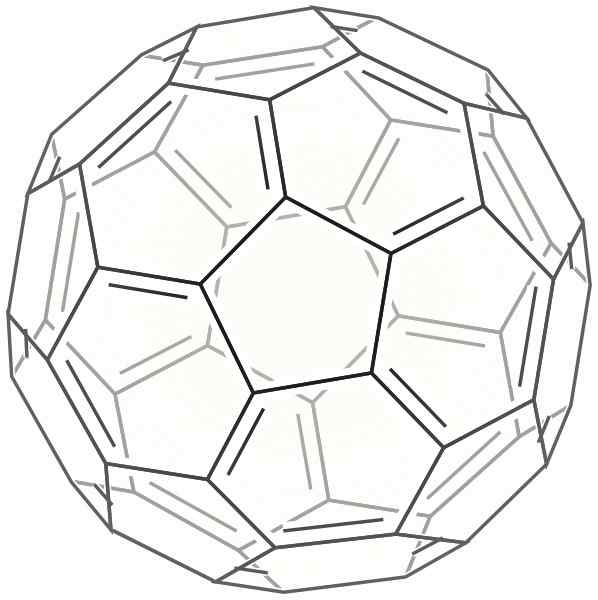 2D Buckminsterfulera Skelett
2D Buckminsterfulera Skelett Dies ist wie eine Kugel geformt, die einem Fußball -Ball sehr ähnlich ist. Es wird auch Bucky Ball genannt.
Eigenschaften
- Hohe elektrische und thermische Leitfähigkeit
- Hoher Spannungsbeständigkeit.
- Sie bilden ein sehr duktiles Material.
- Sie sind relativ inert gegen chemische Reaktionen.
Anwendungen
- Antivirale
- Antioxidantien
- Systeme für Arzneimittelverabreichung
Kohlenstoff-Nanoröhren
 Struktur eines Kohlenstoffnanotubus, bei dem alle Kohlenstoffatome durch nicht -polare kovalente Bindungen zusammen vereint sind
Struktur eines Kohlenstoffnanotubus, bei dem alle Kohlenstoffatome durch nicht -polare kovalente Bindungen zusammen vereint sind Diese bilden die Basis und den Beginn der Nanotechnologie. Sie sind lange Schläge mit tubulärer Form und sind heute eines der am meisten untersuchten Materialien durch die unzähligen Anwendungen ihrer einzigartigen Eigenschaften.
Eigenschaften
Sie haben die gleichen grundlegenden Eigenschaften von Bucky -Bällen, aber wenn sie verlängert werden, sind sie bessere Stromtreiber in axialer Richtung.
Anwendungen
- Bei der Herstellung von nanokomponierten Materialien mit einzigartigen mechanischen, thermischen und elektrischen Eigenschaften.
- Molekulare Elektroniksysteme.
- Hochempfindlichkeit Biosensoren.
- Energiespeichersysteme.
Graphenylen
Dieses alotrope hat eine zweidimensionale Glasstruktur, die Graphen sehr ähnlich ist, jedoch durch Biphenileneinheiten mit Ringen von vier Mitgliedern zwischen den Ringen von sechs, anstatt nur hexagonale Arrangements zu enthalten.
Graphit aa '
Dies ist eine Kohlenstoffform, die 2008 entdeckt wurde. Es ist eine spezielle Art von Graphit, die sich nur so unterscheidet, wie die Graphitblätter auf den anderen gestapelt sind. Es handelt sich um eine metastabile Graphitform, die die Bildung und Eigenschaften einiger Kohlenstoffnanoröhren mehrerer Schichten erklären kann.
Graphenylen
Graphenylen ist ein neuer kürzlich entdeckter Karbonotrop. Sie bestehen aus einer zweidimensionalen Diamantform, die durch Komprimieren von Graphit bei sehr hohen Drücken erhalten wird. Dies führt dazu, dass Graphitblätter miteinander verbunden sind und einen Diamanten von nur wenigen dicken Kohlenstoffatomen bilden.
Amorphes Kohlenstoff
Es besteht im Allgemeinen aus einer Mischung aus verschiedenen Kohlenstoffformen in verschiedenen Anteilen. Nanoröhren können oder andere Arten von Jungs, Graphit usw. enthalten. Es kommt in natürlichen Proben wie Mineral oder Holzkohle vor, die durch Holzpyrolyse verursacht werden.
Es wird hauptsächlich als Kraftstoff bei Heizung, Energieerzeugung oder Lebensmittelkochen verwendet.
Glaskohlenstoff
Es handelt sich um eine Kohlenstoffform, die durch Erhitzen einiger organischer Vorläufer bei hohen Temperaturen erhalten wird. Es ist ein sehr resistentes Material bei hohen Temperaturen und chemischen Angriffen durch Säure und Sauerstoff. Es ist auch unvollständig für Gase.
- « 80 wissenschaftliche Phrasen berühmter Wissenschaftler
- 100 müde Sätze über Leben, Liebe und Glück »

