Amine

- 1110
- 309
- Rieke Scheer
Was sind die Amine?
Der Amine Sie sind organische Verbindungen, die aus Ammoniak stammen. In ihnen gibt es kovalente Gewerkschaften zwischen Kohlenstoff und Stickstoff. Natürlich ist das Stickstoffmolekül kinetisch inert; Dank der biologischen Fixierung wird es jedoch zu Ammoniak, was wiederum nach nachfolgenden Alkylierungsreaktionen leidet.
Wenn das Ammonak. Diese Kohlenstoffe können durchaus von einer Mietgruppe (R) oder Aryl (AR) stammen. Somit gibt es aliphatische Amine (linear oder verzweigt) und aromatisch.
Die Amine sind stärkere organische Basen als das gleiche Ammoniak. Sie sind leicht von der Pflanzenmasse abzunehmen und haben im Allgemeinen starke Wechselwirkungen mit der neuronalen Matrix von Organismen. Daher bestehen viele Medikamente und Medikamente aus Aminen mit komplexen Strukturen und Substituenten.
Aminstruktur
 Allgemeine Formel für einen Amin. Quelle: Mache, Wikimedia Commons.
Allgemeine Formel für einen Amin. Quelle: Mache, Wikimedia Commons. Obwohl es je nach Art von R variiert, ist die elektronische Umgebung des Stickstoffatoms für alle gleich: tetraedrisch. Da jedoch ein paar Elektronen nicht am Stickstoffatom (··) geteilt werden, wird die molekulare Geometrie Pyramiden. Dies ist so bei Ammoniak und Aminen.
Aminas können sowohl mit einem Tetraeder als auch mit Kohlenstoffverbindungen dargestellt werden. So nh3 und Ch4 Sie werden wie Tetraeder gezeichnet, wo sich das Paar (··) in einem der Eckpunkte über dem Stickstoff befindet.
Beide Moleküle sind aquiral; Sie beginnen jedoch, Chiralität zu präsentieren, wenn ihr H ersetzt. Die Amina r2NH ist aquiral, wenn die beiden R unterschiedlich sind. Es fehlt jedoch eine Konfiguration, um ein Enantiomer von einem anderen zu differenzieren (wie es mit den chiralen Kohlenstoffzentren passiert).
Dies liegt daran, dass die Enantiomere:
R2N-H | H-nr2
Sie werden mit einer Geschwindigkeit ausgetauscht, so dass keiner isoliert weder isoliert werden kann; und daher werden die Strukturen der Amine als aquirale angesehen, selbst wenn alle Substituenten im Stickstoffatom unterschiedlich sind.
Amineigenschaften
Polarität
Die Amine sind seit der Amino NH -Gruppe polare Verbindungen2, Für ein Atom aus elektonegativem Stickstoff trägt es zum Dipolmoment des Moleküls bei. Beachten Sie, dass Stickstoff die Fähigkeit hat, Wasserstoffbrückenbindungen zu spenden, die im Allgemeinen hohe Siede- und Fusionspunkte haben.
Physikalische Eigenschaften
In der Welt der Chemie entsteht beim Sprechen über einen Amin die unfreiwillige Akt, seine Nase zu bedecken. Dies liegt daran, dass sie im Allgemeinen normalerweise unangenehme Gerüche haben, von denen einige der von faulen Fischen erscheinen.
Es kann Ihnen dienen: Maillard ReaktionDarüber hinaus haben flüssige Amine normalerweise gelbliche Farbtöne, die das visuelle Misstrauen erhöhen, das sie erzeugen.
Wasserlöslichkeit
Die Amine sind in Wasser tendenziell unlöslich. Je sperriger oder langer die R -Gruppen, desto weniger ihre Löslichkeit im Wasser wird sein.
Wenn sich jedoch eine Säure in der Mitte gibt, wird die Löslichkeit durch die Bildung der sogenannten Aminsalze erhöht. In ihnen hat Stickstoff eine positive teilweise Belastung, die Elektrostern für die Anion- oder Säure -Konjugat -Base anzieht.
Basizität
Amine sind stärkere organische Basen als Ammoniak. Je größer die elektronische Dichte rund um das Stickstoffatom ist, desto grundlegender wird es sein; Das heißt, die Säuren des Medium. Wenn das Amin sehr einfach ist, kann es den Proton sogar aus den Alkoholen schnappen.
Typen (primär, sekundär, tertiär)
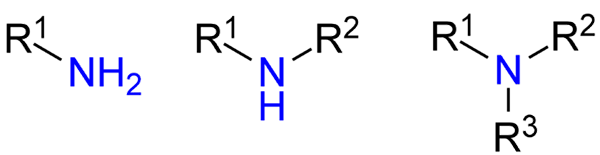 Arten von Aminen. Quelle: Jü über Wikipedia.
Arten von Aminen. Quelle: Jü über Wikipedia. Obwohl sie nicht formell vorgestellt wurden, wurde auf primäre, sekundäre und tertiäre Amine (oberes Bild von links nach rechts) Bezug genommen, obwohl sie von links nach rechts).
Primäramine (RNH2) sind monosustuidas; Die sekundäre (r2NH) werden mit zwei R -Alcomile- oder Arylgruppen aufgelöst; und das Tertiär (r3N) sind trisustuid und fehlt Wasserstoff.
Alle vorhandenen Amine stammen aus diesen drei Typen, sodass ihre Vielfalt und Wechselwirkungen mit der biologischen und neuronalen Matrix enorm sind.
Im Allgemeinen könnte erwartet werden, dass tertiäre Amine die grundlegendsten sein; Eine solche Aussage kann jedoch nicht gemacht werden, ohne die Strukturen von R zu kennen.
Bildung von Aminen
Ammoniakalkylierung
Zuerst wurde erwähnt, dass Amine aus Ammoniak stammen; Daher ist der einfachste Weg, sie zu formen. Dazu wird ein Ammoniaküberschuss mit einem Alkylhalogenid reagiert, gefolgt von der Zugabe einer Basis zur Neutralisierung des Aminsalzes:
NH3 + Rx => rnh3+X- => Rnh2
Beachten Sie, dass diese Schritte zu einer primären Amina führen. Sekundäre und sogar tertiäre Amine können ebenfalls gebildet werden, sodass die Leistung für ein einzelnes Produkt abnimmt.
Einige Trainingsmethoden wie Gabriels Synthese ermöglichen es, primäre Amine zu erhalten, damit andere unerwünschte Produkte nicht gebildet werden.
Kann Ihnen dienen: Ethylalkohol: Struktur, Eigenschaften, Verwendungen, ErhaltenEbenso können Ketone und Aldehyde in Gegenwart von Ammoniak und Primäraminen reduziert werden, um sekundäre und tertiäre Amine zu führen.
Katalytische Hydrierung
Nitroverbindungen können in Gegenwart von Wasserstoff und einem Katalysator reduziert werden, um sich in ihre entsprechenden Amine zu verwandeln.
Arno2 => Rnah2
Die Nitrilos, RC≡N und die Amidas, rconr2, Sie werden auch reduziert, um primäre bzw. tertiäre Amine zu geben.
Nomenklatur
Wie werden die Amine benannt?? Meistens werden sie nach R, der Aquilo oder der Arylgruppe benannt. Zum Namen R, abgeleitet von seinem Alkane, wird ihm am Ende das Wort "Amin" hinzugefügt.
So, ch3CH2CH2NH2 Es ist Propilamin. Andererseits kann es nur zum Alkan und nicht als R -Gruppe ernannt werden: Propanamin.
Der erste Weg, um sie zu benennen, ist genauso bekannt und verwendet.
Wenn es zwei NH -Gruppen gibt2, Der Alkane wird ernannt und die Positionen der Aminogruppen sind aufgeführt. So, h2Nch2CH2CH2CH2NH2 Es heißt: 1,4-Butanodiamin.
Wenn es sauerstoffhaltige Gruppen wie OH gibt, sollte NH Priorität gegeben werden2, das wird als Substituent ernannt. Zum Beispiel Hoch2CH2CH2NH2 heißt: 3-Aminopropanol.
Und in Bezug auf sekundäre und tertiäre Amine werden die N -Buchstaben gemacht, um die R -Gruppen anzuzeigen. Die längste Kette hält den Namen der Verbindung. So, Cho3NHCH2CH3 Es heißt: n-methylethylamin.
Verwendung von Aminen
Farbstoffe
Primäre aromatische Amine können als Ausgangsmaterial für die Synthese von Azofarbstoffen dienen. Anfänglich reagieren die Amine auf Diazoniumsalze, die durch Dachkopulation (oder Diazoikumkupplung) die Verbindungen bilden,.
Aufgrund der Intensive seiner Färbung werden sie in der Textilindustrie als Färbenmaterial verwendet. Zum Beispiel: Methylorange, brauner 138 direkter, gelb Sonnenuntergang FCF und Ponceau.
Drogen und Drogen
Viele Medikamente wirken mit Agonisten und Antagonisten natürlicher Aminneurotransmitter. Beispiele:
-Chloropheniramin ist ein Antihistaminikum, das bei der Kontrolle allergischer Prozesse aufgrund der Einnahme einiger Lebensmittel, Heusefieber, Insektenstich usw. verwendet wird.
-Chlorpromazin ist ein Beruhigungsmittel, kein Schlafinduktor. Es lindert Angst und wird sogar bei der Behandlung einiger psychischer Störungen eingesetzt.
-Ephedrin und Phenymphedrin werden als Abneigung des Atemwegs verwendet.
Kann Ihnen dienen: Osmolarität-Amitriptalin und Imipramin sind tertiäre Amine, die bei der Behandlung von Depressionen verwendet werden. Trizyklischer Antidepressiva werden durch ihre Struktur klassifiziert.
-Opioidanalgetika wie Morphin, Codeline und Heroin sind tertiäre Amine.
Gasbehandlung
Mehrere Amine, einschließlich Diglycolamin (DGA) und Diätolamin (DEA), werden zur Eliminierung von Kohlendioxidgasen (CO2) und Wasserstoffsulfid (H)2S) in Erdgas und Raffinerien vorhanden.
Landwirtschaftliche Chemie
Metilamine sind Zwischenverbindungen in der Synthese von Chemikalien, die in der Landwirtschaft verwendet werden, wie Herbizide, Fungizide, Insektizide und Biozide.
Harzherstellung
Metilamine werden während der Ausarbeitung von Ionenaustauschharzen verwendet, die bei der Wasserdionisierung verwendet werden können.
Tierische Nährstoffe
Trimethylamin (TMA) wird hauptsächlich in der Produktion von Chloridchlorid verwendet, einem Vitamin B -Supplement, das bei Hühnern, Truthähne und Schweinen verwendet wird.
Gummiindustrie
Das Dimethylamin -Öl (DMA) ist ein Emulgator für die Verwendung in der synthetischen Gummiproduktion. DMA wird direkt als Polymerisationsmodifikator in der Dampfphase der Butadien und als Stabilisator des Naturkautschuk -Latex anstelle des Ammoniaks verwendet
Lösungsmittel
Dimethylamin (DMA) und Monomethylamin (MMA) werden verwendet, um Timethylformamid polare polare Lösungsmittel (DMF), Dimethylacetamid (DMAC) und N-methylpirrolidon (NMP) (NMP) zu synthetisieren.
Zu den DMF -Anwendungen gehören: Urethanbeschichtung, Acrylgarnlösungsmittel, Reaktionslösungsmittel und Extraktionslösungsmittel.
DMAC wird zur Herstellung von Farbstoffen und Garnlösungsmittel verwendet. Schließlich wird NMP zur Verfeinerung von Schmierölen, Pickups und Emaillebeschichtung verwendet.
Beispiele für Amine
Kokain
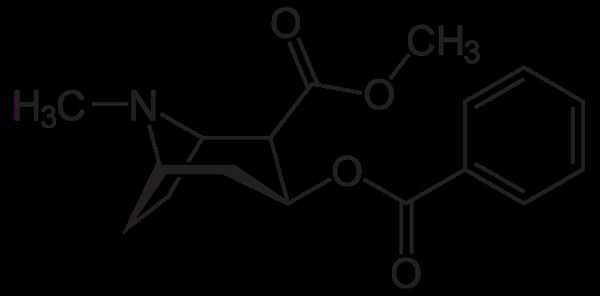 Kokainmolekül. Neurotokeker, Wikimedia Commons
Kokainmolekül. Neurotokeker, Wikimedia Commons Kokain wird in bestimmten Arten von Augenoperationen, Ohren und Hals als Lokalanästhetikum verwendet. Wie gesehen ist es ein tertiäres Amin.
Nikotin
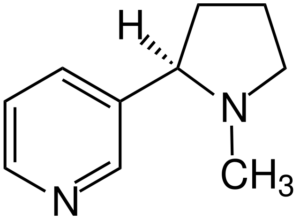 Nikotinmolekül. Quelle: Jü [CC BY-SA 4.0 (https: // creativecommons.Org/lizenzen/by-sa/4.0)] aus Wikimedia Commons
Nikotinmolekül. Quelle: Jü [CC BY-SA 4.0 (https: // creativecommons.Org/lizenzen/by-sa/4.0)] aus Wikimedia Commons Nikotin ist das primäre Mittel der Tabaksucht und chemisch ein tertiäres Amin. Der im Tabakrauch vorhandene Nikotin wird schnell absorbiert und ist sehr giftig.
Morphium
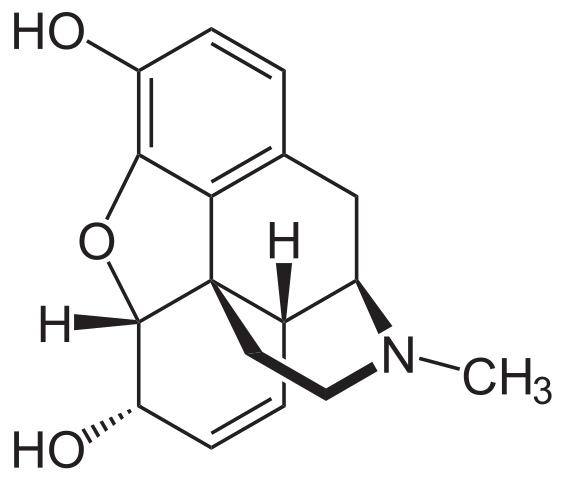 Morphinmolekül. Quelle: Neurotoger [Public Domain] aus Wikimedia Commons
Morphinmolekül. Quelle: Neurotoger [Public Domain] aus Wikimedia Commons Es ist eine der effektivsten Analgetika, um Schmerzen zu lindern, insbesondere Krebs. Es ist wieder ein tertiäres Amin.
Serotonin
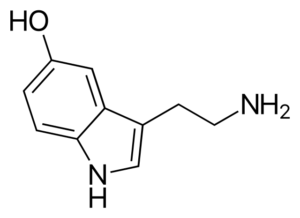 Serotoninmolekül. Quelle: Harbin [Public Domain] aus Wikimedia Commons
Serotoninmolekül. Quelle: Harbin [Public Domain] aus Wikimedia Commons Serotonin ist ein Aminneurotransmitter. Bei depressiven Patienten ist die Konzentration des Hauptmetaboliten von Serotonin verringert. Im Gegensatz zu den anderen Aminen ist dies primär.
Verweise
- Methylamine: Verwendungen und Anwendungen. Erholt von: Chemours.com
- Transparenzmarktforschung. (S.F.). Amine: Wichtige Fakten und Verwendung. Wiederhergestellt von: TransparenzmarkeTresearch.com

