Trainingsanion, Eigenschaften und Typen
- 743
- 55
- Lewis Holzner
A Anion Es ist alles chemische Spezies mit negativer Belastung, zusätzlich zu einer der beiden Arten bestehender Ionen. Die negative Belastung entsteht aus der Tatsache, dass sie im Vergleich zur neutralen Form der Spezies einen Überschuss an Elektronen aufweist. Für jedes zusätzliche Elektron nimmt die negative Belastung in einer Einheit zu.
Die negative Belastung kann sich in einem oder mehreren Atomen befinden und seinen Einfluss auf ein Molekül in seiner Gesamtheit abdecken. Durch die Vereinfachung wird sie unabhängig von der Last (-) als Anion der gesamten Spezies, Verbindung oder Molekül betrachtet.
 Anionen. Quelle: Gabriel Bolívar.
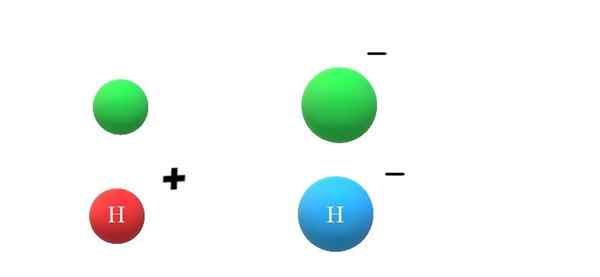
Anionen. Quelle: Gabriel Bolívar. Wenn eine neutrale Spezies ein Elektron gewinnt-, Dies wird auch die Zunahme seines Atomradius (überlegenes Bild, mit grünen Kugeln) tragen). X und x- Sie unterscheiden sich stark in ihren Eigenschaften und in der Art und Weise, wie sie mit ihrer Umgebung interagieren.
Wenn es jetzt soll+ oder h-, bzw. Das Kation h+ Es ist das Wasserstoffionen, auch Proton genannt; und h- Es ist das Hydrid -Anion, das "Einfachste" aller bekannten Anionen.
[TOC]
Ausbildung eines Anion
Die Bildung eines Anion kann leicht in der Theorie erklärt werden; Experimentell kann es jedoch zu einer Herausforderung werden, insbesondere wenn Sie reine wollen, ohne dass positive Gebühren von Ihren negativen Gebühren angezogen werden.
Formelle Lasten und weniger Links
Ein Anion wird gebildet, wenn in einem Atom ein Überschuss oder Elektronengewinn vorliegt. Diese Verstärkung kann durch Verwendung formaler Lasten in einer Lewis -Struktur bestimmt werden. Auch durch die vorherige Methode können Sie genau wissen, welches Atom oder die Gruppe von ihnen die negative Belastung enthält.
Kann Ihnen dienen: Acetonitril (C2H3n)Wenn Atome kovalente Bindungen bilden, kann die Verteilung der Elektronen, obwohl es gerecht ist, einen teilweisen Verlust von Elektronen geben. In diesem Sinne bilden die weniger Verbindungen die elektronenfreisten Paare, die sie haben werden, und weisen daher negative Lasten auf.
Betrachten Sie zum Beispiel das Ammoniakmolekül NH3. Der NH3 Es ist neutral und hat daher keine elektrischen Gebühren. Wenn ein H entfernt würde, wurde ein N-H-Glied gebrochen, das NH-Anion würde erhalten2-. Zeichnen der Lewis -Struktur und Berechnung der formalen Last des N Sie können dies überprüfen.
Nach dem Bruch weiterer N-H-Links haben Sie jetzt den NH-Anion2-; und das letzte h zu beseitigen, wird der Anion n endlich erhalten3-, Anion Nitruro genannt. Stickstoff hat nicht mehr, wie man mehr Elektronen erhält, und seine Last -3 ist die negativste, die er erreichen kann. Seine Orbitale geben nicht mehr.
Reduzierungen
Ein Anion kann ein Produkt einer Reduktion bilden: Gewinne Elektronen, die zu einer anderen Spezies oxidieren, was sie verliert. Sauerstoff zum Beispiel repräsentiert diese Art der chemischen Reaktion sehr gut.
Wenn Sauerstoff reduziert, zu einer anderen Spezies oxidiert wird und zu Oxidanion wird, oder2-; in unzähligen Mineralien und anorganischen Verbindungen vorhanden.
Physisch
Ein Atom kann Elektronen gewinnen, wenn es sich in einer Gasphase befindet:
X (g) + e- => X-(G)
Diese Art, ein Anion zu bilden.
Eigenschaften
Im Allgemeinen werden die typischen Merkmale eines Anion nachstehend erwähnt, bevor sich seine Typen und Beispiele befassen:
-Ist sperriger als das neutrale Atom, aus dem aus.
Kann Ihnen dienen: Chlordioxid (CLO2): Struktur, Verwendungsmöglichkeiten, Erhalten, Risiken, Eigenschaften-Es kann mehr oder weniger stabil sein, trotz der wachsenden elektronischen Abstoßung zwischen seinen eigenen Elektronen.
-Wenn das Anion von einem kleinen elektronegativen Atom wie Kohlenstoff stammt, ist es sehr reaktiv.
-Setzen Sie starke Dipolmomente.
-Erhöht die Wechselwirkung mit polaren Lösungsmitteln weiter.
-Das monoatomische Anion ist isoliert zum edlen Gas seiner Periode; Das heißt, es hat in seiner Valenzschicht die gleiche Anzahl von Elektronen.
-Es kann die elektronische Wolke eines Nachbaratoms polarisieren und seine externen Elektronen abwerfen.
Leute
Monoatomisch
Wie der Name schon sagt, ist es ein Anion, das aus einem einzigen Atom besteht: Die negative Belastung ist gut lokalisiert. Jede Gruppe in der Periodenzüchter hat charakteristische negative Belastungen; Und weil sie Anionen sind, sind sie die Nicht -Metalle, die sich in Block P befinden. Einige Beispiele und ihre Namen sind unten:
-Cl-, Chlorid.
-Yo-, Ich zuletzt.
-F-, Fluorid.
-Br-, Bromid.
-ENTWEDER2-, Oxid.
-S2-, Sulfid.
-ER2-, Seleniuro.
-Tee2-, Telururo.
-Po2-, Polyoniuro.
-N3-, Nitruro.
-P3-, Phosphuro.
-As3-, Arseniuro.
-Sb3-, Antimoniuro.
-C4-, Carbid.
-Ja4-, Siliciuro.
-B3-, Boruro.
Oxoanionen
Oxoanionen sind durch eine x = O -Bindung gekennzeichnet.). Sie können auch einen oder mehrere einfache X-O-Links haben.
Einige Oxoanionen mit ihren jeweiligen Namen sind:
-Clo-, Hypochlorit.
-Bruder-, Hipobromito.
-Io-, Hypoyodit.
-Clo2-, Chlorit.
-Clo3-, Chlorat.
-Io3-, Yodato.
-Clo4-, Perchlorat.
-Po43-, Phosphat.
-CO32-, Karbonat.
-Cro42-, Chromat.
-Cr2ENTWEDER72-, Dicromato.
-SW42-, Sulfat.
-S2ENTWEDER32-, Tiosulfat.
-NEIN3-, Nitrat.
-NEIN2-, Nitrit.
-Bo33-, Borat.
-ASO43-, Arseniato.
-Po33-, Phosphit.
-Mne4-, Permanganat.
Organisch
Organische Moleküle haben funktionelle Gruppen, die elektrisch aufgeladen werden können. Als? Durch Bildung oder Bruch kovalenter Bindungen, sehr ähnlich dem Beispiel des NH -Moleküls3.
Kann Ihnen dienen: Eisen (Element): Eigenschaften, chemische Struktur, verwendetEinige organische Anionen sind:
-CH3Gurren-, Acetat.
-HCOO-, Format.
-C2ENTWEDER42-, Oxalat.
-Rcoo-, Carboxylat.
-CH3Conh-, Inmidato.
-Ro-, Alcoxid.
-R3C-, Carbanion.
-CH3ENTWEDER-, Metoxid.
Polyiatom
Oxoanionen sind auch poliatomische Anionen, dh sie bestehen aus mehr als einem Atom. Gleiches gilt für organische Anionen. Polyiatom sind jedoch keine der vorherigen Klassifizierungen eingeben. Einige von ihnen sind:
-CN-, Cyanid (hat eine dreifache Verbindung, Cwerbing).
-Ocn-, Cyanat.
-Scn-, Tiocianato.
-NH2-, Amiduro.
-Oh-, Hydroxyl, Hydroxid oder Oxydrillo.
-ENTWEDER2-, Superoxid.
-ENTWEDER22-, Peroxid.
Molekular oder komplex
In organischen Anionen wurden einige negativ belastete funktionelle Gruppen erwähnt. Diese Gruppen können Teil eines großen Moleküls sein, und daher kann Anion eine robuste Verbindung und viele Verbindungen sein. Der einfachste dieser Art von Anionen ist das hypothetische H -Molekül2-.
Zu einem anderen Beispiel dieser Anionen gehören Polysulfuros, sN2-, die aus Ketten mit mehreren S-S-Links bestehen. Ebenso können Metallkoordinationsverbindungen mit negativer Belastung gezählt werden, wie z. B. [COCl4(NH3)2]- - und [Cucl4]2-.
Verweise
- Whitten, Davis, Peck & Stanley. (2008). Chemie. (8. Aufl.). Cengage Lernen.
- Wikipedia. (2019). Anion. Geborgen von: ist.Wikipedia.Org
- Helmestine, Anne Marie, ph.D. (21. März 2019). Common Anions Tabelle und Formelnliste. Erholt von: thoughtco.com
- CK-12 Foundation. (29. Juni 2016). Anionenbildung. Chemistry Librettexts. Erholt von: Chem.Librettexts.Org
- Franziskus e. (2002). Anionen. Clackamas Community College. Abgerufen von: dl.Clackamas.Edu
- Amerikanische physische Gesellschaft. (3. November 2011). Synopsis: der einfachste molekulare Anion. Erholt von: Physik.APS.Org
- « Fernando del Paso Biographie, Stil, Werke und Phrasen
- Anisolstruktur, Eigenschaften, Nomenklatur, Risiken und Verwendung »

