Anisolstruktur, Eigenschaften, Nomenklatur, Risiken und Verwendung
- 2349
- 103
- Medine Kedzierski
Er Anisol oder Metoxibenzol Es ist eine organische Verbindung, die aus einem aromatischen Äther besteht, dessen chemische Formel C ist6H5Och3. Sein körperlicher Zustand ist der einer farblosen Flüssigkeit, die gelbe Färben aufweisen kann. Es ist leicht durch seinen charakteristischen Geruch von Anis zu erkennen.
Es ist dann eine flüchtige Verbindung und nicht sehr hohe Kohäsionskräfte; Übliche Eigenschaften in leichten Ether, die in kleinen versiegelten Behältern aufbewahrt werden. .
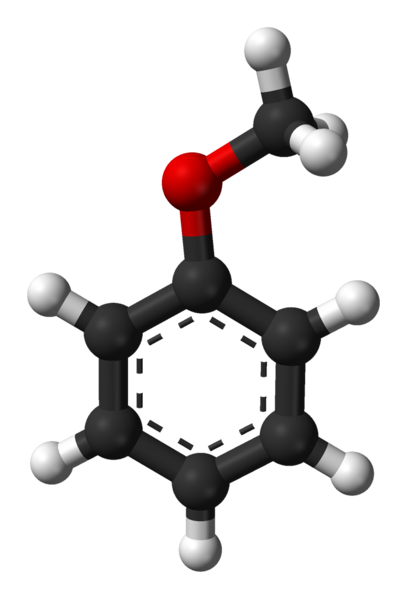
 Anisolmolekül. Quelle: Ben Mills über Wikipedia.
Anisolmolekül. Quelle: Ben Mills über Wikipedia. 6H5- 3 H5-3. Der aromatische Ring und das Vorhandensein von -och3 Als Substituentengruppe namens Metoxi gibt das Anisol eine Nucleophilie, die dem von Benzol und Nitrobenzol überlegen ist. .
Sein charakteristischer Geruch von Anis wurde verwendet, um Kosmetik- und Hygieneprodukte, die einen angenehmen Duft zu erfordern.
[TOC]
Anisolstruktur
Im oberen Bild wird die molekulare Struktur des Anisols mittels eines Kugeln- und Balkenmodells dargestellt. Der aromatische Ring wird geschätzt, dessen Kohlenstoffe SP sind2 3, und seine Hydrogene liegen über oder unter der Ringebene.
Die Bedeutung der -Och -Gruppe3 In der Struktur geht es über das Brechen mit der flachen Geometrie des Moleküls hinaus.
Dipolarem Moment
Dieses Dipolmoment ist auf das Sauerstoffatom zurückzuführen, das die elektronischen Dichten sowohl des aromatischen als auch des Methylrings anzieht. Dank dessen können Anisols Moleküle die halben Dipolo-Kräfte interagieren; Obwohl es keine Möglichkeit gibt, Wasserstoffbrücken zu bilden, weil es ein Ether ist (ROR hat keinen Sauerstoff miteinander verbunden).
. Ebenso sind Londoner Dispersionskräfte vorhanden, abhängig von der molekularen Masse und π -π -Wechselwirkungen zwischen den Ringen selbst.
Kristalle
Anisols Struktur erlaubt es ihm jedoch nicht.. Dies kann auch darauf zurückzuführen sein, dass die elektrostatischen Abstoßungen zwischen benachbarten aromatischen aromatischen Ringen sehr stark sind, wenn intermolekulare Entfernungen reduziert sind.
Daher und nach kristallographischen Studien können Anisolmoleküle in Kristallen bei einer Temperatur von -173 ° C nicht so geordnet werden, dass ihre Ringe ausgesetzt sind; Das heißt3 .
Eigenschaften
Aussehen
.
Geruch
Es riecht leicht ähnlich wie Anissamen.
Geschmack
Süss; Es ist jedoch mäßig giftig, daher ist dieser Test gefährlich.
Molekulare Masse
.
Dichte
0,995 g/ml.
Wasserdampfdichte
3.72 (in Luftbeziehung = 1).
Schmelzpunkt
-.
Siedepunkt
154ºC.
Zündungspunkt
.
475ºC.
Schmiere
.
Oberflächenspannung
34.15 Dins/cm a 30ºC.
Brechung indica
1.5179 bis 20ºC.
Löslichkeit
Schlecht löslich in Wasser (ca. 1 mg/ml). In anderen Lösungsmitteln wie Aceton, Ether und Alkoholen ist es dennoch sehr löslich.
Nucleophilie
Anisols aromatischer Ring ist reich an Elektronen. Dies liegt daran. Folglich wandern mehr Elektronen das aromatische System und erhöhen daher seine Nucleophilie.
Es kann Ihnen dienen: kamphalter Alkohol: Struktur, Formel, Eigenschaften und VerwendungExperimentell wurde die Zunahme der Nucleophilie durch den Vergleich seiner Reaktivität angesichts aromatischer elektrophylischer Substitutionen mit der von Benzol nachgewiesen. Somit wird der bemerkenswerte Effekt der -Och -Gruppe gezeigt3 .
Es sollte auch beachtet werden, dass elektrophile Substitutionen in benachbarten Positionen (-Orto) und gegenüber (-für) zur Metoxi-Gruppe auftreten. Das heißt, dies ist Ortho-für Direktor.
Reaktivität
Anisols aromatische Ring -Nucleophilie ermöglicht es Ihnen bereits, zu sehen, wie seine Reaktivität ist. Die Substitutionen können entweder im Ring (bevorzugt durch ihre Nucleophilie) oder in derselben Metaxi -Gruppe; In letzterem ist der O-CH-Link gebrochen3 Um den -ch zu ersetzen3 von einer anderen alquilischen Gruppe: o-Alquilación.
Daher kann Anisol in einem Alkylierungsprozess eine Gruppe R (Fragment eines anderen Moleküls) akzeptieren, das einen H seines Ringes (C-Lebung) ersetzt oder das CH ersetzt3 Von Ihrer Metoxi -Gruppe. Das folgende Bild zeigt, was gerade gesagt wird:
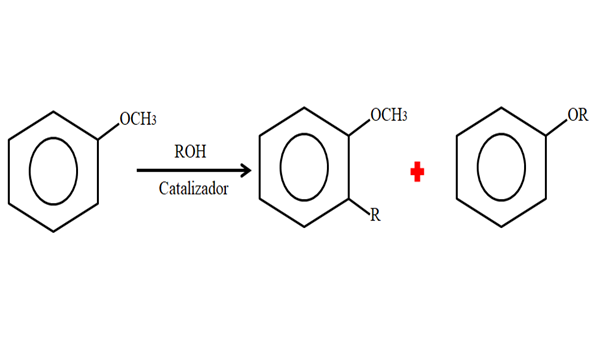 Anisolalkylierung. Quelle: Gabriel Bolívar.
Anisolalkylierung. Quelle: Gabriel Bolívar. Im Bild befindet sich die R -Gruppe in Position -orto, kann aber auch in der Position sein -für -ch3. Wenn o -Alquilación passiert.
Nomenklatur
Der Name 'Anisol' ist der bekannteste und akzeptierte, der höchstwahrscheinlich aus seinem ähnlichen Geruch wie Anis abgeleitet ist. Der Name 'Metoxibenzol' ist jedoch sehr spezifisch, da er einmal die Struktur und Identität dieses aromatischen Äthers festlegt; Dies ist der Name, der der systematischen Nomenklatur regiert.
Ein weiterer weniger gebrauchter Name, aber gleichermaßen gültig, ist der 'Phenylmethylether', der von der traditionellen Nomenklatur bestimmt wird. Dies ist vielleicht der spezifischste Name von allen, da es direkt angibt, welche die beiden strukturellen Teile des Ethers sind: Phoenyl-o-methyl, C6H5-O-ch3.
Risiken
Medizinische Studien konnten die möglichen sterblichen Wirkungen von ANISOL auf den Körper bei niedrigen Dosen noch nicht nachweisen. Wie fast alle chemischen Substanzen erzeugt es jedoch Reizungen, wenn zu Zeit exponiert ist, und in mäßigen Konzentrationen auf Haut, Hals, Lungen und Augen in mäßigen Konzentrationen.
Kann Ihnen dienen: Amagatgesetz: Erklärung, Beispiele, ÜbungenAufgrund der Nucleophilie seines Rings ist ein Teil davon metabolisiert und daher biologisch abbaubar. Infolge dieser Eigenschaft zeigten Simulationen, dass sie sich nicht auf wässrige Ökosysteme konzentriert, da seine Organismen sie zum ersten Mal verschlechtern. Und deshalb können Flüsse, Seen oder Meere Anisol ansammeln.
In den Böden verdunstet es angesichts seiner Volatilität schnell und wird durch Luftströmungen gezogen. Daher wirkt sich weder Gemüsemassen noch Plantagen erheblich aus.
Andererseits reagiert es atmosphärisch mit freien Radikalen und stellt daher kein Risiko einer Luftverschmutzung dar, die wir atmen.
Anwendungen
Organische Synthese
Aus Anisol können andere Derivate durch aromatische elektrophile Substitution erhalten werden. Dies ermöglicht es, als Vermittler für die Synthese von Arzneimitteln, Pestiziden und Lösungsmitteln verwendet zu werden, die ihre Eigenschaften hinzufügen möchten. Synthetische Routen können meistens aus einem bestehen.
Düfte
Zusätzlich zu seiner Verwendung für die organische Synthese kann es direkt als Additiv für Cremes, Salben und Parfums verwendet werden, die Anti -Duftstoffe in solche Produkte einbeziehen.
Verweise
- Morrison, r. T. und Boyd, r, n. (1987). Organische Chemie. 5. Ausgabe. Editorial Addison-Wesley Interamerikaner.
- Carey f. ZU. (2008). Organische Chemie. (Sechste Ausgabe). Mc Graw Hill.
- Graham Solomons t.W., Craig b. Braten. (2011). Organische Chemie. Amine. (10. Ausgabe.). Wiley Plus.
- Nationales Zentrum für Biotechnologie Information. (2019). Anisole. Pubchem -Datenbank, CID = 7519. Erholt von: Pubchem.NCBI.NLM.NIH.Regierung
- Wikipedia. (2019). Anisole. Abgerufen von: in.Wikipedia.Org
- Pereira, Cynthia C. M., De la Cruz, Marcus H. C., & Lachter, Elizabeth R. (2010). Flüssige Phaselation von Anisol und Phenol, die durch Niob -Phosphat katalysiert wurden. Journal of the Brazilian Chemical Society, 21 (2), 367-370. Dx.doi.org/10.1590/S0103-50532010000200025
- Seidel r. W. und Goddard R. (2015). Anisol bei 100 K: die erste Kristallstrukturbestimmung. Crystallogr C struct chem Act. Aug; 71 (Pt 8): 664-6. Doi: 10.1107/S2053229615012553
- Chemische Formulierung. (2018). Metoxibenzol. Wiederhergestellt von: Quimica -Formulierung.com

