Autophagieeigenschaften, Typen, Funktionen, Studien
- 3332
- 546
- Rieke Scheer
Der Autophagie Es ist ein intrazelluläres Abbausystem, das in den Lysosomen aller eukaryotischen Zellen (und den Vakuolen von Hefen) auf konservierte Weise auftritt, auftritt. Das Wort wird im Allgemeinen verwendet, um sich auf den Abbau von Cytosolkomponenten oder die "Teile" der Zelle zu beziehen, die "veraltet" sind oder nicht mehr richtig funktionieren.
Der Begriff Autophagie wurde 1963 an der Rockefeller University von Duve geprägt, der auch die Zellendozytoseprozesse beobachtete und beschrieben hat. Im wahrsten Sinne des Wortes bedeutet das Wort Autophagie "sich selbst konsumieren", obwohl einige Autoren es als "Auto -Kannibalismus" beschreiben.
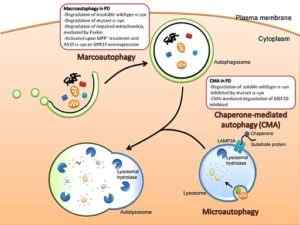 Grafische Darstellung von Makroautophagen und Mikroanophagie (Quelle: Cheung und IP [CC von 3.0 (https: // creativecommons.Org/lizenzen/bis/3.0)] über Wikimedia Commons)
Grafische Darstellung von Makroautophagen und Mikroanophagie (Quelle: Cheung und IP [CC von 3.0 (https: // creativecommons.Org/lizenzen/bis/3.0)] über Wikimedia Commons) Dieses System unterscheidet sich vom Abbau vermittelten Verschlechterung.
Trotz dieser nicht -selektiven Phagozytose hat unterschiedliche Untersuchungen gezeigt, dass Autophagie zahlreiche physiologische und pathologische Auswirkungen hat. Da es in Zeiten der Anpassung an Hunger, während der Entwicklung, zur Beseitigung von eindringenden Mikroorganismen, während des programmierten Zelltods, zur Beseitigung von Tumoren, der Darstellung von Antigenen usw. aktiviert wird, wird es aktiviert.
[TOC]
Eigenschaften
Die Autophagie ist, wie erwähnt, ein Prozess, der durch eine zytoplasmatische Organelle vermittelt wird, die als Lysosom bekannt ist.
Der Prozess „Autophagie“ beginnt mit der Einkapselung der Organelle, die durch eine Doppelmembran abgebaut wird und einen membranösen Körper bildet, der als Autophagosom bekannt ist. Die Autophagosomenmembran schmilzt später mit der lysosomalen Membran oder mit einem späten Endosom.
Jede dieser Schritte zwischen Entführung, Abbau und Befreiung von Aminosäuren oder anderen Komponenten für Recyclingübungen in verschiedenen zellulären Kontexten, was die Autophagie zu einem hoch multifunktionalen System macht.
Autophagie ist ein ziemlich kontrollierter Prozess, da nur markierte Zellkomponenten auf diesen Abbauweg gerichtet sind, und die Markierung tritt im Allgemeinen während der Umgestaltung von Zellen auf.
Zum Beispiel, wenn eine Leberzelle eine Entgiftungsreaktion als Reaktion auf fettlösliche Arzneimittel festlegt, proliferiert ihr glattes endoplasmatisches Retikulum erheblich, und wenn der durch das Arzneimittel erzeugte Stimulus durch das Arzneimittel durch Autophagie übermäßig glattes endoplasmatisches Retikulum abnimmt.
Autophagie -Induktion
Eines der Ereignisse, die autophagische Prozesse am häufigsten auslösen, ist der Hunger.
Kann Ihnen dienen: Exozytose: Prozess, Typen, Funktionen und BeispieleAbhängig vom in Betracht gezogenen Organismus können verschiedene Arten von essentiellen Nährstoffen dieses "Recycling" -System auslösen. In Hefen zum Beispiel, obwohl das Fehlen von Kohlenstoff bestimmter Aminosäuren und Nukleinsäuren Autophagie induzieren kann, ist das Fehlen von Stickstoff der effizienteste Stimulus, der auch für Pflanzenzellen gültig ist.
Obwohl es nicht vollständig verstanden wurde, haben die Zellen spezielle „Sensoren“, um festzustellen, wann ein essentieller Nährstoff oder eine Aminosäure unter sehr geringen Bedingungen ist, und lösen somit den gesamten Recyclingprozess durch die Lysosomen aus.
Bei Säugetieren beteiligen sich einige Hormone an der Regulation (positiv oder negativ) der Autophagie in Zellen, die zu bestimmten Organen gehören, wie Insulin, einige Wachstumsfaktoren oder Interleukine usw.
Leute
Es gibt drei Haupttypen von Autophagie zwischen Eukaryoten: Makroautophagie, Mikroanophagie und Autophagie durch Chaperone vermittelt. Sofern nicht angegeben, bezieht sich der Begriff Autophagie auf Makroautophage.
Obwohl die drei Arten von Autophagie morphologisch unterschiedlich sind, enden alle beim Transport von Substanzen zu Lysosomen für ihren Abbau und ihr Recycling.
Makroautophage
Dies ist eine Art von Autophagie, die vom Training abhängt von novo von phagozytischen Vesikeln, die als Autophagosomen bekannt sind. Die Bildung dieser Vesikel ist unabhängig von der Bildung von "Eigelb" der Membran, da sie durch Expansion gebildet werden.
In Hefen beginnt die Bildung von Autophagosomen an einem bestimmten Ort, der als PAS bekannt ist, während bei Säugetieren viele verschiedene Orte des Cytosols auftreten, die wahrscheinlich mit dem endoplasmatischen Retikulum durch Strukturen verbunden sind, die als "Omegasome" bekannt sind.
Die Größe der Autophagosomen ist sehr variabel und hängt vom Organismus und der Art des Phagozyten -Moleküls oder des organischen Moleküls ab. Kann von 0 variieren.4-0.9 μm Durchmesser in Hefen bis zu 0.5-1.5 μm bei Säugetieren.
Wenn Autophagosom und Lysosomen Membranen mel. Diese Organelle ist dann als Autolisosom bekannt.
Für einige Autoren kann Makroautophagen wiederum in induzierter Autophagie und basaler Autophagie unterklassifiziert werden. Induziertes Makroautophagen wird verwendet, um Aminosäuren nach einer längeren Hungerphase zu produzieren.
Basalmakroautophage.
Kann Ihnen dienen: Lipidflöße: Eigenschaften, Typen, FunktionenMikroanophagie
Diese Art von Autophagie bezieht sich auf den Prozess, in dem der zytoplasmatische Gehalt durch Invaginationen, die in der Membran der Organelle auftreten, in das Lysosom eingeführt wird.
Einmal in das Lysosom eingeführt, schweben die von diesen Invaginationen erzeugten Vesikel frei im Lumen, bis sie aufgelistet sind und der Inhalt freigegeben und durch bestimmte Enzyme abgebaut wird.
Durch Chaperon vermittelte Selbstrumente
Diese Art von Autophagie wurde nur für Säugetierzellen berichtet. Im Gegensatz zur Makroautophagie und Mikroanophagie, bei denen einige zytosolische Teile unspezifische Phagozythe sind.
Einige Forscher haben festgestellt, dass dieses Pentapeptide -Motiv mit der KFERQ -Sequenz zusammenhängt und dass es in mehr als 30% der zytosolischen Proteine beträgt.
Es heißt "Chaperonas vermittelt", da Chaperonproteine dafür verantwortlich sind, diesen Grund aufrechtzuerhalten, um ihre Erkennung zu erleichtern und die Faltung des Proteins darauf zu vermeiden.
Proteine mit diesem Etikett werden in das lysosomale Lumen transloziert und es werden abgebaut. Viele der Abbau -Substrate sind glykolytische Enzyme, Transkriptionsfaktoren und deren Inhibitoren, Calciumgewerkschaftsproteine oder Lipide, Proteosomenuntereinheiten und einige Proteine, die mit dem vesikulären Verkehr beteiligt sind.
Sowie die beiden anderen Arten von Autophagie, Chaperon -vermittelte Autophagie.
Funktionen
Eine der Hauptfunktionen des Autophage.
Dank der Beobachtung elektronischer Mikrofotografien von Lysosomen in Säugetierzellen wurde das Vorhandensein von Peroxisomen und Mitochondrien in diesen nachgewiesen.
In einer Leberzelle beispielsweise beträgt die durchschnittliche Lebenszeit einer Mitochondrien 10 Tage, wonach diese Organelle von den Lysosomen phagoziert wird, wo sie verschlechtert und ihre Komponenten für verschiedene Stoffwechselzwecke recycelt werden.
Unter geringer Konzentration von Ernährungsstoffen können Zellen die Bildung von Autophagosomen auslösen, um Cytosolteile selektiv zu erfassen.
Kann Ihnen dienen: Erythropoese: Stufen und ihre Eigenschaften, Regulierung, StimulanzienFunktionen in Gesundheit und Entwicklung
Die Autophagie hat wichtige Funktionen bei der Umstrukturierung von Zellen im Differenzierungsprozess, da sie daran beteiligt ist, zytosolische Teile zu verworfen, die zu bestimmten Zeiten nicht erforderlich sind.
Es hat auch wichtige Auswirkungen auf die Zellgesundheit, da es Teil der Abwehrmechanismen gegen Viren und eindringende Bakterien ist.
Yoshinori Ohsumi Studies
Yoshinori Ohsumi, ein japanischer Forscher im Jahr 2016 mit dem Nobelpreis für Physiologie und Medizin, beschrieb die molekularen Mechanismen der Selbstverteidigung in Hefen und untersuchten das Stoffwechsel viele Proteine und Vakuolen dieser einzelligen Organismen.
In seinen Werken identifizierte OHSUMI nicht nur die in den Prozess beteiligten Proteine und Routen, sondern auch, wie die Autophagie -Route dank der Wirkung von Proteinen reguliert wird, die in der Lage sind, verschiedene Stoffwechselzustände zu „zensieren“.
Seine Arbeit begann mit präzisen mikroskopischen Beobachtungen während intensiver Abbauereignisse. Vakuolen gelten als Speicherstellen von "Müll" und Zellabfällen von Hefen.
Durch Beobachtung von Hefen mit defekten mutierten Genotypen für verschiedene oder hypothetisch verwandte Gene, die mit Autophagie zusammenhängen (als Gene bezeichnet Atg) Dieser Forscher und seine Mitarbeiter haben es geschafft, das autophagische Hefesystem auf genetischer Ebene zu beschreiben.
Anschließend bestimmte diese Forschergruppe.
Dank der Werke von Yoshinori Ohsumi verstehen wir heute besser die molekularen Aspekte der Autophagie sowie ihre wichtigen Auswirkungen auf die korrekte Funktionsweise der Zellen und Organe, aus denen uns besteht.
Verweise
- Alberts, geb., Johnson, a., Lewis, J., Morgan, d., Raff, m., Roberts, k., & Walter, p. (2015). Biologie des Zellmolekulares (6. Aufl.). New York: Garlandwissenschaft.
- Klionssky, d. J., & Emr, s. D. (2000). Autophagie als regulierter Weg des zellulären Abbaus. Wissenschaft, 290, 1717-1721.
- Mizushima, n. (2007). Autophagie: Prozess und Funktion. Gene & Entwicklung, einundzwanzig, 2861-2873.
- Mizushima, Noboru & Komatsu, m. (2011). Autobahn: Erneuerung von Zellen und Geweben. Zelle, 147, 728-741.
- Rabinowitz, j. D., & Weiß und weiß und. (2010). Autophagie und Stoffwechsel. Wissenschaft, 330, 1344-1348.
- « Mayate -Eigenschaften, Lebensraum, Reproduktion, biologische Kontrolle
- Merkmale von Tarantula, Lebensraum, Arten, Verhalten »

