Bioelements Klassifizierung (primär und sekundär)
- 4209
- 435
- Nick Laurén
"Bioelement„Es ist ein Begriff, der verwendet wird, um sich auf die wichtigsten chemischen Elemente zu beziehen. In einigen Klassifizierungen werden diese in Primärelemente und sekundäre Elemente unterteilt.
Von den 87 bekannten chemischen Elementen, nur 34 organische Substanz, und es ist bekannt, dass 17 dieser 34 fürs Leben wirklich unverzichtbar sind. Darüber hinaus machen fünf von diesen 17 unverzichtbaren Elementen mehr als 90% der Angelegenheit aus, die lebende Organismen umfasst.
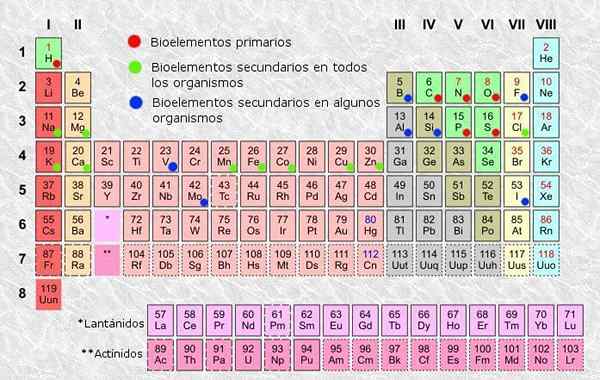
 Die periodische Tabelle der Elemente, die primären und sekundären Bioelemente sind ebenfalls angegeben (Quelle: Alejandro Porto [CC BY-SA 3.0 (https: // creativecommons.Org/lizenzen/by-sa/3.0)] über Wikimedia Commons)
Die periodische Tabelle der Elemente, die primären und sekundären Bioelemente sind ebenfalls angegeben (Quelle: Alejandro Porto [CC BY-SA 3.0 (https: // creativecommons.Org/lizenzen/by-sa/3.0)] über Wikimedia Commons) Die sechs Hauptelemente in organischer Substanz sind Wasserstoff (H, 59%), Sauerstoff (oder 24%), Kohlenstoff (C, 11%), Stickstoff (N, 4%), Phosphor (P, 1%) und Schwefel (Schwefel (Schwefel S, von 0,1 bis 1%).
Diese Prozentsätze spiegeln die Menge der Atome jedes Elements in Bezug auf die Gesamtzahl der Atome wider, die lebende Zellen bilden, und diese sind diejenigen, die als "primäre Bioelemente" bekannt sind.
Sekundäre Bioelemente sind in einem viel geringeren Verhältnis und sind Kalium (k), Magnesium (mg), Eisen (Glaube), Calcium (Ca), Molybdän (MO), Fluor (F), Chlor (Chlor (Chlor (CL)), das Natrium (Na), Jod (I), Kupfer (Cu) und Zink (Zn).
Sekundärelemente sind normalerweise Cofaktoren bei katalytischen Reaktionen und nehmen an zahlreichen biochemischen und physiologischen Prozessen teil, die Organismen von Organismen innewohnt.
[TOC]
Primäre Bioelemente

Kohlenstoff-, Wasserstoff- und Sauerstoffatome sind die strukturelle Grundlage der Moleküle, aus denen organischer Substanz besteht, inzwischen Stickstoff, Phosphor und Schwefel mit den verschiedenen Biomolekülen interagieren, um chemische Reaktionen zu verursachen.
Wasserstoff
Wasserstoff ist ein chemisches Element, das bei Raumtemperatur (25 º c) gasförmige Form vorliegt. Er kann nur in einem festen oder flüssigen Zustand bei Raumtemperatur vorhanden sein, wenn es mit anderen Molekülen verbunden ist.
Es wird angenommen, dass Wasserstoffatome zu den ersten Atomen gehörten, die das primitive Universum bildeten. Die gehandhabten Theorien schlagen vor, dass die im Kern von Wasserstoffatomen enthaltenen Protonen mit den Elektronen anderer Elemente zu verbinden, um komplexere Moleküle zu bilden.
Wasserstoff kann chemisch mit fast jedem anderen Element kombiniert werden, um Moleküle zu bilden, darunter Wasser, Kohlenhydrate, Kohlenwasserstoffe usw.
Dieses Element ist für die Bildung von Bindungen verantwortlich.
Kann Ihnen dienen: Easmotherium Sibiricum: Eigenschaften, Lebensraum, FossilienKohlenstoff
Kohlenstoff bildet den Kern vieler Biomoleküle. Ihre Atome können kovalent mit vier anderen Atomen verschiedener chemischer Elemente und auch mit sich selbst kombiniert werden, um die Struktur großer Komplexitätsmoleküle zu bilden.
Kohlenstoff neben Wasserstoff ist eines der chemischen Elemente, die eine größere Anzahl verschiedener chemischer Verbindungen bilden können. So sehr, dass alle Substanzen und Verbindungen, die als "organische" katalogisiert sind, Kohlenstoffatome in ihrer Hauptstruktur enthalten.
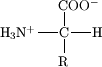 Allgemeine Struktur einer Aminosäure (Quelle: Benutzer: PPFK [CC BY-SA 3.0 (http: // creativecommons.Org/lizenzen/by-sa/3.0/)] über Wikimedia Commons)
Allgemeine Struktur einer Aminosäure (Quelle: Benutzer: PPFK [CC BY-SA 3.0 (http: // creativecommons.Org/lizenzen/by-sa/3.0/)] über Wikimedia Commons) Zu den wichtigsten kohlensäurehaltigen Molekülen von Lebewesen gehören Kohlenhydrate (Zucker oder Saccharide), Proteine und ihre Aminosäuren, Nukleinsäuren (DNA und RNA), Lipide und Fettsäuren unter anderem.
Sauerstoff
Sauerstoff ist ein gasförmiges Element und am häufigsten in der gesamten Erdkruste. Es ist in vielen organischen und anorganischen Komponenten vorhanden und bildet Verbindungen mit fast allen chemischen Elementen.
Es ist verantwortlich für die Oxidation von chemischen und Verbrennungsverbindungen, die auch unterschiedliche Oxidationsformen sind. Sauerstoff ist ein sehr elektronegatives Element, ist Teil des Wassermoleküls und beteiligt sich am Atemprozess vieler Lebewesen.
Reaktive Sauerstoffspezies sind für oxidativen Stress in Zellen verantwortlich. Es ist sehr häufig, die durch oxidierenden Verbindungen zu Makromolekülen im Innenraum von Zellen zu beobachten, da diese die Zellreduktionsinnere aus dem Zellreduzierungen auskommen.
Stickstoff
Stickstoff ist auch überwiegend in gasförmiger Form und bildet etwa 78% der Erdatmosphäre. Es ist ein wichtiges Element in der Ernährung von Pflanzen und Tieren.
Bei Tieren ist Stickstoff ein grundlegender Bestandteil von Aminosäuren, die wiederum die Konstruktionsblöcke für Proteine sind. Proteine strukturieren die Gewebe und viele von ihnen haben die enzymatische Aktivität, die erforderlich ist, um viele der lebenswichtigen Reaktionen für Zellen zu beschleunigen.
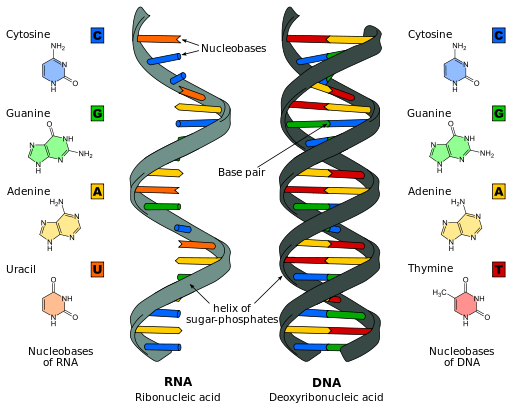 Nitrogóeno ist ein grundlegender Bestandteil der Stickstoffbasen, die ausmachen.SVG: Sponk / *Übersetzung: Sponk [CC BY-SA 3.0 (https: // creativecommons.Org/lizenzen/by-sa/3.0)] über Wikimedia Commons)
Nitrogóeno ist ein grundlegender Bestandteil der Stickstoffbasen, die ausmachen.SVG: Sponk / *Übersetzung: Sponk [CC BY-SA 3.0 (https: // creativecommons.Org/lizenzen/by-sa/3.0)] über Wikimedia Commons) Stickstoff ist in den stickstoffhaltigen Grundlagen von DNA und RNA vorhanden, wesentliche Moleküle für den Transfer genetischer Informationen von Eltern zu Nachkommen und zur ordnungsgemäßen Funktion lebender Organismen als zelluläre Systeme.
Passen
Die am häufigsten vorkommende Form dieses Elements in der Natur ist wie feste Phosphate in fruchtbaren Böden, Flüssen und Seen. Es ist ein wichtiges Element für das Funktionieren von Tieren und Gemüse, aber auch von Bakterien, Pilzen, Protozoen und allen Lebewesen.
Es kann Ihnen dienen: WaldnahrungsketteBei Tieren ist Phosphor in allen Knochen in Kalziumphosphat reichlich vorhanden.
Phosphor ist für das Leben wesentlich, da es auch ein Element ist, das Teil von DNA, RNA, ATP und Phospholipiden ist (grundlegende Komponenten von Zellmembranen).
Diese Bioelement ist immer für Energieübertragungsreaktionen verpflichtet, da sie Verbindungen mit sehr Energieverbindungen bildet, deren Hydrolyse verwendet wird, um verschiedene zelluläre Systeme zu bewegen.
Schwefel
Schwefel ist üblicherweise in Form von Sulfiden und Sulfaten. In vulkanischen Bereichen ist es besonders reichlich vorhanden und ist in der Verschwendung von Cystein- und Methodenaminosäuren vorhanden.
In Protein bilden die Schwefelatome des Cysteins eine intra- oder intermolekulare Wechselwirkung, die sehr stark als "Disulfidbrücke" bekannt ist, was für die Konformation der sekundären, tertiären und quaternären Struktur von zellulären Proteinen essentiell ist.
Coenzym A, ein metabolischer Vermittler mit einer Vielzahl von Funktionen, hat ein Schwefelatom in seiner Struktur.
Dieses Element ist auch für die Struktur vieler enzymatischer Cofaktoren von grundlegender Bedeutung, die an verschiedenen wichtigen Stoffwechselwegen beteiligt sind.
Sekundäre Bioelemente
Wie oben erwähnt, sind sekundäre Bioelemente diejenigen, die in geringerem Verhältnis als das primäre und wichtigste sind, sind Kalium, Magnesium, Eisen, Kalzium, Natrium und Zink.
Sekundäre Bioelemente oder Oligoemente sind an vielen physiologischen Prozessen von Pflanzen, in der Photosynthese, in der Atmung, im zellulären ionischen Gleichgewicht der Vakuole und der Chloroplasten, im Transport von Kohlenhydraten zum Phloem usw. beteiligt.
Dies gilt auch für Tiere und andere Organismen, bei denen diese Elemente, die mehr oder weniger entbehrlich und weniger reichlich vorhanden sind, Teil vieler notwendiger Cofaktoren für den Betrieb aller Zellmaschinen sind.
Eisen
Eisen ist eines der wichtigsten sekundären Bioelemente angesichts der Ausübung von Funktionen in mehreren Energiephänomenen. Es ist sehr wichtig bei der Reduzierung natürlicher Rostreaktionen.
Bei Säugetieren zum Beispiel ist Eisen ein wesentlicher Bestandteil von Hämoglobin, dem Protein, das für den Transport von Sauerstoff im Blut in Erythrozyten oder roten Blutkörperchen verantwortlich ist.
In Pflanzenzellen ist dieses Element auch Teil einiger Pigmente wie Chlorophyll, von grundlegend für photosynthetische Prozesse. Es ist Teil von Cytochrommolekülen und auch für das Atmen wesentlich.
Zink
Wissenschaftler glauben, dass Zink eines der Schlüsselelemente für das Erscheinungsbild eukaryotischer Organismen vor Millionen von Jahren war, da viele der DNA -Union -Proteine für die Replikation, die zu den „primitiven Eukaryoten“ zusammenhielt, Zink als Grund der Vereinigung verwendete.
Kann Ihnen dienen: Homologie (Biologie)Ein Beispiel für diese Art von Protein sind Zinkfinger, die an genetischer Transkription, Proteintranslation, Metabolismus und Proteinbaugruppe usw. beteiligt sind.
Kalzium
Kalzium ist eines der am häufigsten vorkommenden Mineralien auf dem Planeten Erde; Bei den meisten Tieren bestehen Zähne und Knochen in Calciumhydroxyphosphatform. Dieses Element ist für die Muskelkontraktion, die Übertragung von Nervenimpulsen und Blutgerinnung wesentlich.
Magnesium
Der größte Anteil von Magnesium in der Natur ist in fester Form kombiniert mit anderen Elementen, sondern nicht nur im freien Zustand. Magnesium ist ein Cofaktor von mehr 300 verschiedenen enzymatischen Systemen bei Säugetieren.
Die Reaktionen, an denen es teilnimmt. Magnesium ist für die Energieerzeugung in lebenden Organismen für oxidative Phosphorylierung und Glykolyse erforderlich.
Es trägt auch zur Entwicklung von Knochen bei und ist unter anderem für die Synthese von DNA, RNA, Glutathion erforderlich.
Natrium und Kalium
Sie sind zwei sehr reichlich vorhandene Ionen im Zellinnenraum, und die Variationen ihrer internen und externen Konzentrationen sowie ihres Transports sind für viele physiologische Prozesse entscheidend.
Kalium ist das am häufigsten vorkommende intrazelluläre Kation, das das Flüssigkeitsvolumen innerhalb der zellulären Innen- und transmembranalen elektrochemischen Gradienten beibehält.
Sowohl Natrium als auch Kalium beteiligen sich aktiv an der Übertragung von Nervenimpulsen, da sie von der Natrium-Potasio-Pumpe transportiert werden. Natrium beteiligt sich auch an Muskelkontraktion und Nährstoffabsorption durch Zellmembran.
Der Rest der sekundären Bioelemente: Molybdän (MO), Fluorid (F), Chlor (CL) Jod (I) und Kupfer (Cu) erfüllen wichtige Funktionen in vielen physiologischen Reaktionen. Es ist jedoch viel weniger als die sechs oben erklärten Elemente erforderlich.
Verweise
- Egami, f. (1974). Kleinere Elemente und Evolution. Journal of Molekular Evolution, 4 (2), 113-120.
- Hackh, ich. W. (1919). Bioelemente; Die chemischen Elemente der lebenden Materie. Das Journal of General Physiology, 1 (4), 429
- Kaim, w., & Rall, j. (neunzehn sechsundneunzig). Kupfer-a "moderne" Bioelement. Angewandte Chemie International Edition in englischer Sprache, 35 (1), 43-60.
- Nationales Gesundheitsinstitut. (2016). Magnesium: Fact Sheet für Angehörige der Gesundheitsberufe. Aktuelle Version, 27.
- Peñuelas, j., Fernández - Martínez, m., CIAIS, p., Jou, d., Piao, s., OBERSTEER, M.,… & Sardans, J. (2019). Die Bioelemente, das Elementom und die biogeochemische Nische. Ökologie, 100 (5), E02652
- Skalny, a. V. (2014). Bioelemente und Bioelementologie in Pharmakologie und Ernährung: grundlegende und praktische Aspekte. In Pharmakologie und Ernährungsintervention bei der Behandlung von Krankheiten. Intechopen.
- Solioz, m. (2018). Kupfer-eine moderne Bioelement. In Kupfer und Bakterien (pp. 1-9). Springer, Cham.
- Weltgesundheitsorganisation. (2015). Faktenblatt: Salz.

