Aluminiumbromid
- 3490
- 901
- Luca Holdt
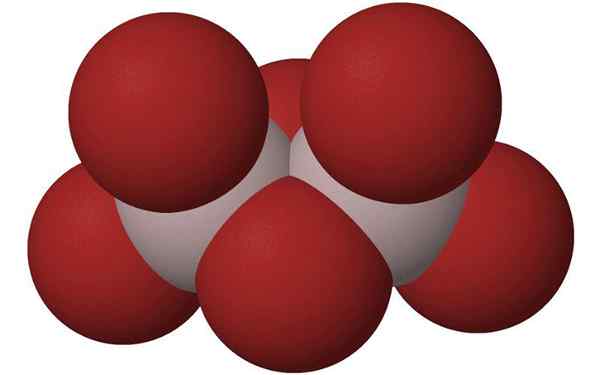
 Kugeln des Aluminium -Bromid -Dimers. Quelle: HOA112008, Wikimedia Commons
Kugeln des Aluminium -Bromid -Dimers. Quelle: HOA112008, Wikimedia Commons Was ist Aluminiumbromid?
Er Aluminiumbromid Es ist eine Verbindung, die durch ein Aluminiumatom und eine unterschiedliche Menge von Bromatomen gebildet wird. Es wird je nach Menge der Valenzelektronen gebildet, die Aluminium hat.
Da eine Verbindung von einem Metall (Aluminium) und einem Nicht -Metall (Brom) angebracht ist.
Aluminiumbromid ist eine Substanz, die normalerweise in einem festen Zustand mit einer kristallinen Struktur präsentiert wird. Die Farben der verschiedenen Aluminiumbromuros erscheinen als blasse Gelb unterschiedlicher Schattierungen, und manchmal wird es ohne offensichtliche Farbe dargestellt.
Die Farbe hängt von der Fähigkeit zur Lichtreflexion ab, die die Verbindung hat, und ändert sich abhängig von den entstandenen Strukturen und den Formen, die sie nimmt.
Der feste Zustand dieser Verbindungen kristallisiert, so dass sie gut definierte Strukturen mit einem ähnlichen Meersalz haben, aber ihre Farbe variieren.
Formel
Das Aluminiumbromid besteht aus einem Aluminium (Al) -atom und unterschiedlichen Mengen an Bromatomen (BR), abhängig von den Valenzelektronen, die Aluminium aufweist.
Daher kann die allgemeine Formel für Aluminiumbromid wie folgt geschrieben werden: ALBX, wobei "x" die Anzahl der Bromatome ist, die an Aluminium binden.
Der häufigste Weg, in dem es präsentiert wird, ist wie der2Br6, Das ist ein Molekül mit zwei Aluminiumatomen als Hauptbasen der Struktur.
Kann Ihnen dienen: Lactophenolblau: Eigenschaften, Zusammensetzung, Vorbereitung, verwendetDie Verbindungen zwischen ihnen werden durch zwei Brome in der Mitte gebildet, so dass jedes Aluminium -Atom vier Bromatome in seiner Struktur hat, aber zweier haben zwei zwei.
Eigenschaften und Eigenschaften von Aluminiumbromid
- Aufgrund seiner Natur ist es in Wasser sehr löslich, ist aber auch in Verbindungen wie Methanol und Aceton teilweise löslich, im Gegensatz zu anderen Substanzen.
- Es hat ein Molekulargewicht von 267 g/mol und wird durch kovalente Bindungen gebildet.
- Das Natriumbromid erreicht seinen Siedepunkt bei 255 ° C und erreicht seinen Schmelzpunkt bei 97.5 ° C.
- Ein weiteres Merkmal dieser Verbindung ist, dass sie beim Verdampfen Toxine abgibt, sodass sie nicht ratsam ist.
Anwendungen
- Eine der Verwendungszwecke dieser Art von Substanz aufgrund ihrer metallischen und nicht -metallischen Natur ist die von Wirkstoffen in chemischen Tests von Reinheiten. Diese Reinheitstests sind sehr wichtig, um die Qualität von Reagenzien zu bestimmen und Produkte herzustellen, mit denen Menschen zufrieden sind.
- In der wissenschaftlichen Forschung wird es sehr variabel verwendet. Zum Beispiel, um komplexe Strukturen zu bilden, Mittel in der Synthese anderer Wertchemikalien, bei der Hydrierung von Dihydroxinaftalenen und in der Selektivität der Reaktionen, unter anderem verwendet.
- Diese Verbindung ist kommerziell nicht beliebt. Wie oben zu sehen, gibt es einige Anwendungen, die sehr spezifisch, aber für die wissenschaftliche Gemeinschaft sehr interessant sind.
Verweise
- Chang, R. (2010). Chemie. McGraw-Hill Inter-American.
- Krahl, t., & Kemnitz und. (2004). Amorphes Eiringum -Bromidfluorid (ABF). Angewandte Chemie - Internationale Ausgabe.

