Wasserstoffbromid (HBR)
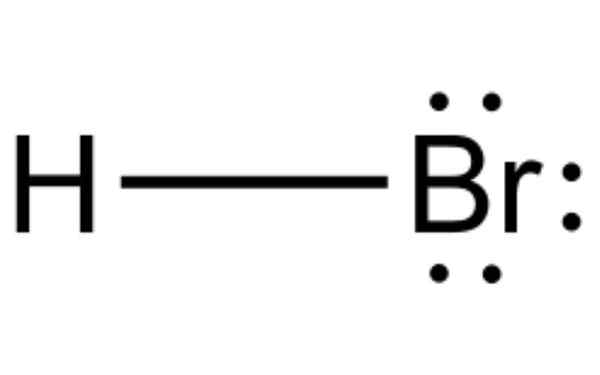
- 4122
- 695
- Rieke Scheer
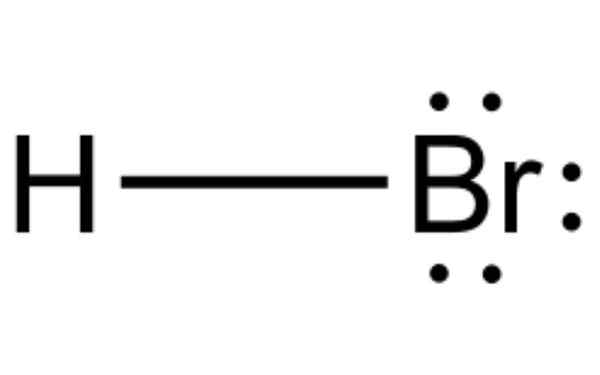 Wasserstoffbromid ist eine chemische Verbindung, die Bromhorsäure in Wasser bildet. Quelle: Rafał Rx
Wasserstoffbromid ist eine chemische Verbindung, die Bromhorsäure in Wasser bildet. Quelle: Rafał Rx Er Wasserstoffbromid Es ist ein diatomisches Molekül mit einer kovalenten Bindung. Die Verbindung wird als Wasserstoffhalogenid klassifiziert und ist ein farbloses Gas, das in Wasserbromhyterinsäure gelöst wurde.
Physikalische und chemische Eigenschaften
- Wasserstoffbromid ist ein farbloses Gas bei Raumtemperatur mit saurem und irritierendem Geruch. Die Verbindung ist stabil, verdunkelt sich aber leicht, wenn sie Luft oder Licht ausgesetzt ist.
- Es hat ein Molekulargewicht von 80.91 g/mol und eine Dichte von 3.307 g/l, was es schwerer macht als die Luft. Das Gas kondensiert eine farblose Kochenflüssigkeit von -66,73 ° C.
- Durch die Weiterkühlung verfestigt sich die Flüssigkeit und erhält weiße Kristalle, deren Schmelzpunkt -86,82 ° C mit einer Dichte von 2.603 g/ml beträgt.
- Wasserstoffbromid ist wasserlöslicher als Wasserstoffchlorid und kann 221 g in 100 ml Wasser bei 0 ° C auflösen, was einem Volumen von 612 Litern dieses Gases für jeden Liter Wasser entspricht. Es ist auch löslich in Alkohol und anderen Bio -Lösungsmitteln.
- In wässriger Lösung (Bromhydsäure) sind die sauren Eigenschaften des HBR dominant (wie bei HF und HCl) und im Zusammenhang zwischen Wasserstoff und Halogen ist es bei Wasserstoffbromid schwächer als im Wasserstoffchlorid.
Wenn Chlor durch das Wasserstoffbromid geleitet wird, wird die Bildung von braunen Dämpfen beobachtet. Die Reaktion, die es erklärt, lautet wie folgt:
2HBR + Cl2 → 2HCl + Br2
Dies ist anzeigt, dass Wasserstoffbromid ein stärkeres Reduktionsmittel ist als Wasserstoffchlorid und dass Wasserstoffchlorid ein besseres oxidierendes Mittel ist.
- Wasserstoffbromid ist eine starke wasserfreie Säure (ohne Wasser). Reagieren Sie schnell und exotherm mit Basen aller Art (einschließlich Amine und Amide).
Kann Ihnen dienen: Amine- Reagieren exotherm mit Carbonaten (einschließlich Kalkstein- und Baumaterialien, die es enthalten) und Wasserstoff -Carbonate, um Kohlendioxid zu erzeugen.
- Reagiert mit Sulfiden, Carbiden, Boruros und Phosphon, um giftige oder brennbare Gase zu erzeugen.
- Reagiert mit vielen Metallen (einschließlich Aluminium, Zink, Kalzium, Magnesium, Eisen, Zinn und allen alkalischen Metallen), um brennbares Wasserstoffgas zu erzeugen.
Reaktivität und Gefahren
Wasserstoffbromid ist eine ätzende und irritierende Verbindung. Es ist äußerst gefährlich bei Hautkontakt (irritierend und korrosiv) und Augen (irritierend) und bei Aufnahme und Inhalation (pulmonaler Reizung).
Die Verbindung wird in Druckbehältern mit verflüssigtem Gas gespeichert. Eine längere Exposition gegenüber der intensiven Wärme oder Wärme kann zum heftigen Bruch des Druckbehälters führen, der durch Freisetzung reizender giftiger Dämpfe ausgelöst werden kann.
Eine längere Exposition gegenüber niedrigen Konzentrationen oder kurzfristige Exposition gegenüber hohen Konzentrationen kann durch Inhalation zu nachteiligen gesundheitlichen Auswirkungen führen.
Die thermische Zersetzung von wasserfreiem Wasserstoffbromid produziert giftiges Brom. Es kann brennbar werden, wenn es durch Freisetzung von Wasserstoff reagiert. In Kontakt mit Cyanid produziert es toxische Wasserstoff -Cyanidgase.
Wenn diese Chemikalie in Lösung mit den Augen in Kontakt kommt, müssen sie sofort mit großen Mengen Wasser gewaschen werden, wobei sie gelegentlich die unteren und oberen Augenlider anheben müssen.
Bei dieser Chemikalie sollten keine Kontaktlinsen verwendet werden. Wenn der Augenstoff gefroren ist, sollte sofortige medizinische Hilfe gesucht werden.
Wenn das Gewebe nicht gefroren ist, spülen Sie die Augen sofort und vollständig mit großen Mengen Wasser für mindestens 15 Minuten aus und heben Sie gelegentlich die unteren und oberen Augenlider an.
Wenn diese Chemikalie in Lösung mit der Haut in Kontakt kommt und kein Gefrieren produziert, spülen Sie die mit Wasser kontaminierte Haut sofort aus. Wenn Sie in die Kleidung eindringen, überprüfen Sie sie sofort und waschen Sie die Haut mit Wasser.
Kann Ihnen dienen: CarbonsäureWenn ein Einfrieren auftritt, suchen Sie sofort medizinische Hilfe auf. Die betroffenen Bereiche oder die Spülung mit Wasser sollten nicht gerieben werden. Um mehr Gewebeschäden zu vermeiden, sollten Sie nicht versuchen, gefrorene Kleidung aus Frostgebieten zu entfernen.
Wenn große Mengen dieser Chemikalie eingeatmet werden, sollte die Person, die in frischer Luft ausgesetzt ist, sofort bewegt werden. Wenn das Atmen aufgehört hat, machen Sie die Mundmundbelastung. Das Opfer sollte heiß und in Ruhe gehalten werden und versuchen, so schnell wie möglich medizinische Hilfe zu erhalten.
Synthese
Gasförmiges Wasserstoffbromid kann im Labor durch Broming-Tetralin (1, 2, 3, 4-Tetrahydronaphthalin) hergestellt werden. Der Nachteil ist, dass die Hälfte des Broms verloren geht. Die Ausbeute beträgt ungefähr 94% oder was gleich ist, 47% der Brom endet als HBR.
C10H12 + 4 Br2 → c10H8Br4 + 4 HBR
Wasserstoffbromidgas kann auch im Labor durch Reaktion der auf Natriumbromid konzentrierten Schwefelsäure synthetisiert werden.
Nabr (s) + h2SW4 → hbr (g) + nahso4
Der Nachteil dieser Methode ist, dass ein Groß.
2 HBR + H2SW4 → Br2 + SW2 + 2 h2ENTWEDER
Wasserstoffbromid kann im Labor durch Reaktion zwischen gereinigtem Wasserstoff und Brom hergestellt werden. Dies wird durch Platin -Asbest katalysiert und in einem Quarzrohr bei 250 ° C durchgeführt.
Br2 + H2[Pt] → 2 HBR
Sie können auch kleinwertiges wasserfreies Wasserstoffbromid für die Trifenylphosphonium -Tromure -Thermolyse in Xylol zu Reflux produzieren.
Sie können HBR durch die rote Phosphormethode erhalten. Erstens wird der rote Phosphor im Wasserreaktor zugegeben und anschließend langsam das Brom unter Agitation und die Reaktion von Bromhorsäure und Phosphorsäure durch Sedimentation, Filtration und die erhaltene Destillation Bromhychlorsäure sein.
Kann Ihnen dienen: Stanislao CannizzaroP4+6 Br2+12 H₂O → 12 HBR + 4 H3Po3
Wasserstoffbromid, die nach den oben genannten Methoden hergestellt werden, können mit BR kontaminiert werden2, Dies kann beseitigt werden, indem das Gas durch eine Phenollösung in Tetrachlormethan oder ein anderes Lösungsmittel geleitet wird, das bei Raumtemperatur angemessen ist und 2, 4, 6-Tribromophenol erzeugt und damit mehr HBR erzeugt wird.
Dieser Vorgang kann auch über Kupferchips oder Kupfergaze bei hoher Temperatur durchgeführt werden.
Anwendungen
- Der HBR wird zur Herstellung von organischen Bromiden wie Methylbromid, Bromoethan usw. verwendet., und anorganisch, wie Natriumbromid, Kaliumbromid, Lithiumbromid und Calciumbromid usw.
- Es wird auch in fotografischen und pharmazeutischen Anwendungen oder zur Synthese von Beruhigungsmitteln und Anästhetika verwendet.
- Es wird in industrieller Trocknung, Textilisbe, Beschichtung, Oberflächenbehandlungsmitteln und Ignifugation angewendet.
- Es wird auch verwendet, um Polysilicio -Blätter für die Herstellung von Computerchips aufzuzeichnen.
- Es ist ein gutes Lösungsmittel für einige Metallmineralien, die in der Verfeinerung von Metall mit hoher Reinheit verwendet werden.
- In der Ölindustrie wird es als Trennung von Alcoxi und Phänoxie verwendet.
- Es wird auch in synthetischen Farbstoffen und Gewürzen verwendet.
- Die Verbindung wird als analytisches Reagenz bei der Bestimmung von Schwefel, Selen, Wismut, Zink und Eisen zur Trennung des Zinns von Arsen und Antimon verwendet. Es ist ein Alkylierungskatalysator und ein Reduktionsmittel, das in der organischen Synthese verwendet wird.
- Es kann zur Herstellung von Bromhydsäure verwendet werden.
- HBR ist für die meisten Metalle hochreaktiv und korrosiv. Säure ist ein häufiges Reagenz in der organischen Chemie, das zur Oxidation und Katalyse verwendet wird.
Verweise
- Wasserstoffbromid. Aus Chemicalbook entnommen.
- Sicherheitsdatenblatt Wasserstoffbromid. Entnommen von Sciencelab.com.

