Formelle Last
- 1117
- 153
- Said Ganzmann
Was ist die formelle Last?
Der Formelle Last (Vgl.) Ist eines, das einem Atom eines Moleküls oder eines Ions zugeordnet ist, das es ermöglicht, seine Strukturen und chemischen Eigenschaften in Abhängigkeit davon zu erklären. Dieses Konzept impliziert die Berücksichtigung des maximalen Charakters der Kovalenz in der A-B-Verbindung; Das heißt, das Elektronenpaar wird gleichermaßen zwischen A und B geteilt.
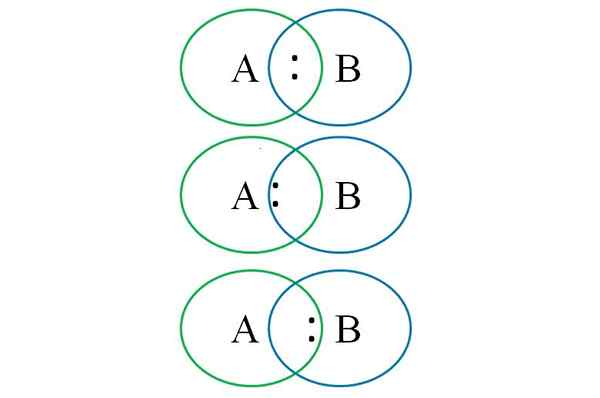
Um das obige im unteren Bild zu verstehen, werden zwei verknüpfte Atome angezeigt: einer mit Buchstabe A und der andere mit Buchstaben B. Wie zu sehen ist, wird im Abschnitt der Kreise ein Glied mit dem Paar gebildet: ". In diesem heteronuklearen Molekül, wenn a und b gleiche Elektronegativitäten haben.

Angesichts der Tatsache, dass zwei verschiedene Atome keine identischen Eigenschaften haben können, ist das Paar ":" wird angezogen, von dem es elektronegativer ist. In diesem Fall ist das Paar „:“, wenn a elektronegativer als B ist, näher an der von B näher. Das Gegenteil tritt auf, wenn B elektronegativer ist als A und nähert sich jetzt ":" A B.
Um dann formelle Gebühren sowohl A als auch B zuzuweisen, muss der erste Fall berücksichtigt werden (den über dem Bild). Wenn die rein kovalente Verbindung A-B kaputt geht, würde eine homolitische Trennung auftreten, wodurch freie Radikale a · und · b erzeugt werden.
Qualitative Vorteile der Verwendung formeller Last
Die Elektronen sind nicht wie im vorherigen Beispiel fix. Wenn es sich um ein diatomisches Molekül handelt, ist bekannt, dass das Paar „:“ geteilt oder zwischen beiden Atomen wandern muss; Gleiches gilt in einem Molekül vom Typ A-B-C, jedoch mit größerer Komplexität.
Wenn jedoch ein Atom untersucht wird und in seinen Verbindungen eine hundertprozentige Kovalenz annimmt, ist es einfacher festzustellen, ob innerhalb der Verbindung Elektronen gewinnt oder verliert. Um diesen Gewinn oder Verlust zu bestimmen, muss Ihr basaler oder freier Zustand mit Ihrer elektronischen Umgebung verglichen werden.
Kann Ihnen dienen: Amagatgesetz: Erklärung, Beispiele, ÜbungenAuf diese Weise ist es möglich, eine positive Belastung (+) zuzuweisen, wenn das Atom ein Elektron verliert, oder eine negative Belastung (-), wenn im Gegenteil ein Elektron gewinnt (die Zeichen müssen in einem Kreis geschrieben werden).
Obwohl die Elektronen nicht genau gefunden werden können.
Das heißt, die formale Belastung eines Atom.
Formel und wie man sie berechnet
Sind formelle Lasten willkürlich zugewiesen? Die Antwort ist nein. Hierzu müssen der Gewinn oder der Elektronenverlust berechnet werden, indem rein kovalente Bindungen angenommen werden, und dies wird durch die folgende Formel erreicht:
Vgl
Wenn das Atom einen CF mit einem Wert von +1 hat, wird eine positive Last ( +) zugewiesen; Wenn Sie einen CF mit einem Wert von -1 haben, wird ihm eine negative Belastung zugewiesen ( -).
Um die CF korrekt zu berechnen, müssen die Schritte unten befolgt werden:
- Suchen Sie, welche Gruppe das Atom innerhalb des Periodenzüchtertabels ist.
- Zählen Sie die Anzahl der Links, die sich mit ihren Nachbarn bilden: Die Doppelverbindungen (=) sind zwei wert und die dreifachen Links sind drei wert (≡).
- Schließlich zählen Sie die Anzahl der nicht geteilten Elektronen, die leicht mit Lewis -Strukturen beobachtet werden können.
Berechnungsschwankungen gemäß der Struktur
Angesichts des linearen Moleküls A-B-C-D können formale Lasten für jedes Atom variieren, wenn die Struktur beispielsweise jetzt als: B-C-A-D, C-A-B-D, A-C-D-B usw. geschrieben ist. Dies liegt daran.
Es kann Ihnen dienen: Meniskus (Chemie)Welche der drei möglichen molekularen Strukturen entspricht der ABCD -Verbindung? Die Antwort lautet: diejenige, die im Allgemeinen die niedrigsten CF -Werte besitzt; Auch diejenige, die den elektronegativsten Atomen negative Lasten (-) zuweist.
Wenn C und D elektronegativer als A und B sind, erwerben sie durch mehr Elektronen positive formale Lasten (aus einer mnemonischen Regel), die aus einer mnemonischen Regel beobachtet werden).
Die stabilste Struktur und die am meisten bevorzugte Energie ist C-A-B-D, da sie sowohl in C als auch in B nur eine Verbindung bilden. Andererseits sind die Struktur A-B-C-D und diejenigen, die ein C oder B haben, das zwei Links (-c- oder -d-) bildet.
Welcher der aller Strukturen ist am instabilsten? A-C-D-B, da nicht nur C und D zwei Verbindungen bilden, sondern auch ihre negativen formalen Belastungen (-) nebeneinander liegen und die Struktur weiter destabilisieren.
Beispiele für formale Lastberechnungen
Bf4- (Tetrafluoroborato Ion)
Das Boratom ist von vier Fluoratomen umgeben. Da das B zu Gruppe IIIA (13) keine gemeinsamen Elektronen und vier kovalente Bindungen fehlt, ist sein CF (3-4-0 = -1). Stattdessen für das F-Element der Gruppe VIIA (17) ist der CF (7-6-1 = 0).
Um die Last des Ionen oder Moleküls zu bestimmen, reicht es aus, die einzelnen CFs der Atome hinzuzufügen, aus denen es komponiert wird: (1 (-1) + 4 (0) = -1).
Die CF für B hat jedoch keine wirkliche Bedeutung; Dies ist, dass sich nicht die größte elektronische Dichte befindet. Tatsächlich wird diese elektronische Dichte auf die vier F -Atome verteilt, viel elektronegatives Element als B.
Kann Ihnen dienen: schwache SäureVerhalten2 (Berylliumhydrid)
Das Beryllium -Atom gehört zu Gruppe IIA (2), bildet zwei Links und fehlt wiederum nicht gemeinsame Elektronen. Somit sind die CF für das und die H: H sind:
VglSei= 2-2-0 = 0
VglH= 1-1-0 = 0
Verhaltenslast2= 1 (0) + 2 (0) = 0
CO (Kohlenmonoxid)
Seine Lewis -Struktur kann dargestellt werden als: Cwerbo: (obwohl sie andere Resonanzstrukturen vorstellt). Wiederholen Sie die Berechnung des CF, diesmal für die C (der Mehrwertsteuergruppe) und die O (der Via -Gruppe), Sie haben:
VglC= 4-3-2 = -1
VglENTWEDER= 6-3-2 = +1
Dies ist ein Beispiel, in dem formelle Gebühren nicht zur Art der Elemente passen. Desto oder ist elektronegativer als das C und sollte daher keine positiven tragen.
Die anderen Strukturen (c = o und (+CO(-)), obwohl sie der kohärenten Allokation der Lasten einhalten, aber die Oktettregel nicht einhalten (das C hat weniger als acht Elektronen Valencia).
NH4+ (Ion Ammonium), NH3 und NH2- (Amiduro Ion)
Je mehr Elektronen das N teilen, desto positiver sein CF (zum Ammoniumionen, da es keine Energieverfügbarkeit hat, um fünf Bindungen zu bilden).
Auch die Berechnungen für das N -Ammonium, das Ammoniak und das Amiduro -Ion anwenden, haben dann:
CF = 5-4-0 = +1 (NH4+)
CF = 5-3-2 = 0 (NH3)
Und schlussendlich:
CF = 5-2-4 = -1 (NH2-)
Das heißt im NH2- Das N hat vier nicht geteilte Elektronen und teilen alle, wenn es den NH bildet4+. CF für H entspricht 0 und daher wird Ihre Berechnung gespeichert.

