Ketonentypen, Eigenschaften, Nomenklatur, Verwendungen, Beispiele
- 3964
- 1153
- Frederike Birkemeyer
Der Ketone Es sind organische Verbindungen mit einer Carbonylgruppe (-co). Sie sind einfache Verbindungen, in denen das Karabone der Carbonylgruppe mit zwei Kohlenstoffatomen (und ihren Substituentenketten) verbunden ist). Die Ketone sind "einfach", weil sie keine reaktiven Gruppen wie -OH oder -Cl mit Kohlenstoff haben.
Als polare Verbindungen erkannt, sind Ketone normalerweise löslich und flüchtig, was sie zu guten Lösungsmitteln und Zusatzstoffen für Parfums macht. Darüber hinaus sind sie leicht vorzubereiten, relativ stabil und haben eine hohe Reaktivität, was sie zu einer fast perfekten Zwischenverbindung gemacht hat, um komplexere organische Verbindungen vorzubereiten.
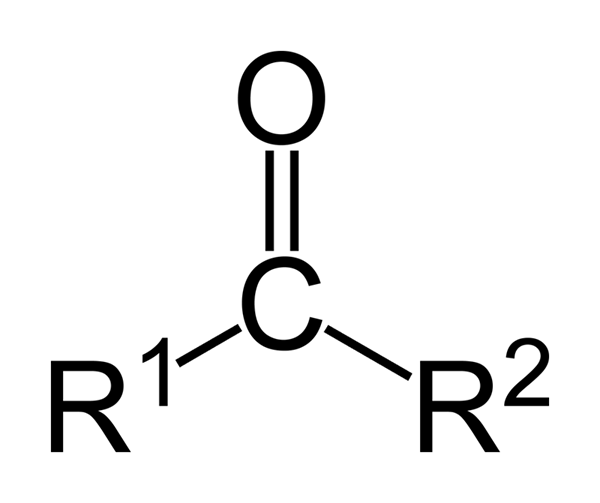
 Allgemeine Formel von Ketonen
Allgemeine Formel von Ketonen Schließlich ist die Eliminierung von Ketonen aus dem menschlichen Körper normalerweise mit einem niedrigen Zuckergehalt (in Diabetik- und/oder extremen Fastenfällen) verbunden, was für den Patienten schwerwiegende Gesundheitsprobleme verursachen kann.
[TOC]
Allgemeine Formel von Ketonen
Die Ketone sind Carbonylverbindungen, in denen diese Gruppe mit zwei Gruppen von Kohlenwasserstoffen verbunden ist. Dies können Alkylgruppen, Gruppen von Benzolringen oder beides sein.
Ein Keton kann einfach als r- (c = o) -r 'dargestellt werden, wobei R und R' zwei Ketten eines Kohlenwasserstoffs sind (Alko, Alkene, Alkine, Cycloalcanos, Derivate von Benzol und anderen). Es gibt keine Ketone mit einem Wasserstoff, der an der Carbonylgruppe angebracht ist.
Es gibt eine Vielzahl von Methoden zur Herstellung von Ketonen im Bereich Industrie und Labor. Darüber hinaus ist es wichtig zu beachten, dass Ketone von verschiedenen Organismen, einschließlich Menschen, synthetisiert werden können.
In der Branche ist die häufigste Methode für die Synthese von Ketonen die Oxidation von Kohlenwasserstoffen, typischerweise unter Verwendung von Luft. In kleinem Maßstab werden Ketone normalerweise durch die Oxidation von sekundären Alkoholen hergestellt, was eine Cetona und Wasserprodukte als Produkte verleiht.
Über diese häufigsten Methoden können Ketone durch Alkene, Alkine, Salze von Stickstoffverbindungen, Estern und vielen anderen Verbindungen synthetisiert werden, wodurch sie leicht erhalten werden.
Arten von Ketonen
Es gibt mehrere Klassifikationen für Ketone, abhängig hauptsächlich von Substituenten in ihren R -Ketten. Die häufigsten Klassifizierungen für diese Substanzen werden nachstehend ernannt:
Gemäß der Struktur seiner Kette
In diesem Fall wird das Keton durch die Art und Weise klassifiziert, in der seine Kette strukturiert ist: Aliphatische Ketone sind solche mit zwei R- und R -Radikalen mit Alkylradikalform (Alkane, Alkene, Alkine und Cycloalcanos).
Es kann Ihnen dienen: Isoamylalkohol: Struktur, Eigenschaften, Verwendung und RisikenAndererseits sind die Aromatischen diejenigen, die Derivate von Benzol bilden, während sie immer noch Ketone sind. Schließlich sind gemischte Ketone diejenigen, die eine alquilische und radikale R -Aril haben oder umgekehrt.
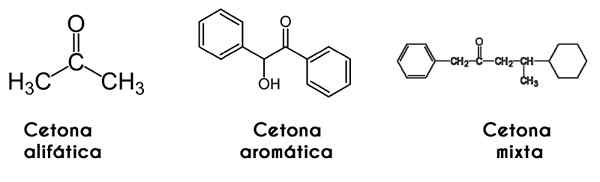 Von links nach rechts: Propanona, Benzrofrona und Phenylmetilbutanonon. Wikimedia Commons Bilder.
Von links nach rechts: Propanona, Benzrofrona und Phenylmetilbutanonon. Wikimedia Commons Bilder. Nach der Symmetrie ihrer Radikalen
In diesem Fall werden die R- und R -Radikale von der Carbonylgruppe untersucht. Wenn diese gleich (identisch) sind, nennt sich das Keton symmetrisch; Aber wenn sie unterschiedlich sind (wie die meisten Ketone), nennt es sich asymmetrisch.
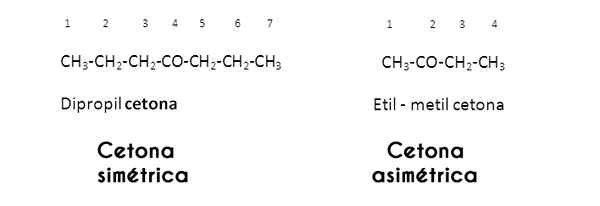 Bilder über Wikimedia Commons.
Bilder über Wikimedia Commons. Nach der Sättigung seiner Radikalen
Ketone können auch nach der Sättigung ihrer Kohlenstoffketten klassifiziert werden. Wenn diese in Form von Alkanen sind, nennt sich das Keton selbst gesättigtes Keton. Andererseits wird das Keton als ungesättigtes Keton bezeichnet, wenn die Ketten wie Alkene oder Alkine sind.
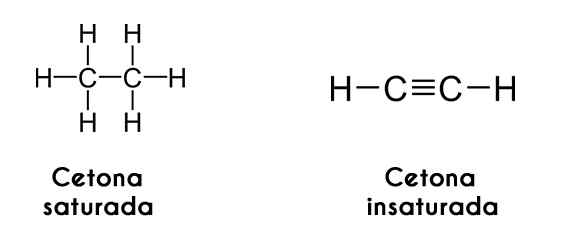 Links das Acetylen rechts. Bilder über Wikimedia Commons.
Links das Acetylen rechts. Bilder über Wikimedia Commons. Dicetone
Dies ist eine Klasse, abgesehen von Cetona, da die Ketten dieses Ketons zwei Carbonylgruppen in seiner Struktur haben. Einige dieser Ketone haben einzigartige Eigenschaften, wie z. B. eine größere Verbindungslänge zwischen Kohlenstoffen.
Zum Beispiel sind Dicetone, die aus dem Cyclohexan abgeleitet sind.
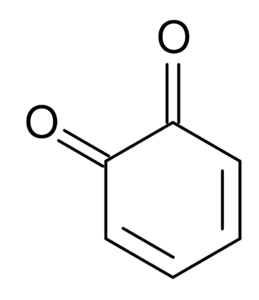 Ortho-Benzoquinon. Süd in englischer Wikipedia / Public Domain
Ortho-Benzoquinon. Süd in englischer Wikipedia / Public Domain Physikalische und chemische Eigenschaften von Ketonen
Die Ketone sind wie die meisten Aldehydos Flüssigmoleküle und haben eine Reihe physikalischer und chemischer Eigenschaften, die je nach Länge ihrer Ketten variieren. Seine Eigenschaften werden unten beschrieben:
Siedepunkt
Die Ketone sind sehr flüchtig, erheblich polar und können keine Wasserstoffbrückenbindungen aus Wasserstoff spenden (sie haben keine Wasserstoffatome, die an ihre Carbonylgruppe gebunden sind).
Der Siedepunkt eines Ketons steigt mit zunehmender Größe des Moleküls. Dies ist auf die Intervention von Van der Waals und Dipolo-Dipolo-Kräften zurückzuführen, die eine größere Menge an Energie erfordern, um angezogene Atome und Elektronen innerhalb von Moleküle zu trennen.
Löslichkeit
Die Löslichkeit von Ketonen hat einen starken Einfluss auf die Kapazität dieser Moleküle, Wasserstoff in ihrem Sauerstoffatom zu akzeptieren und somit Wasserstoffbindung mit Wasser zu bilden. Darüber hinaus sind Kräfte der Anziehung, Dispersion und Dipol-Dipol zwischen Ketonen und Wasser, die ihre lösliche Wirkung erhöhen.
Kann Ihnen dienen: Eisen (Element): Eigenschaften, chemische Struktur, verwendetDie Ketone verlieren die Löslichkeitskapazität umso größer ihres Moleküls, da sie beginnen, mehr Energie zu benötigen, um sich in Wasser aufzulösen. Sie sind auch in organischen Verbindungen löslich.
Säure
Dank ihrer Carbonylgruppe haben Ketone eine saure Natur. Dies geschieht aufgrund der Resonanzstabilisierungskapazität, die diese funktionelle Gruppe besitzt, die Protonen ihrer Doppelbindung zur Bildung einer konjugierten Basis namens Enol verleihen können.
Reaktivität
Ketone sind Teil einer großen Anzahl von organischen Reaktionen; Dies geschieht aufgrund der Anfälligkeit seines Carbonylkohlenstoffs gegenüber der nukleophilen Addition zusätzlich zur Polarität davon.
Wie oben erwähnt, wird die große Reaktivität von Ketonen von einem anerkannten Zwischenprodukt hergestellt, das als Grundlage für die Synthese anderer Verbindungen dient.
Nomenklatur
Die Ketone werden nach der Priorität oder Bedeutung der Carbonylgruppe im gesamten Molekül benannt. Wenn Sie also ein Molekül haben, das von der Carbonylgruppe bestimmt wird.
Es dauert die Hauptkette mit größerer Länge, die die Carbonylgruppe hat, und dann wird das Molekül benannt. Wenn die Carbonylgruppe keine Priorität gegenüber den anderen funktionellen Gruppen des Moleküls hat, wird sie mit "-oxo" identifiziert.
Für kompliziertere Ketone kann die Position der Funktionsgruppe mit einer Zahl identifiziert werden, und im Fall von Dicetonen (Ketone mit zwei Substituenten R und R 'identisch) wird das Molekül mit dem Suffix „-diona“ benannt.
Schließlich kann das Wort "Cetona" auch verwendet werden, nachdem die mit der Carbonylfunktionsgruppe verbundenen radikalen Ketten identifiziert wurden.
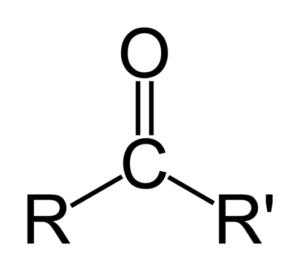
Unterschied zwischen Aldehydos und Ketonen
Der größte Unterschied zwischen Aldehyde und Ketonen ist das Vorhandensein eines Wasserstoffatoms, das der Carbonylgruppe in den Aldehyden befestigt ist.
Dieses Atom hat eine wichtige Wirkung bei der Einbeziehung eines Moleküls in eine Oxidationsreaktion.
Andererseits besitzt ein Cetona diesen Wasserstoff nicht, sodass die für die Oxidation erforderlichen Mindestschritte nicht auftreten.
Es gibt Methoden zum Oxidieren eines Keton.
Kann Ihnen dienen: Ionisation in Physik und Chemie: Konzept, Prozess und BeispieleIndustrielles und tägliches Leben nutzt
In der Branche werden Ketone in Parfums und Gemälden beobachtet, wobei Stabilisierungs- und Kondompapiere angenommen werden, die verhindern, dass andere Komponenten der Mischung sich verschlechtern. Sie haben auch ein breites Spektrum als Lösungsmittel in jenen Branchen, die neben der Pharmazeutikum Sprengstoffe, Gemälde und Textilien herstellen.
Aceton (das kleinste und kleinere Keton) ist eine sehr gut anerkannte Lösungsmittelwelt.
In der Natur können Ketone als Zucker erscheinen, sogenannte Ketusse. Die Ketosas sind Monosaccharide, die eine Cetona von Molekül enthalten. Die bekannteste Ketose ist Fructose, der Zucker in Früchten und Honig.
Die Biosynthese von Fettsäuren, die im Zytoplasma von tierischen Zellen auftreten, erfolgt auch durch die Wirkung von Ketonen. Schließlich und, wie oben erwähnt.
Beispiele für Ketone
Butanona (C4H8ENTWEDER)
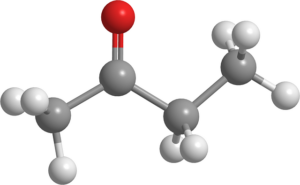 Butanone -Molekül. Quelle: Pixabay.
Butanone -Molekül. Quelle: Pixabay. Diese Flüssigkeit wird auch als MEK (oder MEC) bekannt und wird in der Branche in großem Maßstab hergestellt und als Lösungsmittel verwendet.
Cyclohexanon (c6H10ENTWEDER)
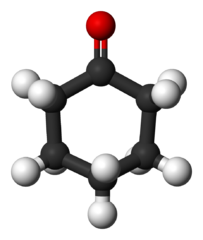 Cyclohexanonmolekül. Benjah-BMM27 / Public Domain
Cyclohexanonmolekül. Benjah-BMM27 / Public Domain Dieses Keton wird in großem Maßstab hergestellt und wird als Vorläufer des Synthetikmaterials Nylon verwendet.
Testosteron (c19H22ENTWEDER2)
 Testosteronmolekül. Wikimedia Commons
Testosteronmolekül. Wikimedia Commons Es ist das Haupthormon des männlichen Geschlechts und eines anabolen Steroids, das in den meisten Wirbeltieren vorkommt.
Progesteron (ceinundzwanzigH30ENTWEDER2)
 Medroxiprogesteronacetat, Cyclofemin -Komponente
Medroxiprogesteronacetat, Cyclofemin -Komponente Endogenes Steroid- und Sexualhormon, die am Menstruationszyklus, der Schwangerschaft und der Embryogenese beim Menschen und anderen Spezies beteiligt sind.
Aceton (CH3(CO) CH3)
 Acetonverbindung. Benjah-BMM27 / Public Domain
Acetonverbindung. Benjah-BMM27 / Public Domain Auch als Propanona bekannt, handelt es sich um eine farblose Verbindung, die für die Herstellung verschiedener Industrieprodukte wie Kunststoffe sowie für Haushygieneprodukte und Kosmetika wie Entfernung verwendet wird.
Cortison (ceinundzwanzigH28ENTWEDER5)
 Kortison. Benjah-BMM27 / Public Domain
Kortison. Benjah-BMM27 / Public Domain Steroidhormon zur Bekämpfung bestimmter Krankheiten und Erkrankungen wie Entzündungen, Akne, Allergien und anderen Arten von Hautreaktionen, Asthma oder Krebs und Leukämie.
Benzofenona (c13H10ENTWEDER)
 Benzofenom. Benjah-BMM27 / Public Domain
Benzofenom. Benjah-BMM27 / Public Domain Zusammensetzung, die bei der Schaffung von Parfums und anderen kosmetischen oder Sonnenschutzprodukten aufgrund ihrer aromatischen Zusammensetzung weit verbreitet sind.
Verweise
- Wikipedia. (S.F.). Keton. Erhalten von in.Wikipedia.Org
- Britannica, e. (S.F.). Keton. Aus Britannica erhalten.com
- Universität, m. S. (S.F.). Aldehyde und Ketone. Aus der Chemie erhalten.MSU.Edu
- Chemguide. (S.F.). Einführung Aldehyde und Ketone. Aus Chemguide erhalten.CO.Vereinigtes Königreich
- Calgary, u. ENTWEDER. (S.F.). Ketone. Erhalten von chem.Ucalgary.AC

