Zyklus (C5H10) Struktur, Eigenschaften und Verwendung
- 3656
- 706
- Frederike Birkemeyer
Er Cyclopentano Dies ist zyklischer Kohlenwasserstoff, insbesondere ein Cycloalcano. Wiederum ist es eine organische Verbindung, deren molekulare Formel C ist5H10. Kann als geschlossene Version der visualisiert werden N-Pentano, offene Kette, in der seine Enden durch Verlust von zwei Wasserstoffatomen verbunden sind.
Im unteren Bild wird das Skelett des Cyclopentano gezeigt. Beachten Sie, wie geometrisch Ihr Skelett trägt, und bildet einen Pentagonalring. Seine molekulare Struktur ist jedoch nicht flach, sondern zeigt Falten, die versuchen, die Spannungen im Ring zu stabilisieren und zu reduzieren. Radfahren ist eine hochflüchtete und brennbare Flüssigkeit, aber nicht so sehr wie die N-Pentano.
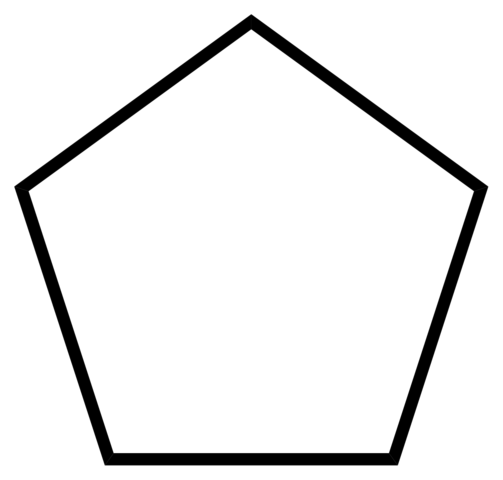 Kohlenstoffskelett des Cyclopentano. Quelle: Ccroberts [Public Domain]
Kohlenstoffskelett des Cyclopentano. Quelle: Ccroberts [Public Domain] Aufgrund seiner Lösungsmittelkapazität ist der Cyclopentano eines der am häufigsten verwendeten Lösungsmittel in der chemischen Industrie. Es ist nicht überraschend, dass viele starke Geruchsprodukte es unter ihrer Komposition enthalten und daher brennbar sind. Es wird auch als Expansionsmittel für Polyurethanschaum verwendet, die in Kühlschränken verwendet werden.
[TOC]
Ciclipentano -Struktur
Intermolekulare Wechselwirkungen
 Molekülstruktur des Cyclopentano, das durch ein Modell von Kugeln und Balken dargestellt wird. Quelle: Jynto [CC0]
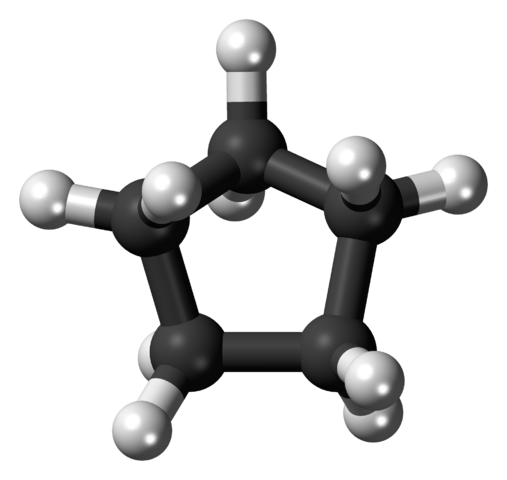
Molekülstruktur des Cyclopentano, das durch ein Modell von Kugeln und Balken dargestellt wird. Quelle: Jynto [CC0] Im ersten Bild wurde das Skelett des Cyclopentano gezeigt. Jetzt sehen wir, dass es mehr als ein einfaches Pentagon ist: An seinen Rändern fällt Wasserstoffatome (weiße Kugeln) hervor, während Kohlenstoffatome den Pentagonal Ring (schwarze Kugeln) ausmachen.
Mit nur C-C- und C-Bindungen ist sein Dipolmoment unbedeutend, sodass Cyclopentano-Moleküle nicht durch Dipol-Dipolo-Kräfte miteinander interagieren können. Stattdessen bleiben sie dank der dispersiven Kräfte von London zusammen, wobei die Ringe versuchen, einen übereinander zu stapeln.
Dieser Stack bietet einen bestimmten Kontaktbereich als zwischen den linearen Molekülen von N-Pentano. Infolgedessen hat der Cyclopentano einen größeren Siedepunkt als der N-Pentano sowie ein niedrigerer Dampfdruck.
Es kann Ihnen dienen: 7 Chemie -Laborpraktiken (einfach)Die dispersiven Kräfte sind für das Cyclopentano verantwortlich. Obwohl es nicht viele Informationen über seine kristalline Struktur gibt, ist dies polymorph und hat drei Phasen: I, II und III, ist Phase II eine ungeordnete Mischung aus I und III.
Konformation und Anulspannung
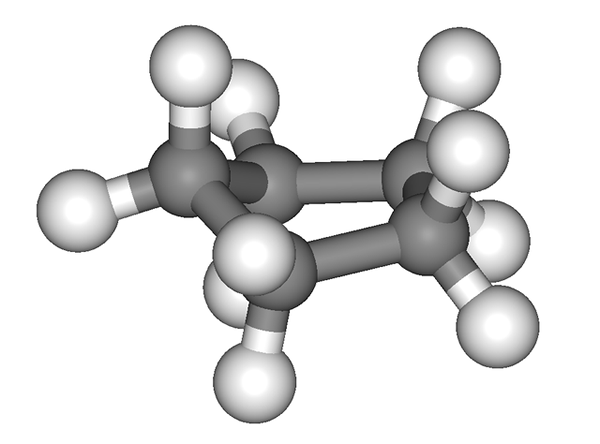 Der Cyclopentano -Ring ist nicht völlig flach. Quelle: Edgar181 [Public Domain]
Der Cyclopentano -Ring ist nicht völlig flach. Quelle: Edgar181 [Public Domain] Das vorherige Bild vermittelt den falschen Eindruck, dass der Zyklus flach ist; Aber das ist nicht so. Alle ihre Kohlenstoffatome haben SP -Hybridisierung3, Ihre Orbitale befinden sich also nicht in derselben Ebene. Ebenso sind Wasserstoffatome, als ob dies nicht genug wäre.
So ist es über Konformationen, von denen einer der Halbstuhl ist (überlegenes Bild). Aus dieser Perspektive ist klar, dass der Cyclopentano -Ring Falten vorstellt, die dazu beitragen.
Diese Spannung ist auf die Tatsache zurückzuführen3.
Trotz dieser Spannung ist der Zyklus eine stabilere und weniger brennbare Verbindung als der Pentaner. Dies kann durch Vergleich seiner Sicherheits -Rhombuss überprüft werden, bei denen die Entflammbarkeit des Zyklus 3 hat, während die des Pentans 4, 4.
Ciclipentano -Eigenschaften
Aussehen
Farblose Flüssigkeit mit einem weichen Geruch ähnlich wie Öl.
Kann Ihnen dienen: ChemiestufenMolmasse
70,1 g/mol
Schmelzpunkt
-93,9 ºC
Siedepunkt
49,2 ºC
Flammpunkt
-37,2 ºC
Selbstdirektionstemperatur
361 ºC
Verdampfungswärme
28,52 kJ/mol bei 25 ºC
Schmiere
0,413 MPa · s
Brechungsindex
1.4065
Dampfdruck
45 kPa bei 20 ° C. Dieser Druck entspricht jedoch etwa 440 atm, jedoch als der der des N-Pentano: 57,90 kPa.
Hier manifestiert sich die Wirkung der Struktur: Der Cyclopentano -Ring ermöglicht effektivere intermolekulare Wechselwirkungen, die im Vergleich zu den linearen Molekülen der linearen Moleküle der linearen Moleküle der linear N-Pentano. Daher hat letzteres einen größeren Dampfdruck.
Dichte
0,751 g/cm3 bei 20 ºC. Andererseits sind seine Dämpfe 2,42 -mal dichter als die Luft.
Löslichkeit
In einem Liter Wasser bei 25 ° C, 156 mg Cyclopentano aufgrund seines hydrophoben Charakters gelöst. Es ist jedoch in apolaren Lösungsmitteln wie anderen Paraffinen, Etherre, Benzol, Kohlenstofftetrachlorid, Aceton und Ethanol mischbar.
Oktanol/Wasserpartitionskoeffizient
3
Reaktivität
Das Radfahren ist stabil, wenn es ordnungsgemäß gespeichert ist. .
In Gegenwart von Sauerstoff verbrennt es in einer Verbrennungsreaktion, sei es vollständig oder unvollständig. Da der Zyklus eine sehr flüchtige Verbindung ist, muss er an Orten gespeichert werden, an denen er keiner Wärmequelle ausgesetzt werden kann.
In Abwesenheit von Sauerstoff erleidet der Cyclopentano eine Pyrolysereaktion, die sich in kleineren und ungesättigten Molekülen zersetzt. .
Es kann Ihnen dienen: MethylalicylatAndererseits kann der Cyclopentano unter ultraviolettem Strahlung mit Brom reagieren. Auf diese Weise wird eine seiner C-H-Bindungen durch C-BR ersetzt, was wiederum durch andere Gruppen ersetzt werden kann. Und so entstehen Cyclopentano -Derivate.
Anwendungen
Industrielles Lösungsmittel
Der hydrophobe und apolare Charakter des Cyclopentano wird durch ein Grad Lösungsmittel neben den anderen paraffinischen Lösungsmitteln hergestellt. .
Ethylenquelle
Wenn der Cyclopentano einer Pyrolyse unterzogen wird, ist Ethylen, das in der Welt der Polymere unzählige Anwendungen hat.
Polyurethan -Isolierschaum
Eine der herausragendsten Verwendungen von Cycopentano ist ein Expansionsmittel für die Herstellung von Polyurethan -Isolierschaum. Das heißt, Cyclopentano -Dämpfe nach ihrem großen Druck, erweitern das polymer.
Einige Unternehmen haben sich entschieden, HFCs durch Cyclopentano bei der Herstellung von Isoliermaterialien zu ersetzen, da sie nicht zur Verschlechterung der Ozonschicht beiträgt und auch die Freisetzung von Treibhausgas an die Umwelt reduziert.
Verweise
- Graham Solomons t.W., Craig b. Braten. (2011). Organische Chemie. (10th Auflage.). Wiley Plus.
- Carey f. (2008). Organische Chemie. (Sechste Ausgabe). Mc Graw Hill.
- Wikipedia. (2020). Cyclopentan. Abgerufen von: in.Wikipedia.Org
- Nationales Zentrum für Biotechnologie Information. (2020). Cyclopentan. Pubchem -Datenbank, CID = 9253. Erholt von: Pubchem.NCBI.NLM.NIH.Regierung
- .V. (2020). Cyclopentan. Scientedirect. Abgerufen von: Scientedirect.com
- GE -Geräte. (11. Januar 2011). . Erholt von: Druckroom..com
- « Emulgatoremulsionsprozess, molekulare Aspekte, Anwendungen
- Industrial City, wie geboren wird, Struktur, Folgen, Probleme »

