Chlorsäure (HCLO2)
- 4733
- 22
- Tizian Liebich
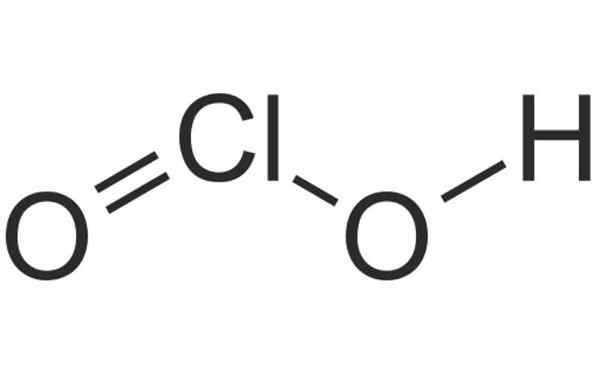
 Chemische Struktur von Chloring -Säure. Quelle: HBF878, Wikimedia Commons
Chemische Struktur von Chloring -Säure. Quelle: HBF878, Wikimedia Commons Was ist Chloro?
Er Chlorsäure Es ist eine anorganische Verbindung der HCLO -Formel2. Diese Säure ist eine der Oxazidensäuren von Chlor, wo sie mit Oxidationszustand 3 gefunden wird+.
Obwohl die Säure in reiner Substanz schwer zu erhalten ist, ist die aus diesen Säuren abgeleitete konjugierte Base, das Chloritionen, stabil. Ein Beispiel für ein Salz dieses Anion ist Natriumchlorit. Diese und andere damit verbundene Salze werden manchmal bei der Herstellung von Chlordioxid verwendet.
Chlorsäure ist eine schwache Säure. Die reine Substanz ist instabil, überproportional mit hypoklorischer Säure (Oxidationsstatus Cl +1) und Chlorsäure (Oxidationszustand CL +5):
2HCLO2 → HCLO + HCLO3
Chlorsäure wird zusammen mit der chlorischen Säure bei der Zersetzung der wässrigen Chlordioxidlösung erhalten.
Die Chlor -Säure -Lösung wurde zuerst durch Reduzieren der Chlorsäure mit Tartarsäure erhalten. Die Hauptmethode zum Erhalten dieser Säure besteht jedoch darin, eine Suspension von Bariumchlorid mit Schwefelsäure zu behandeln:
BA (Clo2)2 + H2SW4 → Baso4 + 2HCLO2
Chlorsäure ist ein starkes Oxidationsmittel.
Chlor ist das einzige Halogen, das eine isolierbare Formel -Säure -HXO bildet2. Weder Bromous -Säure noch Jodosesäure wurden isoliert. Einige Salze von Witzsäure, Witze sind bekannt, aber außer als Vermittler bei Reaktionen gibt es keine Yoditos -Salze.
Physikalische und chemische Eigenschaften
- Chlorsäure ist, wenn es möglich ist zu isolieren, eine farblose Flüssigkeit ohne charakteristisches Aroma.
Es kann Ihnen dienen: Cycloalcinos- Die Verbindung hat ein Molekulargewicht von 68.456 g/mol. Es hat einen Siedepunkt (berechnet) von 502,07 ° C und eine Wasserlöslichkeit von 1 × 10 (berechnet)6 mg/l.
- Der HCLO2 Es ist aufgrund der Dissensreaktion (oder des Unverhältnisses) instabil, um chlorische und hypoklorische Säure zu produzieren, ähnlich der von Brom- und Jodanalogsäuren:
2HCLO2 → HCLO + HCLO3
- Chlorsäure wird als schwache Säure angesehen, obwohl ihre Dissoziationskonstante in der Größenordnung von 1 x 10 liegt-2, Was macht es nicht so schwach wie andere Säuren mit einem PKA von 1,96.
Risiken
Chlorsäure ist eine instabile Verbindung und ein starkes Oxidationsmittel, das mit Reduktionsmitteln und Alkalien nicht kompatibel ist.
Chlorsäure ist im Falle eines Kontakts mit Haut und Augen irritierend und ist bei Aufnahme und Inhalation gefährlich.
Bei Augenkontakt müssen Sie überprüfen, ob Kontaktlinsen verwendet werden, und sie sofort entfernen. Die Augen sollten mindestens 15 Minuten lang mit fließendem Wasser gespült werden und die Augenlider offen halten. Kaltes Wasser kann verwendet werden, aber keine Augensalbe.
Wenn die Chemikalie mit der Kleidung in Kontakt kommt, behalten Sie sie so schnell wie möglich und schützen Sie ihre eigenen Hände und Körper. Legen Sie das Opfer unter eine Sicherheitsdusche.
Wenn sich die Chemikalie in der exponierten Haut des Opfers wie den Händen ansammelt, wird die mit fließende Wasser und nicht abrasive Seife kontaminierte Haut sanft gewaschen und vorsichtig.
Kaltes Wasser kann verwendet werden. Wenn Reizungen bestehen, suchen Sie medizinische Hilfe auf. Waschen Sie kontaminierte Kleidung, bevor Sie sie wieder benutzen.
Kann Ihnen dienen: PhosphatgruppeWenn der Hautkontakt schwerwiegend ist, sollte er mit einer Desinfektionsseife gewaschen werden und die mit einer antibakterielle Creme kontaminierte Haut bedecken.
Im Inhalation sollte das Opfer in einem gut belüfteten Bereich stehen dürfen. Wenn die Inhalation ernst ist, muss das Opfer so bald wie möglich in einen sicheren Bereich evakuiert werden. Lose enge Kleidung wie Hemdhals, Gürtel oder Krawatte.
Wenn das Opfer schwer zu atmen ist, muss Sauerstoff verabreicht werden. Wenn das Opfer nicht atmet, wird eine Wiederbelebung der Mundmund gemacht. Immer berücksichtigt, dass es für die Person gefährlich sein kann, die Hilfe bietet, die Hilfe für die Wiederbelebung des Mundes anbieten, wenn das inhalierte Material giftig, infektiös oder korrosiv ist.
Im Falle einer Aufnahme verursacht es kein Erbrechen. Lösen Sie die enge Kleidung. Wenn das Opfer nicht atmet, machen. In allen Fällen sollte sofortige medizinische Versorgung gesucht werden.
Anwendungen
- Es wurden Studien durchgeführt, bei denen meta-stabile Lösungen von Chlorsäure/Chloroxid wie oraler Spülung zur Plattenreduktion durchgeführt wurden.
Die Studie wurde an eine Gruppe von Freiwilligen von 18 bis 27 Jahren durchgeführt. Seine Auswirkung auf die Entwicklung der Platte und der Speichelzählung wurde getestet, wobei eine Verringerung von bis zu 34,5% reduzierter Dentalplattenwerte im Vergleich zu einer Placebo -Gruppe erhöht wurde.
- Chlorsäure ist an der Herstellung von Natriumsäure Chlorit beteiligt, das antimikrobielle Eigenschaften aufweist und für die Verwendung hauptsächlich als Spray oder Eintauchlösung für Geflügel, Fleisch, Gemüse, Obst und Meeresnahrungsmittel ausgelegt ist. Es wird auch in Corral -Vogelkühlwasser verwendet.
Kann Ihnen dienen: degenerierte Orbitale- Natriumsäurechlorit wird durch Zugabe von Nahrungsmittelqualitätsäure (z2).
Die Kombination von Säure mit der Natriumchloritlösung führt zu Chloritumwandlungen in eine Chlormessersäure (HCLO2).
Naclo2 + H+ ⇌ HCLO2 + N / A+
Diese Lösung kann anschließend eine Mischung mit Chlorit (CLO) bilden2-), Chlordioxid (CLO2) und Chlorid (CLM). Die Reaktion erzeugt eine oxidative Lösung mit oxychlorierten Spezies mit antimikrobiellen Eigenschaften.
- Natriumsäurechlorit ist so konzipiert, dass sie als Teil eines integrierten Ansatzes verwendet werden sollen.
Natriumsäure -Chlorit -Lösung reduziert die Anzahl der Krankheitserreger (zum Beispiel, Escherichia coli, UND. Coli O157: H7, Salmonella spp., Campylobacter spp., Und Listeria monocytogenes).
Verweise
- Chlorsäure. Von EBI geborgen.AC.Vereinigtes Königreich.
- Nationales Zentrum für Biotechnologie Information. Aus Pubchem geborgen.

