Chlorsäure (HCLO3)
- 3010
- 203
- Lewis Holzner
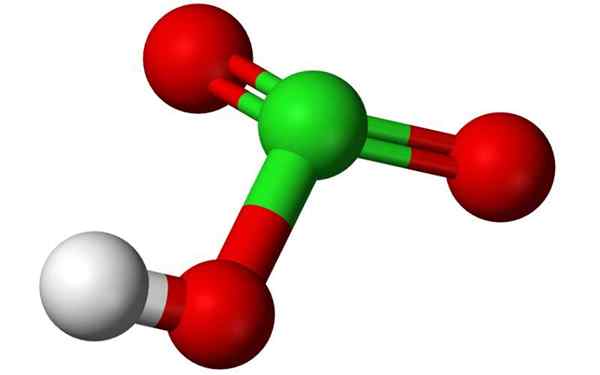
 Chemische Struktur von Chlorsäure in einem 3D -Ballonmodell. Quelle: Benjah-BMM27, Wikimedia Commons
Chemische Struktur von Chlorsäure in einem 3D -Ballonmodell. Quelle: Benjah-BMM27, Wikimedia Commons Was ist Chlorsäure?
Er Chlorsäure Es ist eine anorganische Verbindung der HCLO -Formel3, Eine Oxazid aus Chlor und formaler Vorläufer von Chloratsalzen. Es ist eine starke Säure, die in der Lage ist, einen Wasserstoff an einen Akzeptor oder eine Base Tronsted zu spenden.
Die Verbindung wird mit Bariumchlorat (Barite -Chlorat) mit Schwefelsäure erhalten, um Bariumsulfat zu produzieren, was nach der folgenden Reaktion unlöslich ist:
BA (Clo3)2 + H2SW4 → 2HCLO3 + Baso4
Eine andere Methode zum Erhitzen ist das Erhitzen hypochlorischer Säure, um Chlorsäure und Wasserstoffchlorid gemäß der Reaktion zu erhalten:
3HCLO → HCLO3 + 2HCL
Die Chlorsäure (HCLO3) ist ein starkes Oxidationsmittel, da sie in der Lage ist, auf Oxidationszustände +3, +1 und -1 zu reduzieren. Es wird für die Herstellung von Chloratsalzen verwendet.
Es zersetzt sich in Konzentrationen von mehr als 30%. Es bricht auch beim Erhitzen zusammen, so dass es die ganze Zeit kalt gehalten werden muss, und alle bisher verwendeten Glasgläser müssen zuvor gekühlt werden.
Physikalische und chemische Eigenschaften
- Chlorsäure existiert nur in Lösung. Es ist eine farblose Flüssigkeit ohne charakteristisches Aroma.
- Die Verbindung hat ein Molekulargewicht von 84.459 g/mol und eine Dichte von 1 g/ml bei 25 ° C.
- Es hat einen Siedepunkt von mehr als 100 ° C und eine Wasserlöslichkeit von 40 g pro 100 ml dieses Lösungsmittels bei 25 ° C.
- Die Chlorsäure beschleunigt das Verbrennen brennbarer Materialien und kann die Mehrheit in Kontakt einschalten. Die Verbindung ist für Metalle und Gewebe korrosiv.
Kann Ihnen dienen: CoprecipitationSelbstreaktiv
- Die Konzentrationen von Chlorsäure über 40% zersetzen.
- Antimonsulfid und konzentrierte Lösungen der Chloriksäure reagieren mit Gling.
- Arsensulfid und konzentrierte Lösungen von Chlorsäure reagieren mit Glühlampe.
- Reagiert mit Kraft, explodiert sogar mit anderen Metallsulfiden, dh Kupfersulfid.
- In Kontakt mit oxidierbaren Materialien, einschließlich Ammoniak, können Reaktionen extrem gewalttätig sein.
- Das Filterpapier entzündet sich nach dem Eintauchen in Salzsäure.
- Explosionen wurden durch chlorische Säurelösungsmischungen mit Metallen wie Antimon, Wismut und Eisen aufgezeichnet. Dies ist auf die Bildung von explosiven Verbindungen zurückzuführen, einschließlich Wasserstoff.
Reaktivität und Gefahren
Chlorsäure ist eine instabile Verbindung. Als starke Säure ist es äußerst gefährlich bei Hautkontakt (korrosiv und irritierend), Augenkontakt (irritierend) und bei Aufnahme. Auch das sehr gefährlich bei Inhalation.
Eine schwere Überbelichtung kann zu Lungenschäden, Ersticken, Wissensverlust oder Tod führen. Eine längere Exposition kann zu Hautverbrennungen und Geschwüren führen.
Inhalation Überbelichtung kann Atemreizungen verursachen. Die Entzündung des Auges ist durch Rötung, Bewässerung und Juckreiz gekennzeichnet. Die Hautentzündung ist durch Juckreiz, Schälen, Rötungen und gelegentlich Ampules -Bildung gekennzeichnet.
Die Substanz ist giftig für die Nieren, Lungen und Schleimhäute. Wiederholte oder längere Exposition gegenüber der Substanz kann diese Organe beschädigen.
Bei Augenkontakt müssen Sie überprüfen, ob Kontaktlinsen verwendet werden, und sie sofort entfernen. Die Augen sollten mindestens 15 Minuten lang mit fließendem Wasser gespült werden und die Augenlider offen halten. Kaltes Wasser kann verwendet werden. Es sollten keine Augenblätter verwendet werden.
Kann Ihnen dienen: Acetonitril (C2H3n)Wenn die Chemikalie mit der Kleidung in Kontakt kommt, behalten Sie sie so schnell wie möglich und schützen Sie ihre eigenen Hände und Körper. Legen Sie das Opfer unter eine Sicherheitsdusche.
Wenn sich die Chemikalie in der exponierten Haut des Opfers wie den Händen ansammelt, wird die mit fließende Wasser und nicht abrasive Seife kontaminierte Haut sanft gewaschen und vorsichtig.
Sie können Säure auch mit verdünntem Natriumhydroxid oder mit einer schwachen Base wie Natriumbicarbonat neutralisieren. Wenn Reizungen bestehen, suchen Sie medizinische Hilfe auf. Waschen Sie die kontaminierte Kleidung, bevor Sie sie erneut verwenden.
Wenn der Hautkontakt schwerwiegend ist, sollte er mit einer Desinfektionsseife gewaschen werden und die mit einer antibakterielle Creme kontaminierte Haut bedecken.
Im Inhalation sollte das Opfer in einem gut belüfteten Bereich stehen dürfen. Wenn die Inhalation ernst ist, muss das Opfer so bald wie möglich in einen sicheren Bereich evakuiert werden.
Lose enge Kleidung wie Hemdhals, Gürtel oder Krawatte. Wenn das Opfer schwer zu atmen ist, muss Sauerstoff verabreicht werden. Wenn das Opfer nicht atmet, wird eine Wiederbelebung der Mundmund gemacht.
Es sollte berücksichtigt werden, dass es für die Person, die Hilfe bietet, gefährlich sein kann.
Im Falle einer Aufnahme verursacht es kein Erbrechen. Lose enge Kleidung wie Hemdhälse, Gürtel oder Krawatten. Wenn das Opfer nicht atmet, machen. In allen Fällen sollte sofortige medizinische Versorgung gesucht werden.
Anwendungen
Die Chlorsäure wird hauptsächlich zur Bildung von Chlortsalzen wie Natrium, Kalzium, Magnesium, Strontium, Blei, Kupfer und Silberchlor sowie zum Protoclorat- und Quecksilberpercelor verwendet, das unter Verwendung der Chlorsäure als Reagenz als Reagenz als Reagenz hergestellt wird als Reagenz.
Kann Ihnen dienen: enzymatische Aktivität: Einheit, Messung, Regulierung und FaktorenStabiler Vorläufer von Chlordioxid, wird in der Elektrochemie -Produktion von Hochreinheit Ammonium verwendet.
Die Hauptproduktion von Chlorsäure begann während der industriellen Revolution in Europa und wurde zur Herstellung von Vinylchlorid für PVC -Rohre verwendet.
Eine weitere Verwendung für Säure in zahlreichen kleineren Anwendungen, einschließlich Hausreinigung, Gelatineproduktion und anderen Lebensmittelzusatzstoffen, Dekalkifizierung und Lederverarbeitung.
Verweise
- Chlorsäure (s).F.). Von Weebly geborgen.com.
- Chlorsäure (s).F.). Aus Chemicalbook wiederhergestellt.com.

