Struktur für Eisenchlorid (FECL2), Verwendungen, Eigenschaften

- 3675
- 1095
- Medine Kedzierski
Er Eisen Chlorid Es ist ein anorganischer Feststoff, der von der Vereinigung eines Glaubenskation gebildet wird2+ und zwei Anionen Chlorid CL-. Seine chemische Formel ist FECL2. Es neigt dazu, Wasser aus der Umwelt zu absorbieren. Eines seiner Hydrate ist Fecl Tetrahydrat2 •4H2Oder was ein grünlicher Feststoff ist.
Markieren Sie, dass es in Wasser sehr löslich ist und in Gegenwart von Luft, die das Eisen -Fecl -Chlorid bildet, leicht oxidieren3. Um leicht oxidierbar zu sein und daher in der Lage zu sein, als Reduzierer zu fungieren.
 Ferroso Tetrahydratchlorid -Fecl2 •4H2Oder fest. Craven [CC BY-SA 3.0 (https: // creativecommons.Org/lizenzen/by-sa/3.0)]]. Quelle: Wikimedia Commons.
Ferroso Tetrahydratchlorid -Fecl2 •4H2Oder fest. Craven [CC BY-SA 3.0 (https: // creativecommons.Org/lizenzen/by-sa/3.0)]]. Quelle: Wikimedia Commons. Eisenchlorid hat mehrere Verwendungszwecke, darunter anderen Mitteln bei der Oxidation von Schlamm, die aus Abwasser- oder Abwasserbehandlung stammen. Es wird auch im Metall -Eisenbeschichtungsprozess verwendet und hat einige Verwendungszwecke in der Pharmaindustrie.
Die FECL -Verwendung wurde ebenfalls erfahren2 Bei der Wiederherstellung wertvoller Metalle der verbrauchten Katalysatoren in den Abgasrohren von Fahrzeugen, die mit Benzin oder Diesel arbeiten.
Es wird in der Textilindustrie verwendet, um Farben in einigen Arten von Stoff zu reparieren.
[TOC]
Struktur
Eisen Chlorid wird durch ein Eisen -Glaubension gebildet2+ und zwei Ionen Chlorid CL- Durch ionische Verbindungen vereint.
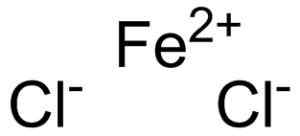 Ferroso Chloruro Fecl2 Wo sind die Ionen, die es ausmachen. EPOP [Public Domain]. Quelle: Wikimedia Commons.
Ferroso Chloruro Fecl2 Wo sind die Ionen, die es ausmachen. EPOP [Public Domain]. Quelle: Wikimedia Commons. Der Eisen Glaube2+ Es hat die folgende elektronische Struktur:
1s2, 2s2 2 p6, 3s2 3p6 3d6, 4s0
wo Sie sehen können, dass Sie zwei Elektronen der 4S -Schicht verloren haben.
Diese Konfiguration ist nicht sehr stabil und aus diesem Grund tendenziell oxidieren, dh ein anderes Elektron, diese Zeit der 3D -Schicht, die das Glaube bildet3+.
Für seinen Teil das Ion Chlorid CL- Es hat die folgende elektronische Struktur:
1s2, 2s2 2 p6, 3s2 3p6
Wo Sie sehen können, dass Sie ein zusätzliches Elektron in Layer 3P erhalten haben, um es zu vervollständigen. Diese Konfiguration ist sehr stabil, da alle elektronischen Schichten abgeschlossen sind.
Nomenklatur
- Eisen Chlorid
- Eisenchlorid (ii)
Es kann Ihnen dienen: Bestimmung der Asche: Methoden und Beispiele- Eisendichlorid
- Tetrahydrat -Eisenchlorid: FECL2 •4H2ENTWEDER
Eigenschaften
Körperlicher Status
Farbenfroh bis hellgrün, Kristalle.
Molekulargewicht
126,75 g/mol
Schmelzpunkt
674 ºC
Siedepunkt
1023 ºC
Bestimmtes Gewicht
3,16 bis 25 ° C/4 ºC
Löslichkeit
Sehr löslich in Wasser: 62,5 g/100 ml bei 20 ° C. Löslich in Alkohol, Aceton. Etwas löslich in Benzol. Praktisch unlöslich im Äther.
Andere Eigenschaften
Der Fecl2 wasserzutäuger ist sehr hygroskopisch. Absorbieren Sie mit Leichtigkeit der Umwelt Wasser und bilden eine Vielzahl von Hydraten, insbesondere das Tetrahydrat, in dem für jedes FECL -Molekül2 Es gibt 4 Stunden Moleküle2Oder damit verbunden (FECL2 •4H2ENTWEDER).
In Gegenwart von Luft oxidiert es langsam zu FECL3. Dies bedeutet, dass der Glaube Ion2+ Leicht zu ionischen Glauben oxidiert3+.
Wenn Sie in Gegenwart von Schnellluft -Eisen -Chlorid -FECL erwärmen3 Und Eisenoxid Fe2ENTWEDER3.
Der Fecl2 Es ist korrosiv für Metalle und Gewebe.
Erhalten
Es wird erhalten, indem ein Überschuss an eisernem Glauben mit wässriger Lösung von HCl -Salzsäure bei hohen Temperaturen behandelt wird.
Glaube0 + 2 HCl → FECL2 + 2 h+
Aufgrund des Vorhandenseins von Wasser durch diese Methode wird jedoch Eisen -Tetrahydratchlorid erhalten2 •4H2ENTWEDER.
Um wasserfrei (ohne Wasser in die Kristalle eingebaute Wasser) zu erhalten, haben einige Forscher die Reaktion von Eisenstaub mit wasserfreiem Hügeln (ohne Wasser) im Tetrahydrofuran -Lösungsmittel (THF) bei einer Temperatur von 5 ° C ausgewählt.
Die FECL -Verbindung wird auf diese Weise erhalten2 •1,5thF, das bei 80-85 ° C in der Hohlraum oder in Stickstoffatmosphäre (um das Vorhandensein von Wasser zu vermeiden) die FECL erzeugt2 wasserfrei.
Anwendungen
Eisen Chlorid hat verschiedene Verwendungszwecke, die auf seiner reduzierenden Kapazität basieren, dh es kann leicht oxidiert werden. Es wird beispielsweise in Gemälden und Beschichtungen verwendet, da es hilft, sie von der Oberfläche zu reparieren.
Eisen ist ein essentieller Mikronährstoff für die menschliche Gesundheit und einige Tiere. Es ist an der Proteinsynthese, der Atmung und der Multiplikation von Zellen beteiligt.
Deshalb der FECL2 Es wird in pharmazeutischen Präparaten verwendet. Das Glaube Ion2+ Als solches ist es besser absorbiert als der Glaube Ion3+ Im Darm.
Kann Ihnen dienen: Calciumcarbonat: Struktur, Eigenschaften, Bildung, verwendetEs wird für die FECL -Herstellung verwendet3. Es wird in Metallurgie und in Eisenbeschichtungen verwendet, um eine duktilere Ablagerung zu ermöglichen.
Hier sind andere prominente Verwendungen.
In Stofffärbung
Der Fecl2 Es wird in einigen Arten von Stoff als unterbrochener oder farbiger Fixiermittel verwendet. Der Unterricht reagiert chemisch und verbindet sich gleichzeitig mit dem Farbstoff und dem Stoff, der eine unlösliche Verbindung darf.
Auf diese Weise ist der Farbstoff am Stoff befestigt und seine Farbe verstärkt sich.
 Eisen Chlorid Fecl2 Ermöglicht die Fixierung der Farben auf Stoffen. Gina Pina [CC von 2.0 (https: // creativecommons.Org/lizenzen/by/2.0)]]. Quelle: Wikimedia Commons.
Eisen Chlorid Fecl2 Ermöglicht die Fixierung der Farben auf Stoffen. Gina Pina [CC von 2.0 (https: // creativecommons.Org/lizenzen/by/2.0)]]. Quelle: Wikimedia Commons. In Abwasserbehandlung
Der Fecl2 Es wird in Abwasser- oder Abfallbehandlungsanlagen (Abwasserwasser) verwendet.
In dieser Anwendung beteiligt sich das Eisenchlorid durch einen Prozess, der als Fenton -Oxidation bezeichnet wird. Diese Oxidation bewirkt das Bruch von Schlammfächern und ermöglicht die Freisetzung von Wasser, die stark daran befestigt ist.
 Abschnitt einer Abwasserbehandlungsanlage, in der Sie den Schlamm sehen können. Manchmal wird dies mit Ferroso -Fecl -Chlorid behandelt2 damit es leichter von Wasser getrennt werden kann. Evelyn Simak/Abwasser arbeitet nördlich von Dickleburgh. Quelle: Wikimedia Commons.
Abschnitt einer Abwasserbehandlungsanlage, in der Sie den Schlamm sehen können. Manchmal wird dies mit Ferroso -Fecl -Chlorid behandelt2 damit es leichter von Wasser getrennt werden kann. Evelyn Simak/Abwasser arbeitet nördlich von Dickleburgh. Quelle: Wikimedia Commons. Dann kann der Schlamm trocknen und wegwerfen. Die Verwendung von Eisen Chlorid senkt die Prozesskosten.
Kürzlich wurde auch vorgeschlagen, die Bildung von Sulfidgas oder Wasserstoffsulfid in den Abwasserkanälen zu verringern.
Auf diese Weise würden die Korrosion, die durch dieses Gas und die unangenehmen Gerüche erzeugt werden, verringert.
In chemischen Studien
Für seine reduzierenden Eigenschaften (das Gegenteil der Oxidation) des FECL2 Es wird in verschiedenen Forschungen in Laboratorien Chemie, Physik und technische Ingenieurwesen häufig verwendet.
Bestimmte Wissenschaftler verwendeten Eisen Chloriddampf.
Diese Katalysatoren werden verwendet, um schädliche Gase für menschliches Wesen und die Umwelt zu beseitigen. Sie befinden sich im Fluchtrohr von Autos und Lastwagen, die mit Benzin oder Diesel arbeiten.
Kann Ihnen dienen: Molmasse: Wie sie berechnet wird, Beispiele und gelöste Übungen Abgabrohr eines Fahrzeugs, in dem ein voluminöserer Abschnitt beobachtet wird, an dem sich der Katalysator befindet, um schädliche Gase mit der Umwelt in freundliche Gase umzuwandeln. Ahanix1989 bei English Wikipedia [Public Domain]. Quelle: Wikimedia Commons.
Abgabrohr eines Fahrzeugs, in dem ein voluminöserer Abschnitt beobachtet wird, an dem sich der Katalysator befindet, um schädliche Gase mit der Umwelt in freundliche Gase umzuwandeln. Ahanix1989 bei English Wikipedia [Public Domain]. Quelle: Wikimedia Commons. Nach einer bestimmten Zeit wird der Katalysator für das Fahrzeug ausgegeben und verliert Effektivität und Sie müssen es ersetzen. Der verbrauchte Katalysator wird verworfen und es werden Anstrengungen unternommen, um die wertvollen Metalle, die er enthält.
 Keramiknetz des Katalysators, in dem sich die Spuren wertvoller Metalle mit FECL erholen, die sich erholen können2. Global-kat Recycling [CC BY-SA 3.0 (https: // creativecommons.Org/lizenzen/by-sa/3.0)]]. Quelle: Wikimedia Commons.
Keramiknetz des Katalysators, in dem sich die Spuren wertvoller Metalle mit FECL erholen, die sich erholen können2. Global-kat Recycling [CC BY-SA 3.0 (https: // creativecommons.Org/lizenzen/by-sa/3.0)]]. Quelle: Wikimedia Commons. Nach Angaben der Forscher bildeten diese Metalle mit dem Eisen des Eisenchlorids Magnetlegierungen.
Die Legierungen konnten mit Magneten extrahiert werden und haben dann die wertvollen Metalle nach bereits bekannten Methoden gewonnen.
In biochemischen Studien
Für den Besitz des Glaubens Kation2+, Das ist ein wichtiger Mikronährstoff beim Menschen und einigen Tieren, der FECL2 Es wird in Biochemie und Medizinstudien verwendet.
Bestimmte Studien, die nachweisen dürfen, dass Eisenchlorid die fungizide Wirksamkeit von Argon -Kaltplasma verbessert.
Kaltplasma ist eine Technologie zur Sterilisation medizinischer Oberflächen und Instrumente. Es basiert auf der Bildung von Hydroxylradikalen aus der Luftfeuchtigkeit der Umwelt. Diese Radikale reagieren mit der Zellwand des Mikroorganismus und verursachen ihren Tod.
In dieser Untersuchung das FECL2 Die Wirkung von kaltem Plasma verbesserte und beschleunigte die Eliminierung eines Pilzes, der gegen andere Desinfektionsmethoden resistent ist.
Einige Wissenschaftler fanden heraus, dass die Verwendung von FECL2 Es ermöglicht eine zunehmende Leistung bei Glukose, die Reaktionen auf der Grundlage von Zuckerrohrbagasse erhalten.
In diesem Fall Glaube sein2+ Ein wesentlicher Mikroement für die menschliche Gesundheit, die Präsenz in Spuren im Produkt würde den Menschen nicht beeinflussen.
Verweise
- Fukuda, s. et al. (2019). Eisen Chlorid und Eisensulfat verbessern die fungizide Wirksamkeit von kaltem atmosphärischem Argonplasma auf melanisiertem Aureobasidium Pullulans. J Biosci Bioeng, 2019, 128 (1): 28-32. NCBI erholte sich.Clm.NIH.Regierung.
- Ismal, oder.UND. und yildirim, l. (2019). Metallgebebags und Biomordanten. In den Auswirkungen und Aussichten einer grünen Chemie für die Textiltechnologie. Kapitel 3, pp.57-82. Von Scientedirect erholt.com.
- Zhang, w. et al. (2019). Ko-Katalyse von Magnesiumchlorid und Eisenchlorid für Xylo-Oligosaccharide und Glucoseproduktion aus Zuckerrohrbagasse. Bioresoral Technol 2019, 291: 121839. NCBI erholte sich.NLM.NIH.Regierung.
- Zhou, x. et al. (2015). Rolle des indigenen Eisen bei der Verbesserung der Schlammentwässerbarkeit dieser Peroxidation. Wissenschaftliche Berichte 5: 7516. NCBI erholte sich.NLM.NIH.Regierung.
- RATHNAYAKE, d. et al. (2019). Wasserstoffsulfidkontrolle in Abwasserkanälen durch Katalyse der Reaktion mit Sauerstoff. Wissenschaft des Gesamtumfelds 689 (2019) 1192-1200. NCBI erholte sich.NLM.NIH.Regierung.
- Taninouchi und. und Okabe, t.H. (2018). Wiederherstellung von Platingruppenmetallen von verbrauchten Katalysatoren unter Verwendung von Eisenchloriddampfbehandlung. Metall und Materi Trans B (2018) 49: 1781. Link wiederhergestellt.Springer.com.
- ODER.S. Nationalbibliothek für Medizin. (2019). Eisen Chlorid. Erholt von: Pubchem.NCBI.NLM.NIH.Regierung.
- Aresta, m. et al. (1977). Eisen (0) Oxidation durch Wasserstoffchlorid in Tetrahydrofuran: Einfacher Weg zum wasserfreien Eisen (II) Chlorid. Anorganische Chemie, vol. 16, nein. 7, 1977. Aus Pubs geborgen.ACS.Org.
- Baumwolle, f. Albert und Wilkinson, Geoffrey. (1980). Fortgeschrittene anorganische Chemie. Vierte Edition. John Wiley & Söhne.
- « Portugal Flag -Geschichte und Bedeutung (überarbeitete Bilder)
- Herkunft der christlichen Ethik, Grundlagen, Vertreter »

