Chemische Verbindung
- 1525
- 24
- Medine Kedzierski
Wir erklären, aus welchen chemischen Verbindungen bestehen, welche Typen existieren, welche Unterschiede zu den chemischen Elementen bestehen, und geben mehrere Beispiele an.
 Chemische Verbindungen sind alle Substanzen, die Atome von zwei verschiedenen chemischen Elementen aufweist
Chemische Verbindungen sind alle Substanzen, die Atome von zwei verschiedenen chemischen Elementen aufweist Was ist eine chemische Verbindung?
A chemische Verbindung Es ist eine Substanz, die durch die Vereinigung von zwei oder mehr Atomen verschiedener chemischer Elemente gebildet wird. Die chemischen Verbindungen bleiben dank der chemischen Bindungen vereint, die mit den Elektronen der verknüpften Atome zusammenhängen. Das heißt, in einer chemischen Verbindung intervenieren die (äußersten) Elektronen der Atome in die Bildung der Glieder.
Die Komponenten chemischer Verbindungen (chemische Elemente) können nicht durch physikalische Methoden voneinander getrennt werden: Destillation, Zentrifugation, Filtration usw., Erfordernder chemischer Methoden, um dies zu erreichen.
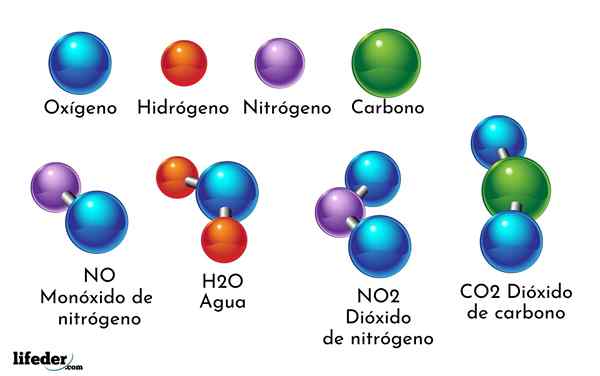
Ein Beispiel für chemische Verbindung ist Wasser. Es wird nur durch zwei Atome von zwei verschiedenen chemischen Elementen gebildet: Sauerstoff und Wasserstoff mit der chemischen Formel H2ENTWEDER. Daher binden zwei H an eins oder an die H2ENTWEDER.
Ein chemisches Element ist im Gegensatz zu chemischen Verbindungen der einfachste und grundlegendste Weg, der Materie darstellt. Es wird als ein einzigartiges Atomtyp vorgestellt, der durch chemische Reaktionen nicht in einfachere Substanzen unterteilt werden kann.
Arten von chemischen Verbindungen
Chemische Verbindungen können hauptsächlich nach zwei Kriterien klassifiziert werden:
- Entsprechend der Art der Bindung, die die in der chemischen Verbindung vorhandenen chemischen Elemente vereint.
- Gemäß Zusammensetzung und Struktur der chemischen Verbindung.
Gemäß der Art der Verbindung
Abhängig von der Art der Verbindung können chemische Verbindungen:
- Moleküle. Es sind chemische Verbindungen, die durch zwei oder mehr Arten verschiedener chemischer Elemente gebildet werden, die durch eine kovalente Bindung verbunden sind. Dieser Link ist durch das Teilen eines oder mehrere Paare externer Elektronen oder Valencia zwischen zwei Atomen gekennzeichnet.
- Ionen. Elektrisch beladene chemische Verbindungen werden als Ionenchemieverbindungen bezeichnet und ihre Ionen werden durch die vereint Ionic Link. Diese Bindung tritt beim Verbinden eines chemischen Elements des Metalltyps mit einem nicht -metal -chemischen Element auf.
- Intermetallische Verbindungen. Es ist eine Art Metalllegierung, die ein festes Material besteht, das zwischen zwei oder mehr chemischen Metallelementen liegt, um sie zusammenzuhalten.
- Koordinierung. Sie werden durch ein zentrales metallisches Element gebildet, das als Koordinationszentrum bezeichnet wird und eine Reihe von Vereinigten Molekülen oder Ionen, die als Liganden bezeichnet werden, umgeben. Hämoglobin ist zum Beispiel ein Protein, das in roten Blutkörperchen vorkommt und Sauerstoff im Blut transportiert. Hämoglobin hat eine Koordinationsverbindung namens Grupo Hemo. In der Mitte des Hämos befindet sich ein Eisenatom, das den Sauerstofftransport durch Hämoglobin interveniert.
Nach Zusammensetzung und Struktur
Nach diesem Kriterium werden chemische Verbindungen als organisch und anorganisch eingestuft.
- Organische Verbindungen. Es sind Verbindungen, deren Hauptchemikaliell -Element Kohlenstoff ist, die normalerweise Verbindungen mit Atomen desselben Kohlenstoffs und Wasserstoffs bilden. Sie sind jedoch auch vorhanden, wenn auch in geringerem Maße, Sauerstoff, Stickstoff, Schwefel, Bor, Phosphor usw. Organische Verbindungen können sein:
- Aliphatisch. Die Moleküle der aliphatischen Verbindungen können lineare oder zyklische Formen haben, dh in geschlossenen Formen wie Dreiecken, Quadräten, Pentagonen usw. Sie können Kohlenstoffbindungen von drei Typen haben: Einfach (C-C), Double (C = C) oder Triple (C≡C).
- Aromatisch. Sie sind zyklische Verbindungen, die abwechselnd einfache Kohlenstoffkohlenstoffbindungen und doppelte Kohlenstoffkohlenstoffbindungen aufweisen.
- Heterocyclic. Sie sind Verbindungen mit einer zyklischen Struktur, die den Austausch eines Kohlenstoffatoms durch ein anderes chemisches Element (O, S, N usw.) aufweisen kann (O, S, N usw.).
- Organometallisch. Sie sind organische Verbindungen, die in ihren Metallelementen der Zusammensetzung auftreten können.
- Polymere. Es handelt.
- Anorganische Verbindungen. Anorganische Verbindungen haben im Gegensatz zu organischen keine Kohlenstoff als zentrales chemisches Element, sondern eingreifen in ihre Zusammensetzung die meisten bekannten chemischen Elemente. Anorganische Verbindungen können sein:
- Grundoxide. Sie werden durch die Reaktion eines metallchemischen Elements wie Natrium, Kalzium, Eisen, Kupfer usw. gebildet., Mit Sauerstoff. Zum Beispiel ist Natriumoxid (NaO) ein Basisoxid. Sie werden Basisoxide genannt, weil sie zu den Basen oder Hydroxiden führen werden.
- Säureoxide. Sie stammen von der Reaktion eines nicht -metallischen chemischen Elements wie Chlor, Fluor, Schwefel, Brom usw., Mit Sauerstoff. Zum Beispiel Bromoxid (BR2ENTWEDER5) Es ist ein Säuroxid. Sie werden Säureoxide genannt, weil sie zu Säuren führen.
- Hydrors. Sie präsentieren in ihrer chemischen Zusammensetzung das Vorhandensein von Wasserstoff. Es gibt zwei Arten: metallische Hydros und nicht -metallische Hydrors.
- Metall. Sie werden durch die Reaktion von Wasserstoff mit dem Oxidationszustand -1 mit einem Metall gebildet. Diese chemischen Verbindungen sind die einzigen, bei denen Wasserstoff mit dem Oxidationszustand -1 vorhanden ist. Zum Beispiel CAH2 Es ist Calciumhydrid.
- Nicht metallisch. Sie werden durch die Reaktion von Wasserstoff mit Oxidationszustand + 1 mit einem nicht -metallischen Element mit seinem niedrigeren Oxidationszustand gebildet. Chlorhydrid (HCl) ist ein Gas, das bei Salzsäure in Wasser gelöst wird.
- Säuren. Sie sind anorganische chemische Verbindungen, obwohl es organische Säuren gibt, die einen pH -Wert von weniger als 7 haben und sich der Farbe von Rot -Red -Papier zu Rot wenden. Sie können in Hydrocycids und Oxaziden eingeteilt werden.
- Hydrapie. Sie stammen aus der Reaktion von Wasserstoff mit einem Nicht -Metall, um ein Hydrid zu bilden, das in Wasser auflöst, eine Säure; Zum Beispiel iarhydrische Säure (HI).
- Oxcaziden. Es stammt aus der Reaktion eines Oxids eines nicht -metallischen chemischen Elements mit Wasser. Zum Beispiel Schwefeloxidreaktion (also3) Mit Wasser produziert Schwefelsäure (h2SW4).
- Du gehst raus. Sie sind chemische Verbindungen, die durch die Wechselwirkung von Säure- und Grundverbindungen stammen. In seiner Komposition kann es so viele Metallelemente wie nicht -metallisch geben. Salze werden als:
- Neutrale Salze. Sie stammen aus einer Reaktion der Neutralisation zwischen einer Säure und einer Basis mit der Bildung von Salz und Wasser. Beispielsweise erzeugt die Natriumhydroxidreaktion (NaOH) mit Salzsäure (HCl) Natriumchlorid (NaCl), Salz und Wasser. Sie werden als neutral bezeichnet, weil sie keine Variation des pH -Werts erzeugen.
- Säuresalze. Sie werden durch die Reaktion eines Metallhydroxids mit Valencia +1 mit einer Säure mit mehreren Hydrogenen gebildet. Die Reaktion von Lithiumhydroxid (Lioh) mit Kohlensäure (H)2CO3), erzeugt den Ersatz von nur einem Wasserstoff durch Lithium, wodurch das Bicarbonat von Lithium (Lihco3) Ein Säuresalz und Wasser.
- Basissalze. Sie werden durch die Reaktion einer Basi. Bei der Reaktion von Säure mit Calciumhydroxid, CA (OH)2, Ein Chloratom ersetzt eine Hydroxylgruppe (OH). Dies erzeugt Calciumhydroxychlorid (Cuckloh), ein Basissalz und Wasser.
Unterschiede zwischen chemischen Verbindungen und chemischen Elementen
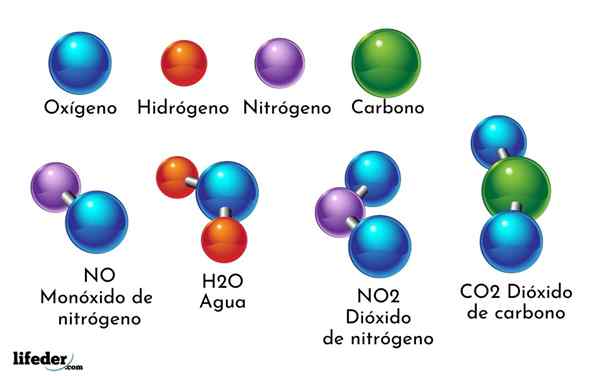 Die chemischen Elemente und die chemischen Verbindungen hoch. Chemische Verbindungen werden durch die obigen Elemente gebildet
Die chemischen Elemente und die chemischen Verbindungen hoch. Chemische Verbindungen werden durch die obigen Elemente gebildet Jedes chemische Element entspricht einem bestimmten Atom und nur mit dieser Art von Atom; Das heißt, ein chemisches Element hat keine unterschiedlichen Arten von Atomen. Das Atom ist das Elementarteilchen der Materie, das nicht durch physikalische oder chemische Methoden geteilt wird.
Das Atom eines chemischen Elements kann mit den Atomen anderer chemischer Elemente zur Bildung chemischer Verbindungen verbunden werden, die unter Verwendung chemischer Methoden in ihre Komponenten (chemische Elemente) unterteilt werden können.
Die chemischen Elemente und chemischen Verbindungen mit einem Puzzle können ausgestattet werden: Die Puzzleteile haben unterschiedliche Eigenschaften, sodass sie den chemischen Elementen entsprechen können.
Die Puzzleteile können sich verbinden, um verschiedene Figuren zu bilden. Die gebildeten Zahlen könnten mit chemischen Verbindungen gleichgesetzt werden. Sobald die Aktivität beendet ist.
Beispiele für chemische Verbindungen
Im Folgenden finden Sie eine Reihe von Beispielen für tägliche chemische Verbindungen:
- HCL: Salzsäure
- H2S: Sulfhydsäure
- HF: Fluorhydsäure
- H2SW4: Schwefelsäure
- HCLO4: Perchlorsäure
- H3Po4: Phosphorsäure
- H2CO3: Kohlensäure
- Hno3: Salpetersäure
- NaOH: Natriumhydroxid
- CA (OH)2: Kalziumhydroxid
- Glaube (OH)2: Eisenhydroxid
- Glaube (OH)3: Eisenhydroxid
- Nah: Natriumhydrid
- Cu2O: Kupferoxid
- Cuo: Cupricoxid
- Glaube2ENTWEDER3: Eisenoxid
- Cl2ENTWEDER7: Perchloroxid
- Br2O: hipobromes Oxid
- Yo2ENTWEDER3: Hypoyodoseoxid
- NaCl: Natriumchlorid
- Fecl3: Eisenchlorid
- HCO3: Natriumbicarbonat
- CH3Pfad: Natriumacetat
- N / A2SW4: Natriumsulfat
- Feso4: Eisensulfid
- H2O: Wasser
- CO2: Kohlendioxid
- C6H12ENTWEDER6: Glukose
- C12H22ENTWEDERelf: Saccharose
Andere Themen von Interesse
Chemische Reaktionen
Chemie im Alltag: Beispiele
Organische Verbindungen
Anorganische Verbindungen
Chemische Bindung
Reine Substanzen
Verweise
- Whitten, Davis, Peck & Stanley. (2008). Chemie. (8. Aufl.). Cengage Lernen.
- Wikipedia. (2021). Chemische Verbindung. Abgerufen von: in.Wikipedia.Org
- Helmestine, Anne Marie, ph.D. (27. August 2020). Verbindungsdefinition in der Chemie. Erholt von: thoughtco.com
- TOPPR. (S.F.). Was ist Verbindung in der Chemie? Arten der chemischen Verbindung. Erholt von: topppr.com

