Quartärverbindungen Eigenschaften, Training, Beispiele
- 4050
- 772
- René Riediger
Der Quartärverbindungen Sie sind alle, die vier verschiedene Atome oder Ionen haben. Daher können sie molekulare oder ionische Spezies sein. Seine Vielfalt deckt sowohl die organische als auch die anorganische Chemie ab und ist eine sehr sperrige Gruppe. Obwohl vielleicht nicht so sehr im Vergleich zu binären oder ternären Verbindungen.
Der Grund, warum Ihre Zahl kleiner ist, ist, dass die vier Atome oder Ionen durch ihre chemischen Affinitäten vereint werden müssen. Nicht alle Elemente sind miteinander kompatibel und noch weniger, wenn sie als Quartett betrachtet werden. Plötzlich sind ein paar von ihnen mehr miteinander verwandt als mit dem anderen Paar.
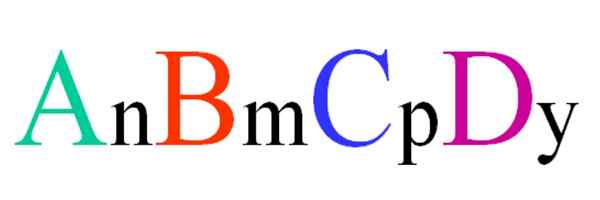 Allgemeine und zufällige Formel für eine quaternäre Verbindung. Quelle: Gabriel Bolívar.
Allgemeine und zufällige Formel für eine quaternäre Verbindung. Quelle: Gabriel Bolívar. Betrachten Sie eine quaternäre Verbindung der ABCD -Zufallsformel. Die Indexs N, M, P e y sind die stöchiometrischen Koeffizienten, die wiederum angeben, welcher Anteil jedes Atoms in Bezug auf die anderen ist.
Somit ist Formel aNBMCPDUnd Es wird gültig sein, wenn es Elektroneuterität erfüllt. Darüber hinaus ist eine solche Verbindung möglich, wenn ihre vier Atome nahe genug miteinander sind. Es ist zu sehen, dass diese Formel nicht für viele Verbindungen, sondern insbesondere für Legierungen oder Mineralien gilt.
[TOC]
Eigenschaften von quaternären Verbindungen
Chemikalien
Eine quaternäre Verbindung kann ionisch oder kovalent sein und die erwarteten Merkmale für ihre Natur aufweisen. Es wird erwartet, dass ABCD -Verbindungen in Wasser, Alkoholen oder in anderen polaren Lösungsmitteln löslich sein. Sie müssen hohe Siede- und Fusionspunkte haben und gute Stromtreiber sein, wenn sie verschmelzen.
In Bezug auf ABCD -kovalente Verbindungen bestehen die meisten aus Stickstoff-, Sauerstoff- oder halogenierten organischen Verbindungen; Das heißt, seine Formel würde c werdenNHMENTWEDERPNUnd oder cNHMENTWEDERPXUnd, X ist ein Halogenatom. Von diesen Molekülen wäre es logisch zu glauben, dass sie angesichts der hohen Elektronegativitäten von O, N und X polar waren.
Kann Ihnen dienen: Natriumchlorid (NaCl)Eine rein kovalente ABCD-Verbindung kann viele Verbindungsmöglichkeiten haben: A-B, B-C, D-A usw., Abhängig von den Affinitäten und elektronischen Fähigkeiten von Atomen. Während in einer rein ionischen ABCD -Verbindung ihre Wechselwirkungen elektrostatisch sind: a+B-C+D-, Zum Beispiel.
Bei einer Legierung, die eher als eine feste Mischung als eine Verbindung als richtig gespielt angesehen wird, besteht ABCD aus neutralen Atomen in basalen Zuständen (theoretisch) aus neutralen Atomen.
Der Rest kann eine ABCD.
Physisch
Physikalisch gesehen ist es wahrscheinlich, dass ABCD kein Gas wird, da vier verschiedene Atome immer eine größere molekulare Masse oder Formulierung beinhalten. Wenn es sich nicht um eine Flüssigkeit mit einem hohen Siedepunkt handelt, wird erwartet, dass es ein Feststoff ist, dessen Zerlegung viele Produkte erzeugen muss.
Wieder seine Farben, Geruch, Textur, Kristalle usw., Sie werden der Art und Weise unterliegen, wie sie A, B, C und D in der Verbindung koexistieren, und werden von ihren Synergien und Strukturen abhängen.
Nomenklatur
Bisher wurde die Frage von quartären Verbindungen auf globale und ungenaue Weise angesprochen. Abgesehen von organischer Chemie (Amidas, Benchilo -Chloride, quaternäre Ammoniumsalze usw.) In der anorganischen Chemie gibt es gut definierte Beispiele, die als saure und grundlegende Oxisals bezeichnet werden.
Säureoxisals
Säureoxisals sind solche. Somit werden ein oder mehrere seiner Hydringen durch Metallkationen ersetzt, und je weniger Restwasserstoff besitzt, desto weniger saure wird es sein.
Zum Beispiel Phosphorsäure, H3Po4, Bis zu zwei Säuresalze können zu sagen, Natrium. Diese sind: nah2Po4 (N / A+ ersetzt ein Wasserstoff, das zu H entspricht+) und na2HPO4.
Kann Ihnen dienen: Selen: Geschichte, Eigenschaften, Struktur, erhalten, verwendet, verwendetNach der traditionellen Nomenklatur werden diese Salze ebenso genannt wie die Oxisals (völlig ungeschütz. So der NaH2Po4 Es wäre Natriumdease -Phosphat und der Na2HPO4 Natriumsäurephosphat (weil es ein H hat hat.
Andererseits bevorzugt die Aktiennomenklatur das Wort "Wasserstoff", das "Säure". Der Nah2Po4 Es wäre, Natriumdihydrogen und der Na zu sein2HPO4 Wasserstoff -Natriumphosphat. Beachten Sie, dass diese Salze vier Atome haben: Na, H, P und O.
Grundlegende Oxisals
Basisoxisals sind diejenigen, die Anion OH in ihrer Komposition enthalten-. Betrachten Sie zum Beispiel Salzkano3Oh (ca2+ NEIN3- Oh-). Um es zu nennen, würde es ausreichen, dem Namen des Metalls das Wort "grundlegend" zu geben. Sein Name wäre also: Basic Calciumnitrat. Und wie wäre es mit Cuio3Oh? Sein Name wäre: CUPRIC BASIC YODATO (CU2+ Io3- Oh-).
Nach der Aktiennomenklatur wird das Wort "Basic" durch Hydroxid ersetzt, gefolgt von der Verwendung eines Skripts vor dem Namen des Oxoanion.
Wiederholung der vorherigen Beispiele, ihre Namen würden für jedes: Calciumhydroxid-Nitrat und Kupferhydroxid-Andodat (II); Denken Sie daran, dass die Metallvalencia in Klammern und mit römischen Zahlen angegeben werden muss.
Doppelsalze
In Doppelsalzen interagieren zwei verschiedene Kationen mit derselben Art von Anion,. Angenommen das Doppelsalz: Cu3Glaube (po4)3 (Cu2+ Glaube3+ Po43-). Es ist ein Eisen- und Kupferphosphat, aber der am besten geeignete Name, der sich darauf bezieht.
Hydratisierte Salze
Dies sind Hydrate, und der einzige Unterschied besteht darin, dass am Ende ihrer Namen die Anzahl der Wasserformulate angegeben ist. Zum Beispiel die MNCL2 Es ist Manganchlorid (ii).
Kann Ihnen dienen: Benzoine: Struktur, Eigenschaften, Verwendungen und RisikenSein Hydrat, Mncl2· 4h2O Es heißt Manganchlorid (ii) Tetrahydrat. Beachten Sie, dass es vier verschiedene Atome gibt: Mn, Cl, H und O.
Ein berühmtes doppeltes und hydratisiertes Salz ist Mohrs Faith (NH4)2(SW4)2· 6h2ENTWEDER. Sein Name ist: Doppel -Eisensulfat (II) und Hexahydrat Ammonium.
Ausbildung
Wir konzentrieren uns wieder auf anorganische quaternäre Verbindungen und haben hauptsächlich ein Produkt von partiellen Neutralisationen. Wenn diese in Gegenwart mehrerer Metalloxide auftreten, sind doppelte Salze wahrscheinlich; Und wenn das Medium sehr grundlegend ist, fällen die Grundoxisals aus.
Und wenn auch auch, dass Wassermoleküle eine Affinität zu Metall haben, koordinieren sie direkt mit ihm oder mit den umgebenden Ionen und bilden die Hydrate.
Auf der Seite der Legierungen müssen vier verschiedene Metalle oder Metalloide für die Herstellung von Kondensatoren, Halbleitern oder Transistoren geschweißt werden.
Beispiele
Schließlich ist unten eine Liste mit verschiedenen Beispielen für quaternäre Verbindungen aufgeführt. Der Leser kann es verwenden, um sein Wissen über die Nomenklatur zu testen:
- PBCO3(OH)2
- CR (HSO4)3
- Nahco3
- Znioh
- Cu2(OH)2SW3
- Li2Kaso4
- Cuso4· 5h2ENTWEDER
- Agau (so4)2
- Fall4· 2H2ENTWEDER
- Fecl3· 6h2ENTWEDER
Verweise
- Shiver & Atkins. (2008). Anorganische Chemie. (Vierte Edition). Mc Graw Hill.
- Whitten, Davis, Peck & Stanley. (2008). Chemie. (8. Aufl.). Cengage Lernen.
- Anorganische Nomenklatur und Formulierung. [PDF]. Abgerufen aus: Ressourcen.Ausbildung.Ist
- Erika Thalîa gut. (2019). Doppelsalze. Akademie. Erholt von: Akademie.Edu
- Wikipedia. (2019). Quartäres Ammoniumkation. Abgerufen von: in.Wikipedia.Org

