Organische Verbindungen

- 3488
- 834
- Ivan Pressler
Wir erklären, was organische Verbindungen sind, welche Eigenschaften, die Typen, die Unterschiede zu den anorganischen Verbindungen und geben mehrere Beispiele an
 Organische Verbindungen stammen aus Lebewesen
Organische Verbindungen stammen aus Lebewesen Was sind organische Verbindungen?
Der Organische Verbindungen Sie sind solche, die aus Lebewesen stammen und Kohlenstoff- und Wasserstoffatome enthalten, die in Form von offenen Ketten oder geschlossenen Zyklen miteinander verbunden sind.
Zusätzlich zu Kohlenstoff und Wasserstoff können organische Verbindungen auch andere Elemente wie Sauerstoff (O), Stickstoff (N), Schwefel (S), Phosphor (P), Fluor (F), Chlor (CL), Brom (BR) enthalten. oder Jod (ich). Alle diese werden als Heteroátomos bezeichnet.
Ohne organische Verbindungen wäre das Leben nicht möglich, daher enthalten alle Lebewesen sie. Es gibt Tausende dieser Substanzen und wir können sie überall finden, angefangen mit unseren eigenen Körpern.
Eigenschaften organischer Verbindungen
Sie basieren auf der Kohlenstoffchemie
Kohlenstoff bildet die Grundlage aller organischen Verbindungen. In diesen Verbindungen können Kohlenstoffatome miteinander oder mit anderen Elementen verbunden werden. Jedes Kohlenstoffatom bildet immer insgesamt 4 Bindungen zwischen einfachen, doppelten und dreifachen Bindungen.
Sie haben kovalente Links
Es gibt drei Arten von chemischen Hauptverbindungen, die die kovalente, ionische und metallische Bindung sind. Organische Verbindungen sind durch Besitz von nur kovalenten Bindungen zwischen all ihren Atomen gekennzeichnet.
Sie sind Kraftstoffe
 Kohlenstoff ist ein Brennstoff, der aus den im Holz vorhandenen organischen Verbindungen erhalten wird
Kohlenstoff ist ein Brennstoff, der aus den im Holz vorhandenen organischen Verbindungen erhalten wird Durch so viele Kohlenstoffatome sind organische Verbindungen brennbar. Dies bedeutet, dass sie durch eine Verbrennungsreaktion mit dem Sauerstoff der Luft brennen können.
Die Verbrennungsreaktionen organischer Verbindungen sind exotherme Reaktionen, die sehr Wärme freisetzen. Alle Lebewesen nutzen all diese Energie, um alle Reaktionen durchzuführen, die uns am Leben erhalten.
Sie haben Isomeria
Viele organische Verbindungen haben die gleiche molekulare Formel, aber sie sind völlig unterschiedliche Verbindungen. Diese Eigenschaft heißt iomeía und ist charakteristisch für organische Verbindungen.
Zum Beispiel haben beide metilische Ethanolethanol die molekulare Formel C2H6Oder, aber das erste ist ein Gas, während die zweite eine Flüssigkeit ist.
Sie können Polymere bilden
Ein weiteres Merkmal von organischen Verbindungen ist, dass sie gigantische Moleküle bilden können, die eine Gruppe von Atomen wieder in einer langen Kette wiederholen können. Diese Verbindungen werden als Polymere bezeichnet und ein typisches Beispiel dafür sind Kunststoffe.
Löslichkeit
Eine andere Eigenschaft, die organische Verbindungen charakterisiert, ist ihre Löslichkeit. Viele von ihnen, insbesondere polare organische Verbindungen, sind in Wasser löslich. Andere Verbindungen lösen sich nicht in Wasser auf, sondern in organischen Lösungsmitteln wie Cyclohexan.
Kann Ihnen dienen: Succinsäure: Struktur, Eigenschaften, erhalten, verwendet, verwendetArten von organischen Verbindungen
Organische Verbindungen haben Eigenschaften und Eigenschaften, die sie sehr von anorganischen Verbindungen unterscheiden (solche, die nicht von Lebewesen wie Mineralien stammen).
Viele dieser Eigenschaften ermöglichen es ihnen, sie auf unterschiedliche Weise zu klassifizieren, was zu verschiedenen Arten von organischen Verbindungen führt. Die wichtigsten Klassifizierungskriterien sind:
- Nach seiner Herkunft.
- Nach seiner Struktur und Komposition.
- Gemäß der funktionalen Gruppe.
- Nach seiner Polarität.
Als nächstes werden die nach jeder dieser Kriterien klassifizierten organischen Verbindungen beschrieben:
Arten von organischen Verbindungen nach ihrem Ursprung
Wenn sie aus kommen, können organische Verbindungen sein:
- Natürliche organische Verbindungen: Sie sind diejenigen, die in der Natur gefunden werden und die direkt von Lebewesen kommen. Cellulose ist ein gutes Beispiel, da sie die am häufigsten vorkommende natürliche organische Verbindung der Erde ist.
- Synthetische organische Verbindungen: Sie beziehen sich auf jene organischen Verbindungen, die von Chemikalien in einem Labor oder in einer chemischen Anlage synthetisiert werden. Alle Kunststoffe, die wir täglich verwenden, sind synthetisch und auch viele Medikamente.
Arten von organischen Verbindungen gemäß ihrer Struktur und Zusammensetzung
Nach den Atomen, die sie umfassen, und der Art und Weise, wie diese Atome zusammen vereint sind, können organische Verbindungen:
- Aliphatische Kohlenwasserstoffe: Nur durch Kohlenstoff und Wasserstoff gebildet und dort, wo Kohlenstoffe offene Ketten bilden, entweder linear oder verzweigt. Dazu gehören Alquenos und Alkines.
- Aromatische Kohlenwasserstoffe: Die Verbindungen, die zu dieser Familie gehören, auch Sands genannt, enthalten ungesättigte Zyklen (die noch mehr Wasserstoff haben können), die eine große molekulare Stabilität aufweisen. Diese Eigenschaft wird als Aromatizität bezeichnet und ist charakteristisch für Benzol und alle seine Derivate.
- Heterocyclische Verbindungen: Es sind zyklische Verbindungen, bei denen ein oder mehrere Kohlenstoffatome durch ein Heteroátomo ersetzt werden, der Sauerstoff, Stickstoff, Schwefel oder Phosphor sein kann. Beispiele für Heterocyclen sind Pyridin und Furano.
- Organometallische Verbindungen: Sie sind eine besondere Klasse von Verbindungen, die auf halbem Weg zwischen organisch und anorganisch sind. Sie sind durch einen organischen Teil mit einem Heteroátom gekennzeichnet.
Arten von organischen Verbindungen gemäß der funktionellen Gruppe
Der Teil eines organischen Moleküls, in dem chemische Reaktionen normalerweise auftreten. Es gibt verschiedene funktionale Gruppen, die es ermöglichen, organische Verbindungen in:
- Schließt: Sie enthalten nur Kohlenstoff und Wasserstoff, die nur durch einfache Bindungen verbunden sind. Zum Beispiel Butan.
- Alkene: Es sind Kohlenwasserstoffe, die eine Doppelkohlenstoffbindung enthalten. Zum Beispiel das Buutene.
- Alkine: Es sind Kohlenwasserstoffe, die eine dreifache Kohlenstoffkohlenstoffbindung enthalten. Zum Beispiel Etino, auch als Acetylen bekannt.
- Alkyl -Halogenuros: Organische Verbindungen, die einen Halogen (F, Cl, Br oder I) enthalten, der mit einem aliphatischen Kohlenstoff verbunden ist. Zum Beispiel Chlormethan.
- Alkohole: Alkohole sind polare organische Verbindungen, die eine Hydroxylgruppe (-OH) zusammen mit einem aliphatischen Kohlenstoff enthalten.
- Phenole: Diese Verbindungen enthalten auch eine Hydroxylgruppe (-OH), in diesem Fall zusammen mit einem aromatischen Kohlenstoff.
- Ethers: Sie sind leicht zu erkennen, da es sich um zwei Kohlenstoffeketten zusammen miteinander durch ein Sauerstoffatom. Zum Beispiel der Methylether.
- Amine: Es sind organische Verbindungen, die aus Ammoniak (NH3). Sie enthalten eine oder mehrere aliphatische Kohlenstoffe (Alkylgruppen), die durch einfache Bindungen mit einem Stickstoffatom verbunden sind.
- Aldehyde: Sauerstoffhaltige organische Verbindungen, die eine Carbonylgruppe (C = O) zusammen mit einem Wasserstoff in einem seiner terminalen Kohlenstoffe enthalten. Im Allgemeinen haben sie charakteristische Gerüche wie das Cinamaldehyd, das den Geruch von Zimt verleiht.
- Ketone: Es handelt sich um sauerstoffhaltige organische Verbindungen, die eine Carbonylgruppe (C = O) zusammen mit zwei Kohlenstoffketten enthalten.
- Carbonsäuren: Auch als organische Säuren bezeichnet, sind schwache Säuren, die eine Carboxylgruppe (-COOH) in einem ihrer terminalen Kohlenstoffe enthalten.
- Ester: Sie stammen aus der Vereinigung einer Carboxylsäure mit einem Alkohol. In diesem Fall wird der Wasserstoff der Carboxylgruppe durch eine Mietgruppe ersetzt.
- Inmitten: Sie stammen aus der Vereinigung einer Carbonsäure mit einem Amin. In diesem Fall wird die OH der Carboxylgruppe durch einen Stickstoff ersetzt, der an zwei Wasserstoffen, einem Wasserstoff und einem Alkyl oder zwei Alkals, angebracht ist.
Arten von organischen Verbindungen gemäß ihrer Polarität
Wir können auch organische Verbindungen in Polar und Apolar klassifizieren:
- Polare organische Verbindungen: Diese Verbindungen haben polare kovalente Bindungen mit Atomen wie Stickstoff und Sauerstoff, die das gesamte Molekül polar machen. Die meisten dieser Verbindungen sind in Wasser löslich.
- Apolare organische Verbindungen: Sie sind diejenigen, die keine polaren Links haben, oder die Polaritäten ihrer Links werden miteinander abgesagt. Diese Verbindungen sind in Wasser nicht löslich.
Unterschiede zwischen organischen Verbindungen und anorganischen Verbindungen
Die folgende Tabelle fasst die Unterschiede zwischen organischen und anorganischen Verbindungen zusammen:
Organische Verbindungen | Anorganische Verbindungen | |
Herkunft: | Kommen aus Lebewesen oder ihren Überresten. | Sie kommen nicht aus Lebewesen. |
Komposition: | Fast ausschließlich von C, N, O, S, P, F, Cl, Br und I gebildet. | Sie können durch ein beliebiges Element der Periodenzüchttabelle gebildet werden. |
Arten von Links: | Sie bilden kovalente Bindungen sowohl polar als auch apolar. | Sie können alle Arten von chemischen Verbindungen bilden, einschließlich polarer, apolarer, ionischer oder metallischer kovalenter Bindungen. |
Isomery: | Die meisten präsentieren iomeía. | Nur einige vorhandene iomeía. |
Kraftstoffe: | Sie sind Kraftstoffe. | Die meisten sind nicht brennbar. |
Beispiele für organische Verbindungen
1. Methan (Ch4)
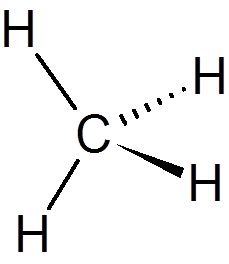
2. Ethylacetat (C4H8ENTWEDER2)
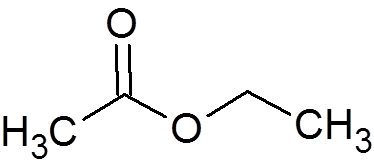
3. Benzol (c6H6)
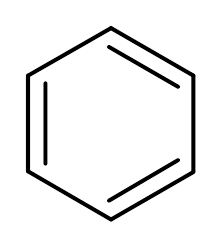
4. Ethylalkohol (C2H6ENTWEDER)
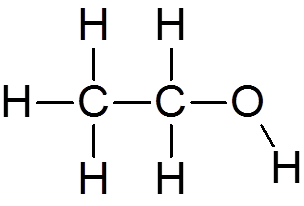
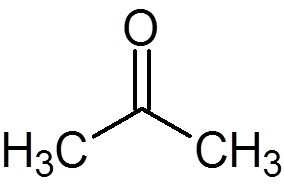
5. Aceton (c3H6ENTWEDER)
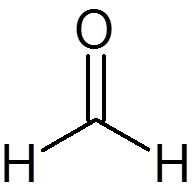
6. Formaldehyd (Ch2ENTWEDER)
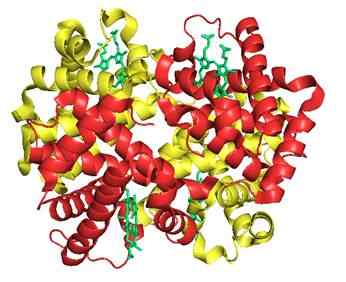
7. Hämoglobin (ein Protein)
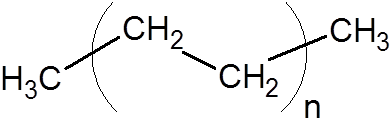
8. Polyethylen (eine der häufigsten Kunststoffe)
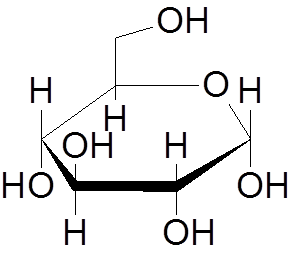
9. Glukose (c6H12ENTWEDER6)
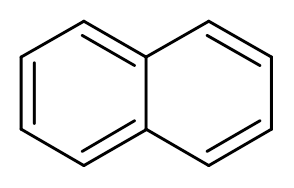
10. Naphthalin (c10H8)
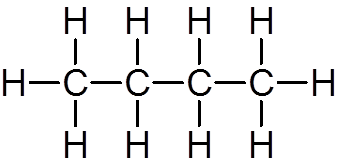
elf. Butano (c4H10)
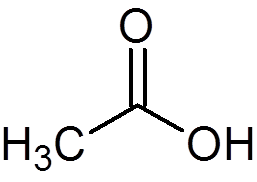
12. Essigsäure oder Essig (C. C2H4ENTWEDER2)
13. Neopentano (c5H12)
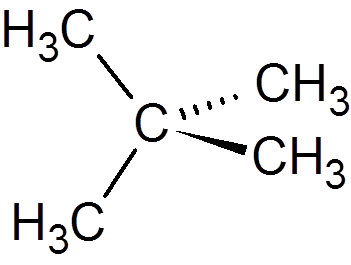
14. Cyclohexan (c6H12)
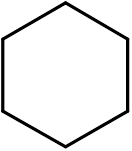
fünfzehn. Pyridin (c5H5N)
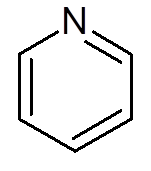
16. Guanina (c5H5N5ENTWEDER)
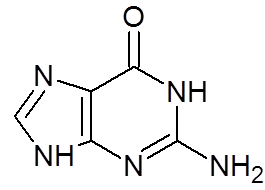
17. Fructose (c6H12ENTWEDER6)
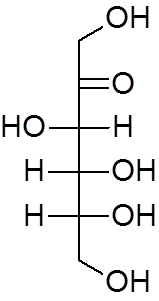
18. Ethylether (c4H10ENTWEDER)
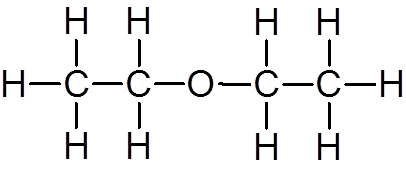
19. Methanol (Ch4ENTWEDER)
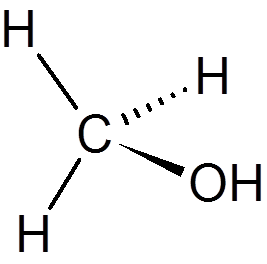
zwanzig. Chloroform (Chcl3)
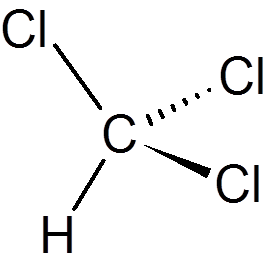
einundzwanzig. Phenol (c6H6ENTWEDER)
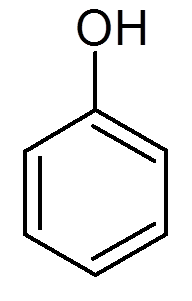
22. Acetylen (c2H2)
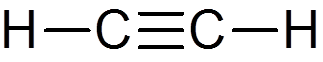
23. Tifenylphosphin ((C)6H6)3P)
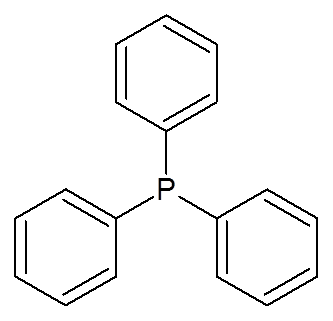
24. Trans-Buteodiosäure (C4H4ENTWEDER4)
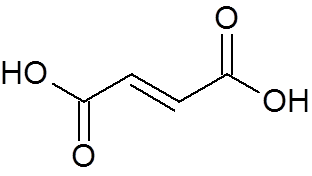
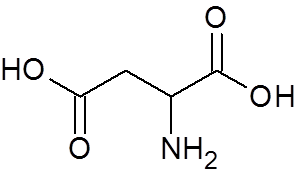
25. Asparaginsäure (eine Aminosäure) (C. C4H7NEIN4)
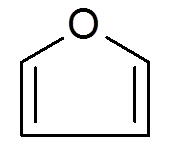
26. Furano (c4H4ENTWEDER)
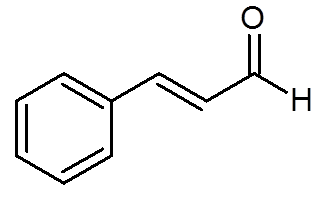
27. Cinamaldehyd (Aroma von Zimt) (C. C9H8ENTWEDER)
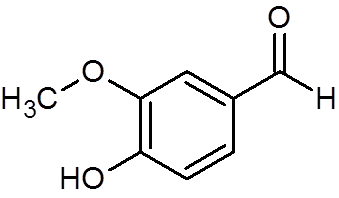
28. Vaniline (c8H8ENTWEDER3)
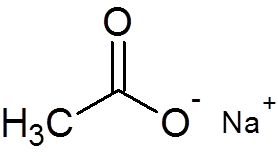
29. Natriumacetat (C2H3ENTWEDER2N / A)
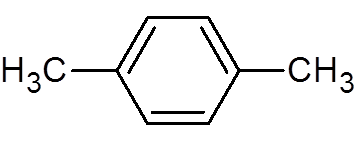
30. P-Xylol (c8H10)
Verweise
- Carey, f., & Giuliano, r. (2013). Organische Chemie, 9. Ausgabe (9. Aufl.). New York City, New York: McGraw-Hill-Ausbildung.
- Schloss a., M. G. (S.F.). Hauptklassen von organischen Verbindungen und funktionellen Gruppen. Aus VAEH geborgen.Edu.mx
- Chang, R., & Goldsby, K. ZU. (2012). Chemie, 11. Ausgabe (11. Ausgabe.). New York City, New York: McGraw-Hill-Ausbildung.
- Klein, d. R. (2011). Organische Chemie (1.Zu ed.). Hoboken, New Jersey: Wiley.
- Morrison, r. T., & Boyd, r. N. (2003). Organische Chemie (6. Aufl.). Boston, Massachusets: Allyn & Bacon.

