Konstanten von Antoine -Formeln, Gleichungen, Beispielen
- 4687
- 1085
- Rieke Scheer
Der Konstanten von Antoine Es gibt drei Parameter, die in einer empirischen Beziehung zwischen Sättigungsdampfdruck und Temperatur für reine Substanzen auftreten. Sie hängen von jeder Substanz ab und sollen in einem bestimmten Temperaturbereich konstant sein.
Aus diesem Bereich verändern die Konstanten von Antoine ihren Wert. Die Konstanten werden durch eine Gleichung verwandt, die 1888 vom französischen Ingenieur Louis Charles Antoine (1825-1897) geschaffen wurde.
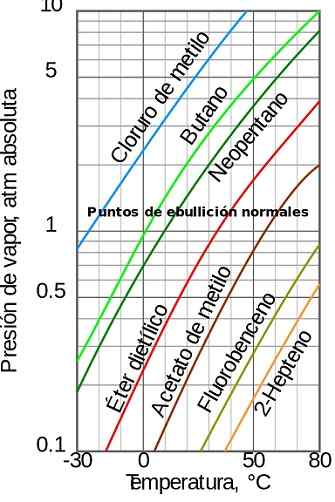
 Abbildung 1. Dampfdruck abhängig von der Temperatur. Quelle: Wikimedia Commons
Abbildung 1. Dampfdruck abhängig von der Temperatur. Quelle: Wikimedia Commons [TOC]
Formeln und Gleichungen
Die üblichste Art, Antoines Funktion auszudrücken, ist:

In dieser Formel P repräsentiert es den Sättigungsdampfdruck, der in Quecksilbermillimetern (mmHg) ausgedrückt wird. T ist die Temperatur, die die unabhängige Variable ist und in ℃ ausgedrückt wird.
A, B und C sind die Konstanten oder Parameter der Antoine -Formel.
Die Bedeutung dieser Formel, die trotz empirisch einen einfachen analytischen Ausdruck liefert, der bei thermodynamischen Berechnungen leicht verwendet werden kann.
Die Formel von Antoine ist nicht einzigartig, es gibt genauere Ausdrücke, die Erweiterungen dieser Formel sind, aber mit dem Nachteil, der sechs oder mehr Parameter aufweist, und deren mathematischer Ausdruck ist komplexer, was sie zu sehr praktizieren, die in den thermodynamischen Berechnungen verwendet werden können.
Sättigungsdampf
Da die Formel von Antoines Sättigungsdampfdruck misst, ist es notwendig, zu erklären, woraus sie besteht.
In einem Glasampulle oder einem anderen Behälter wird eine Flüssigkeit platziert. Alle Luftluft wird extrahiert. Das Set wird in ein Wärmebad gelegt, bis das Gleichgewicht erreicht ist.
Am Anfang ist alles flüssig, aber weil es ein Vakuum gibt, beginnen die schnellsten Moleküle, die Flüssigkeit aufzugeben, die ein Gas aus derselben Substanz der Flüssigkeit bildet.
Kann Ihnen dienen: gleichmäßige geradlinige Bewegung: Eigenschaften, Formeln, ÜbungenDer vorherige Prozess ist der Verdunstung Und mit zunehmender Dampfdruck.
Einige der Dampfmoleküle verlieren Energie und kehren in die flüssige Phase der Substanz zurück. Dies ist der Prozess von Kondensation.
Dann treten zwei Prozesse, Verdunstung und Kondensation gleichzeitig auf. Wenn die gleiche Anzahl von flüssigen Molekülen, die darin eingebaut sind, herauskommen, a dynamisches Gleichgewicht Und zu diesem Zeitpunkt tritt der maximale Dampfdruck auf, der als Sättigungsdruck bekannt ist.
Es ist dieser Dampfsättigungsdruck, der die Antoine -Formel für jede Substanz und jede Temperatur vorhersagt.
Bei einigen Feststoffen gibt es ein ähnliches Phänomen, wenn es direkt von der festen Phase bis zur Soda übergeht, ohne die flüssige Phase zu durchlaufen. In diesen Fällen kann auch ein Sättigungsdampfdruck gemessen werden.
Es ist nicht einfach, ein theoretisches Modell zu etablieren, das von frühen Prinzipien beginnt. Aus diesem Grund werden in der Praxis empirische Formeln verwendet.
Wie ist die Konstante von Antoine??
Es gibt keine theoretische Methode, um die Konstanten von Antoine zu erhalten, da es sich um eine empirische Beziehung handelt.
Sie werden aus den experimentellen Daten jeder Substanz erhalten und die drei Parameter A, B und C angepasst.
Für den Endbenutzer, der im Allgemeinen Chemieingenieure sind, gibt es Tabellen in den Chemiehandbüchern, in denen diese Konstanten für jede Substanz angegeben sind, die die maximalen und minimalen Temperaturbereiche anzeigen, in denen sie anwendbar sind.
Kann Ihnen dienen: Widerstandsthermometer: Eigenschaften, Betrieb, verwendetOnline -Dienste sind auch verfügbar, die die Werte der Konstanten A, B und C wie bei DDBST -GmbH -Onlines -Diensten angeben.
Bei derselben Substanz kann es mehr als einen Validitätstemperaturen geben. Abhängig vom Arbeitsbereich wird die eine oder andere Gruppe von Konstanten ausgewählt.
Die Schwierigkeiten können auftreten, wenn der Temperaturarbeitsbereich zwischen zwei Validitätsbereichen der Konstanten liegt, da die Formeldruckvorhersagen in der Grenzzone nicht übereinstimmen.
Beispiele
Beispiel 1
Finden Sie den Wasserdampfdruck bei 25 ℃.
Lösung
Wir haben die Tabellen konsultiert, um die Konstanten von Antoine zu bestimmen.
Es gibt zwei Wasserbereiche:
Zwischen 1 ℃ und 100 ℃ und zwischen 99 ℃ bis 374 ℃.
Da wir uns für 25 ℃ interessieren, nehmen wir den ersten Bereich, in dem der Wert von Antoines Konstanten liegt:
A = 8,07131
B = 1730.63
C = 233,426
P = 10^(8,07131 - 1730,63/(25 + 233,426))
Berechnung des Exponenten
Berechnen wir zuerst den Exponenten: 1.374499
P = 10^1,374499 = 23.686 mmHg = 0,031166 atm
Ergebnisanalyse
Diese Ergebnisse werden wie folgt interpretiert:
Angenommen, reines Wasser wird in einen hermetischen Behälter gelegt, zu dem die Luft von einer Vakuumpumpe extrahiert wurde.
Der Behälter mit Wasser wird in einem Wärmebad bei einer Temperatur von 25 ° C gelegt, bis das thermische Gleichgewicht erreicht.
Wasser im hermetischen Behälter verdampft teilweise, bis der Sättigungsdampfdruck erreicht ist. Dies ist nichts anderes als der Druck, bei dem der dynamische Gleichgewicht zwischen der flüssigen Phase des Wassers und der Dampfphase festgelegt wird.
Kann Ihnen dienen: Dirac Jordan Atomic Model: Merkmale und PostulateDieser Druck in diesem Fall ergab sich bei 25 ℃ 0,031166 atm.
Beispiel 2
Finden Sie den Wasserdampfdruck bei 100 ℃.
Lösung
Wir haben die Tabellen konsultiert, um die Konstanten von Antoine zu bestimmen. Es gibt zwei Wasserbereiche:
Zwischen 1 ℃ und 100 ℃ und zwischen 99 ℃ bis 374 ℃.
In diesem Fall liegt die Interessenstemperatur in den beiden Bereichen.
Wir verwenden den ersten Bereich [1 ℃, 100 ℃]
A = 8,07131
B = 1730.63
C = 233,426
P = 10^(8,07131 - 1730,63/(100 + 233,426))
Berechnung des Exponenten
Berechnen wir zuerst den Exponenten: 2.8808
P = 10^1,374499 = 760,09 mmHg = 1.0001 atm
Als nächstes verwenden wir den zweiten der Bereiche [99 ℃, 374 ℃]
In diesem Fall sind die Konstanten
A = 8.14019
B = 1810.94
C = 244.485
P = 10^(8.14019 - 1810.94/(100 + 244.485))
Berechnen wir zuerst den Exponenten: 2.88324
P = 10^2.88324 = 764.2602 mmHg = 1.0056 atm
Es gibt einen prozentualen Unterschied zwischen den beiden Ergebnissen von 0,55%.
Verweise
- Anwendung der Gesetze von Raoult und Dalton und der Antoine -Gleichung. Abgerufen von: meinen eigenen und alten.WordPress.com
- Online -Taschenrechner der Antoine -Formel. Erholt von: ddbonline.DDBST.von/antoinecalcion/antoinecalculaticgi.exe
- Gecousb. Thermodynamik und Dampftische / Konstante von Antoine. Erholt von: Gecousb.com.gehen
- Wärmeeigenschaften der Materie. Wiederhergestellt von: Webserver.DMT.Upm.Ist
- Gier und Yang. Antoine konstante Tabellen für mehr als 700 organische Verbindungen. Wiederhergestellt von: Benutzer.Eng.Umd.Edu
- Wikipedia. Antoine -Gleichung. Von Wikipedia geborgen.com
- Wikipedia. Clausius-Clapeyron-Gleichung. Von Wikipedia geborgen.com
- Wisniak J. Historische Entwicklung der Dampfdruckgleichung aus Dalton Toy Antoine. Erholt von: Link.Springer.com
- « Berechnung der relativen Dichte, Beispiele, Übungen
- Moody -Diagrammgleichungen, wofür es, Anwendungen »

