Was ist das elektronegativste Element und warum?
- 2521
- 507
- Ibrahim Steuk
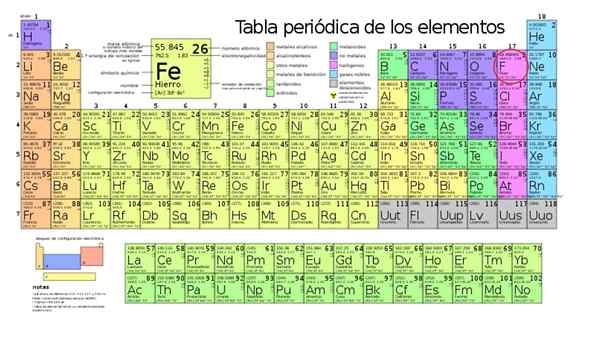
 Das elektronegativste Element ist Fluorid (F), der im roten Kreis gesperrt ist
Das elektronegativste Element ist Fluorid (F), der im roten Kreis gesperrt ist Er Mehr elektronegatives Element In der Periodenzüchter ist es das Fluor, deren Chemikalie f ist und zur Halogengruppe gehört. Unter allen Elementen des Periodensystems ist Fluorid am besten, Elektronen aus anderen Atomen zu fangen.
Dieses Element, das bei Raumtemperatur gasförmig ist, ist hochreaktiv und es ist daher nicht leicht, es in einem reinen Zustand in der Natur zu finden. Fluor verbindet sich leicht mit anderen Elementen wie Schwefel, Calcium und Metallen sowie zahlreichen Verbindungen, insbesondere solchen, die Wasserstoff enthalten.
Mit seiner hohen Elektronegativität können Sie sogar mit edlen Gasen wie Xenon, Kripton und Radon kombinieren.
Nach Fluor ist Sauerstoff das zweite Element mit der höchsten Elektronegativität. Im Gegensatz dazu sind die Elemente mit der niedrigsten Elektronegativität Francio (FR) und Cäsium (CS).
 Da es das elektronegativste Element ist, bildet Fluor zahlreiche Verbindungen wie Fluorit oder Calciumfluorid. Quelle: Wikimedia Commons
Da es das elektronegativste Element ist, bildet Fluor zahlreiche Verbindungen wie Fluorit oder Calciumfluorid. Quelle: Wikimedia Commons Dies sind daher die meisten elektropositiv Das existiert, obwohl Francio radioaktiv und sehr wenig reichlich vorhanden ist.
Elektronegativität und Periodenzüchter
Das Ausmaß der Elektronegativität wurde vom Chemiker und Preis der Nobel Linus Pauling (1901-1994) entwickelt, obwohl das Konzept auf den schwedischen Chemiker Jöns Jakob Berzelius (1779-1848) zurückzuführen ist.
Die Paulingskala, die der Elektronegativität dimensionale numerische Werte zuweist.
Jedes Element hat seine eigene Elektronegativität, die von seinen atomaren Eigenschaften abhängt. Es wird experimentell und indirekt ermittelt, beispielsweise die Messung der Verbindungsenergie, wie es Pauling um 1932 getan hat.
Auf der Skala Pauling Electronegativitäten ist Fluorid zuerst mit einem ungefähren Wert von 3.98 ≈ 4.0.
Kann Ihnen dienen: Aliphatische Kohlenwasserstoffe: Eigenschaften, Nomenklatur, Reaktionen, TypenElektronegativität ist eine regelmäßige Eigenschaft der Elemente. In den meisten Fällen (es gibt einige Ausnahmen) wird festgestellt.
Und erhöhen Sie sich auch von unten nach oben, indem Sie sich auf einer Spalte bewegen.
 Die Periodenschaftstabelle der Elektronegativitäten gemäß der Paulingskala. Fluor ist das elektronegativste Element, das sich oben und rechts befindet, während Francio das am wenigsten elektronegativ für alle oder das elektropositive, falls bevorzugt ist und sich in der linken und unten -Säule befindet. Quelle: f. Zapata.
Die Periodenschaftstabelle der Elektronegativitäten gemäß der Paulingskala. Fluor ist das elektronegativste Element, das sich oben und rechts befindet, während Francio das am wenigsten elektronegativ für alle oder das elektropositive, falls bevorzugt ist und sich in der linken und unten -Säule befindet. Quelle: f. Zapata. Fluorelektronegativität
Der Grund dafür, dass Fluor das elektronegativste Element in der Periodenplatte ist, liegt auf der elektronischen Konfiguration (die Art und Weise, wie seine Elektronen in Orbitalen um den Kern angeordnet sind).
Diese Konfiguration ist 1s22s22 p5, Fluorid hat also 5 Elektronen in seiner äußersten Schicht.
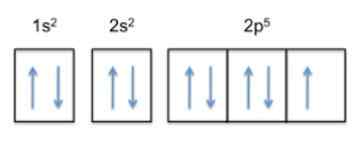
Da der Trend des Atoms darin besteht, seine äußere Schicht zu vervollständigen , deren elektronische Konfiguration 1s beträgt22s22 p6.
Das Fluoratom hat einen sehr geringen Radius, da die Protonen in ihrem Kern Elektronen sehr stark anziehen und sie näher halten als in den Atomen weniger elektronegativer Elemente wie Cesium und Francio.
Daher sind letztere bereit, Elektronen leicht aufzugeben, um Verbindungen zu bilden.
Verweise
- Aguilar, c. Leitfaden für die chemische Lerneinheit I. Abgerufen von: IPN.mx.
- Atkins, p. (2005). Prinzipien der Chemie, die Wege der Entdeckung. 3. Auflage. Pan -American Medical Editorial.
- Clark, j. Elektronegivität. Erholt von: Chem.Librettexts.Org.
- Hein, m. (2014). Grundlagen der College -Chemie. 14. ed. Wiley.
- Lentech. Chemische Elemente, die durch seine Elektronegativität geordnet sind. Erholt von: lentech.Ist.

