Elektrodialyse Wie funktioniert, Vor-, Nachteile, Verwendungsmöglichkeiten
- 1424
- 361
- Tizian Liebich
Der Elektrodialyse Es ist die Ionenbewegung durch eine semipermeable Membran, die von einer elektrischen Potentialdifferenz angetrieben wird. Die in der Elektrodialyse verwendeten Membranen haben die Eigenschaft, Ionenaustauscher für Kationen oder für Anionen zu sein.
Kationenaustauschmembranen haben negative Belastungen: Sie lassen Kationen die Anionen passieren und abstoßen. In der Zwischenzeit haben anionische Austauschmembranen eine positive Ladung: Sie lassen die Anionen und Ablehnung Kationen.
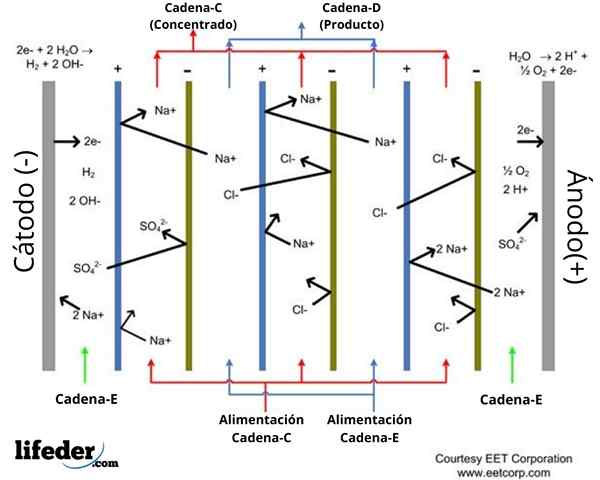
 Schema einer Packung von fünf Elektrodialysezellen. Quelle: CommonShelper2 über Wikipedia.
Schema einer Packung von fünf Elektrodialysezellen. Quelle: CommonShelper2 über Wikipedia. Elektrodialysekameras oder Zellen sind in Paketen mit mehreren Anionen- und kationischen Austauschmembranen organisiert, die sich miteinander abwechseln. Anionische und kationische Austauschmembranen begrenzen die Räume, in denen die Verdünnungs- und Konzentrationsprozesse von Flüssigkeiten durchgeführt werden.
Die treibende Kraft der ionischen Flüsse, die die Membranen von Elektrodialysezellen überschreitet.
In der Umkehrosmose ist der Wasserfluss aus dem Kompartiment mit der größten Osmolarität zum unteren Osmolaritätskompartiment auf eine Erhöhung des hydrostatischen Drucks zurückzuführen, der durch die Wirkung einer Pumpe verursacht wird.
[TOC]
Wie funktioniert in der Wasserverdünnung?
Beschreibung einer Packung von fünf Elektrodialysezellen
In dem gezeigten Schema (überlegenes Bild) ist die Position von sechs Ionenaustauschmembranen angegeben: drei Kationenaustausch und drei Anionenaustausch, die miteinander durchsetzt sind. Diese Membranen begrenzen fünf Kompartimente, in denen Flüssigkeiten, die an der Elektrodialyse beteiligt sind, zirkulieren (siehe rote und bläuliche Pfeile).
Anionische Austauschmembranen sind positiv beladen und erscheinen im blaugelenkten Schema. Diese ermöglichen die Anionen die Kationen für die elektrostatische Abstoßung.
Die Kationenaustauschmembranen haben zwar eine negative Belastung, was im grünen Schema anzeigt. Sie werden von Kationen gekreuzt, aber die Anionen abwehrt.
Es kann Ihnen dienen: Test: Merkmale, Typen, Beispiele für VerwendungenBeide Arten von Membranen sind wasserdicht für Wasser. Das Schema zeigt zwei Räume, in denen eine Verdünnung des Salzgehalts des Wassers auftritt. Im Schema sind die wässrigen Ein- und Ausstiegsströme dieser Räume blau angezeigt, die als Strom d identifiziert werden d identifiziert werden.
In der Zwischenzeit gibt es drei Räume, in denen Wasser mit einem hohen Salzgehalt zirkuliert und rot identifiziert wird. Einkommens- und Ausstiegsströme zu diesen Kompartimenten werden im Schema als aktuelles C angegeben.
Ebenso sind die Kompartimente von Anode (+) und Kathoden (-) im Schema angegeben, durch das der Strom und der.
Elektrodialyse -Betrieb
Die Kationen werden von der Last der Kathode (-) angezogen, während die Anode (+) abgewehrt wird. Die Anionen werden von der Last der Anode (+) angezogen und durch die Last der Kathode (-) abgewehrt.
Die Beobachtung beispielsweise von Zellen drei, vier und fünf zeigt Folgendes an: In den Zellen drei und fünf zirkuliert konzentrierte Flüssigkeit, während in Zellen vier Flüssigkeit zirkuliert.
Der Ion Cl- von Fach vier wird von der Last der Anode angezogen und überschreitet die anionische Austauschmembran, die sie von Fach fünf trennt.
Inzwischen das Na -Ion+ von Fach fünf wird durch die positive Belastung der Anode abgestoßen, aber nicht in den Fach vier eingeben. Dies liegt daran, dass die Membran, die Kompartimente vier und fünf trennt.
Andererseits die NA+ von Fach vier wird durch die Anode (+) abgestoßen und überquert die Kation-Austauschmembran (-), die sie vom Abteil drei trennt.
Zusammenfassung: Na -Konzentration+ und Cl- Vier Fächer neigen tendenziell ab. Dann verringert sich die Kochsalzstoffkonzentration in Verdünnungskompartimenten und erhöht sich in den Konzentrationskompartimenten.
Es kann Ihnen dienen: Angewandte Chemie: Studienobjekt, Zweige, Wichtigkeit, BeispieleVorteile und Nachteile
Vorteile
-Die Elektrodialyse ist einfach und kontinuierlicher Betrieb.
-Chemische Behandlung ist nicht erforderlich, um Austauschmembranen zu regenerieren.
-Es gibt niedrige Betriebskosten und Wartungskosten, die wenig Platz für den Betrieb erfordern.
Nachteile
-Partikel mit einem Durchmesser von mehr als 1 µm können die Ionenaustauschmembranen durchsetzen.
-Es wird nicht empfohlen, Wasser mit einer Härte von mehr als 1 zu verwenden, da Calciumcarbonat eine Kruste in Konzentratzellen erzeugt.
-Benötigt Kohlendioxid -Eliminierungsbehandlung (CO2), da dies beim Dissoziieren die Wasserleitfähigkeit verändern kann.
Unterschied zwischen Dialyse und Elektrodialyse
Die Dialyse ist Wasserfluss durch eine semipermazierbare Membran des kleineren Osmolaritätskompartiments zum größeren Osmolaritätskompartiment. Das Kompartiment mit weniger osmolarität hat eine größere Konzentration an Wassermolekülen.
Aus diesem Grund fließt Wasser zugunsten seines Konzentrationsgradienten des Kompartiments mit weniger Osmolarität gegen das Kompartiment mit größerer Osmolarität.
Die Elektrodialyse hingegen ist ein Ionenstrom durch eine Ionenaustauschmembran, die je nach elektrischer Ladung zu Ionen übergeht oder nicht. Die treibende Kraft der Ionenbewegung ist ein Unterschied im elektrischen Potential.
Im Gegensatz zur Dialyse gibt es bei der Elektrodialyse keinen Wasserfluss durch Membranen und es gibt nur Ionenfluss.
Elektrodialyseanwendungen
Wasser Demineralisierung
Es gibt Elektrodialyseanlagen, die Wasser mit hohen Salzen verarbeiten, um Trinkwasser zu produzieren. Electrodialyse wird auch verwendet, um Abwasser aus dem Inland und industriellen Gebrauch zu verarbeiten, um sie für den anschließenden Verbrauch geeignet zu machen.
Es kann Ihnen dienen: Erlenmeyer Flask: Eigenschaften, Verwendungsmöglichkeiten, VerwendungsmethodenInsbesondere wird die Elektrodialyse zur Wiederherstellung wertvoller Metalle verwendet, die in den Abwassergewässern der Industrie vorhanden sind. Es wird auch zur Entfernung von Salzen und Säurelösungen und bei der Trennung von ionischen Verbindungen von neutralen Molekülen verwendet.
Nahrungsmittelindustrie
Obwohl die Elektrodialyse in der Pharmaindustrie, in Kosmetik sowie in anderen Branchen verwendet wird, ist der am weitesten verbreitete Einsatz in der Lebensmittelindustrie. Unter allen Ihrer Anwendungen können wir Folgendes erwähnen:
-Smineralisierung von Serum und Melasse
-Weinstabilisierung von Weintartarsäure
-Abnahme der Säure von Fruchtsäften
-Produktion von pflanzlichem Protein isoliert
-Versagen von Serumproteinen
-Demineralisierung von Soja- und Fischölen
-Eliminierung von Rübenalkalischen Ionen und Rohrmelasse
-Behandlung mit Meeresfrüchten
-Demineralisierung von Trauben und Kartoffelsaft
-Konzentration und Wiederherstellung von organischen Säuren
-Soja -Proteinproduktion
-Antioxidansanreicherung
Verweise
- Whitten, Davis, Peck & Stanley. (2008). Chemie. (8. Aufl.). Cengage Lernen.
- Wikipedia. (2020). Elektrodialyse. Abgerufen von: in.Wikipedia.Org
- Lentech b.V. (2020). Was ist EDI? Erholt von: lentech.com
- Mondor m., Ipperiel d., Lamarche f. (2012) Elektrodialyse in der Lebensmittelverarbeitung. In: Boye J., Arcand und. (Hrsg.) Grüne Technologien in der Lebensmittelproduktion und -verarbeitung. Food Engineering -Serie. Springer, Boston, MA. doi.org/10.1007/978-1-4614-1587-9_12
- Akhter M, Habib G, Qamar sein (2018) Anwendung von Elektrodiasis bei der Abwasserbehandlung und Auswirkungen der Verschmutzung auf die Prozessleistung. J Memb Sci Technol 8: 182. Doi: 10.4172/2155-9589.1000182
- H. Strathmann. (6. Dezember 2006). Elektrodiasis und ihre Anwendung in der chemischen Prozessindustrie. Taylor & Francis online. doi.org/10.1080/03602548508068411
- « Dritte Person, die Merkmale und Beispiele entwerfen
- Die 8 Beispiele für relevanteste grafische Ressourcen »

