Enantiomere
- 5824
- 375
- Nick Laurén
Wir erklären, was Enantiomere und Chiralität, ihre Eigenschaften, Nomenklatur und mehrere Beispiele sind
 Diese beiden Verbindungen sind Enantiomere, da sie von denselben Atomen gebildet werden, vereint auf die gleiche Weise und sind spiegelende Bilder voneinander
Diese beiden Verbindungen sind Enantiomere, da sie von denselben Atomen gebildet werden, vereint auf die gleiche Weise und sind spiegelende Bilder voneinander Was sind die Enantiomere??
Der Enantiomere Es sind Paare von Verbindungen, die nicht -überlampbare Spiegelbilder voneinander sind. Diese Verbindungspaare sind eine bestimmte Art von Isomeren, dh sie sind verschiedene Verbindungen, die die gleiche molekulare Formel haben.
Es gibt verschiedene Arten von Isomeren, darunter Stereoisomere, bei denen alle Atome in derselben Reihenfolge und mit derselben Art von Links vereint sind, aber sie haben unterschiedliche Orientierungen im Raum (Stereo bedeutet Raum).
Innerhalb der Stereoisomere finden wir die Enantiomere, deren Hauptmerkmal es ist, Spiegelbilder miteinander zu sein.
Enantiomere sind in der Natur sehr häufig. Tatsächlich gehören fast alle in den Zellen aller Lebewesen vorhandenen organischen Verbindungen eines von zwei möglichen Enantiomeren.
Zum Beispiel entsprechen alle Aminosäuren, die Teil natürlicher Proteine sind.
Andererseits existieren die Wirkstoffe der überwiegenden Mehrheit der Medikamente auch als Paar Enantiomere, von denen nur einer wirksam ist. Die Schwierigkeit bei der Trennung von Enantiomeren voneinander bedeutet, dass jene Medikamente, die nur das nützliche Isomer enthalten.
Enantiomere und Chiralität
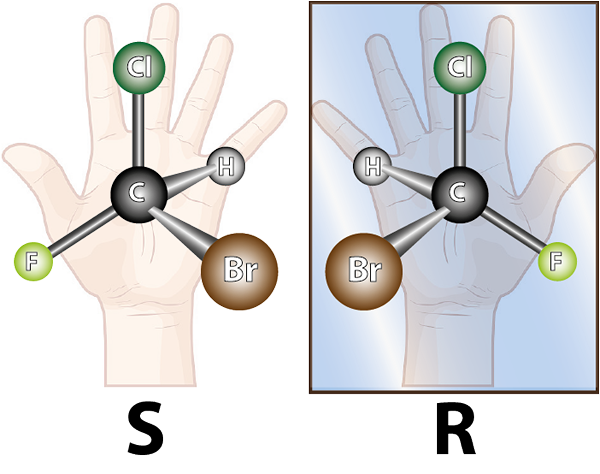
Enantiomere werden durch chirale Moleküle gebildet. Chiralität ist die Eigenschaft, sich nicht mit seinem Spiegelbild zu überlappen. Das Wort Chiral kommt vom griechischen Begriff, Kheir Dies bedeutet Hand, sich an die Tatsache zu erinnern, dass die Hände auch spiegelende Bilder voneinander sind und sich nicht überlappen können.
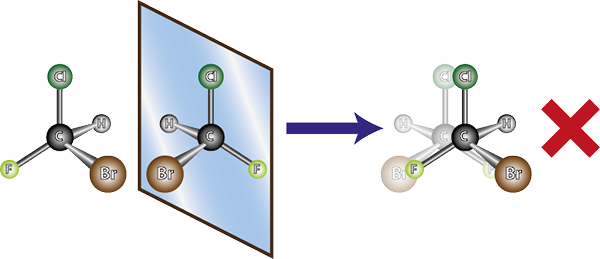 Das Molekül der linken ist chiral, da es beim Vergleich mit seinem Spiegelbild ersichtlich ist, dass sie sich nicht überlappen. Mit anderen Worten, es gibt keine Möglichkeit, es so zu drehen oder zu drehen, dass alle Atome miteinander überfallen
Das Molekül der linken ist chiral, da es beim Vergleich mit seinem Spiegelbild ersichtlich ist, dass sie sich nicht überlappen. Mit anderen Worten, es gibt keine Möglichkeit, es so zu drehen oder zu drehen, dass alle Atome miteinander überfallen In Anbetracht des oben genannten kann abgeleitet werden, dass es für jedes chirale Molekül ein anderes chirales Molekül geben muss. Mit anderen Worten, wann immer ein Molekül gesagt wird.
Kann Ihnen dienen: Neodymium: Struktur, Eigenschaften, verwendetChirale Zentren
Viele chirale Verbindungen haben ein oder mehrere asymmetrische Zentren, die für die Chiralität des Moleküls verantwortlich sind. Diese werden als chirale Zentren bezeichnet und in vielen organischen Verbindungen bestehen aus Kohlenstoffatomen, die mit 4 Atomen oder Gruppen verschiedener Atome verbunden sind.
Die besondere Form, da diese vier Gruppen um asymmetrischen Kohlenstoff verteilt sind, bestimmt, welcher der beiden Enantiomere einem chiralen Molekül entspricht. Das Vorhandensein eines einzelnen quiralen Zentrums stellt sicher, dass das Molekül chiral ist, aber wenn es mehr als einen gibt, kann es chiral sein.
Enontiomer -Eigenschaften
Die meisten physikalischen und chemischen Eigenschaften sind identisch
Wie die rechte Hand und die linke Hand kommen die Enantiomere nur paarweise zu paar. Diese Verbindungen sind praktisch miteinander identisch. Tatsächlich sind die meisten physikalischen und chemischen Eigenschaften wie der Fusionspunkt, Kochen, Dampfdruck und Löslichkeit in einigen Lösungsmitteln identisch.
Optische Aktivität
Alle chiralen Verbindungen haben eine einzigartige Eigenschaft, die sie von denen unterscheidet, die es nicht sind: Sie können die Ebene des polarisierten Lichts drehen. Diese Eigenschaft heißt Optische Aktivität, Und es ist eines der wenigen Eigenschaften, die eine chirale Verbindung von seinem Enantiomer unterscheiden.
Letzteres ist auf die Tatsache zurückzuführen Symbol -).
Wenn eine quirale Verbindung die polarisierte Lichtebene in eine Richtung dreht, dreht ihr Enantiomer sie in die entgegengesetzte Richtung.
-
Beispiel
Eine D-Glucosa-Lösung dreht die polarisierte Lichtebene in Richtung der Taktnadeln (rechts ist es dextrogyral), während eine L-Glycose-Lösung sie in die entgegengesetzte Richtung dreht.
Es kann Ihnen dienen: Erlenmeyer Flask: Eigenschaften, Verwendungsmöglichkeiten, VerwendungsmethodenDifferentialreaktivität
Eine andere Eigenschaft, die es ermöglicht, eine Enantión von der anderen zu unterscheiden, ist seine Reaktivität gegen andere chirale Verbindungen.
Die differentielle Reaktivität kann mit der Art und Weise verglichen werden, wie ein Handschuh für eine Hand nur gut aussieht, aber nicht der anderen oder als rechter Schuh gut zum rechten Fuß passt, aber nicht nach links.
Eine wichtige Folge der unterschiedlichen Reaktivität sind die unterschiedlichen Effekte, die die beiden Enantiomere einiger Medikamente verursachen können. Diese Unterschiede können harmlos sein, aber sie können auch sehr gefährlich sein.
-
Beispiele
- Von den beiden Enantimeren des Aspartams (was ein künstlicher Süßstoff ist) ist einer süß, während der andere keinen Geschmack hat.
- Nur die Enantiomer von Omeprazol sind als Magenschutz wirksam, während der andere keinen Effekt erzeugt.
- D-Penicilamin ist ein Medikament gegen rheumatoide Arthritis, während sein Enantiomer L-Penicilamin ein gefährliches Gift ist.
Differentielle Absorption
Enantiomere unterscheiden sich auch in der Art und Weise, wie sie in Harzen oder Feststoffen absorbiert werden, die auch Chirale sind. Ein Misch.
Nomenklatur von Enantiomeren
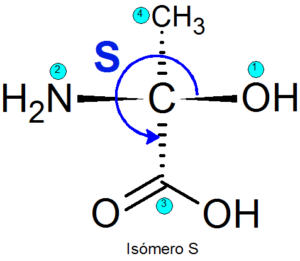
Es gibt verschiedene Methoden, um das eine oder andere Enantiomer zu identifizieren, aber das am häufigsten verwendete CHN-Ingold-Prelog (CIP) -System. Dies besteht aus den folgenden Schritten:
- Eine Hierarchiestufe wird den vier an jedem chiralen Zentrum verbundenen Gruppen zugeordnet. Die Priorität der Gruppen wird gemäß der Atomzahl des Atoms zugewiesen, das direkt mit dem quiralen Zentrum verbunden ist. Wenn es zwei gleiche Atome gibt, werden die Atomnummern der Atome, die mit den ersten verbunden sind, hinzugefügt, um die Atomzahlen hinzuzufügen.
- Die Richtung, in die die drei Prioritätsgruppen befahren sind, wenn die niedrigsten Prioritätspunkte zurück bestimmt werden.
- Wenn sich die Richtung der Route in Richtung der Takthände befindet, ist die Konfiguration zugewiesen R, Andernfalls wird die Konfiguration zugewiesen S.
Beispiel
Beispiele für Enantiomere
D-Glyceraldehyd und L-Glyceraldehyd
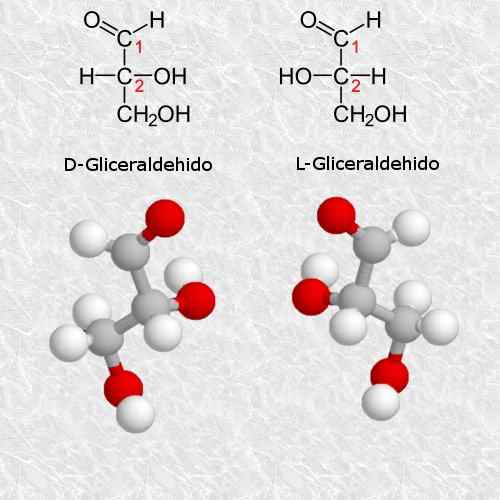
Glyceraldehyd ist der einfachste und kleine quirale Kohlenhydrat, der existiert und für Chemie und Biologie sehr wichtig ist.
Gemäß den Regeln des Cahn-Ingold-Prelog-Systems entspricht das D-Isomer dem Isomer (R) und dem L-Isomer entspricht (s) (s).
D-Alanina und L-Alanina
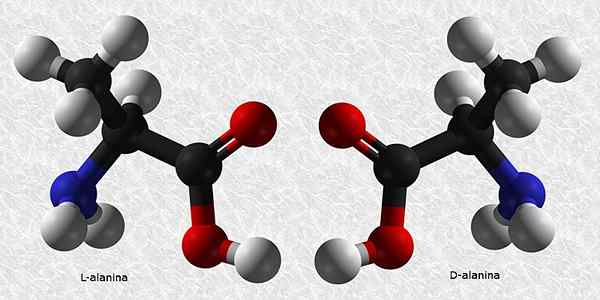
Alanin ist eine der wesentlichen Aminosäuren für den Bau von Proteinen. Wie fast alle Aminosäuren hat es einen chiralen Kohlenstoff, so dass es zwei Enantiomere hat:
Von diesen beiden ist L-Alanina die häufigste und in allen Lebewesen vorhanden, während D-Alanina nur in einigen bakteriellen Zellwänden vorhanden ist.
D-Tartarische und L-Tartarsäure
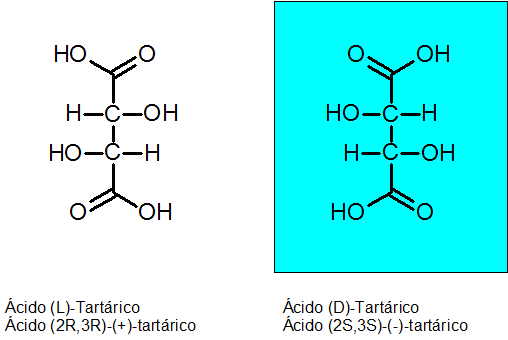
Die Chiralität wurde 1848 von Louis Pasteur dank Tartarsäure entdeckt. Diese Verbindung hat 2 asymmetrische Kohlenstoffe und kann als zwei Enantiomere sowie ein drittes Isomer existieren, das als Meso -Verbindung bezeichnet wird.
Die absolute Konfiguration der beiden chiralen Kohlenstoffe ist R für die Enantiómero Levógiro und S für den Dextrogyan Enantiom.
2-Butanol
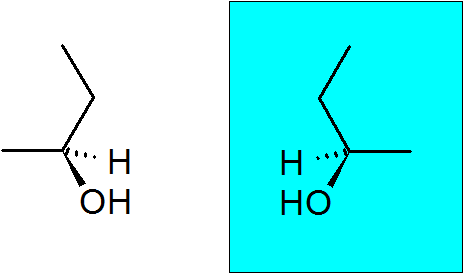
Dieser Alkohol hat auch einen quiralen Kohlenstoff, wodurch diese Verbindung zwei Enantiomere hat.
Bromocloretan
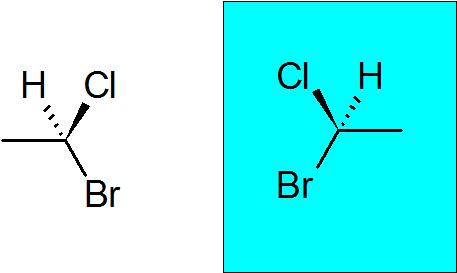
Es ist eine sehr einfache chirale Verbindung mit nur zwei Kohlenstoffen. Quiraler Kohlenstoff hat sich einem Brom, einem Chlor, einem Methyl und einem Wasserstoff angeschlossen.
Verweise
- Chiralität (Chemie). (18. März 2021) auf Wikipedia.com
- Carey, f. ZU. (2008). Organische Chemie. Boston: McGraw-Hill Hochschulbildung.
- Smith, m., März, j., & March, j. (2001). Die fortgeschrittene organische Chemie des März: Reaktionen, Mechanismen und Stadel. New York: Wiley.
- M.H. Hyun (2012). 8.13 Chromatographische Trennungen und Analyse: Chiral Crown Ether-basierte chirale stationäre Phasen. Herausgeber (en): Erick M. Carreira, Hisashi Yamamoto. Chiralität verstehen. Elsevier. Seiten 263-285. ISBN 9780080951683,
- Nguyen, l. ZU., Er, h., & Pham-Huy, C. (2006). Chirale Drogen: Ein Überblick. Internationales Journal of Biomedical Science: IJBS, 2(2), 85-100.

