Glycosidischer Link Was ist Merkmale, Typen, Nomenklatur
- 1035
- 51
- Timo Rabenstein
Der Glycosidische Links Sie sind die kovalenten Bindungen, die zwischen Zuckern (Kohlenhydraten) und anderen Molekülen auftreten, die andere Monosaccharide oder andere Moleküle verschiedener Natur sein können.
Diese Verbindungen ermöglichen das Vorhandensein mehrerer grundlegender Komponenten für das Leben, nicht nur bei der Bildung von Reservefuhren und Strukturelementen, sondern auch von wesentlichen Informationstransportmolekülen für die zelluläre Kommunikation.
Die Bildung von Polysacchariden hängt grundsätzlich von der Aufstellung von glykosidischen Bindungen zwischen Alkoholemen oder freien Hydroxylgruppen einzelner Monosaccharideinheiten ab.
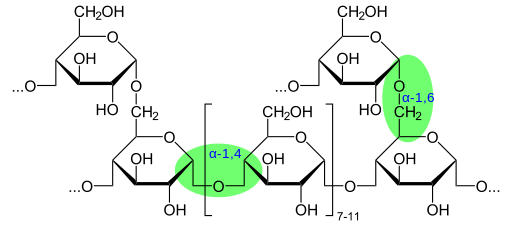 Beispiel für Glycosidbindungen in Glykogen (Quelle: Glykogen.SVG-Neurotkerrivivativ-Arbeit-Marek-M-Public-Domain über Wikimedia Commons)
Beispiel für Glycosidbindungen in Glykogen (Quelle: Glykogen.SVG-Neurotkerrivivativ-Arbeit-Marek-M-Public-Domain über Wikimedia Commons) Glycosidische Verbindungen treten in mehreren Zellkontexten auf, einschließlich der Vereinigung der Polarkopfgruppe einiger Sphingolipide, wesentlichen Bestandteilen der Zellmembranen vieler Organismen und der Bildung von Glykoproteinen und Proteoglykanen.
Wichtige Polysaccharide wie Cellulose, Chitin, Agar, Glykogen und Stärke wären ohne glucosidische Bindungen nicht möglich. Ebenso ist die Proteinglykosylierung, die im endoplasmatischen Retikulum und im Golgi -Komplex auftritt, für die Aktivität vieler Proteine von größter Bedeutung.
Eigenschaften
Glykosidbindungen sind viel unterschiedlicher als ihre Analoga in Proteinen und Nukleinsäuren, da im Prinzip in vielerlei Hinsicht zwei Zuckermoleküle sich in vielerlei Hinsicht zusammenschließen können, da sie mehrere Gruppen haben, die an der Bildung des Links teilnehmen können.
Darüber hinaus bieten die Isomere der Monosaccharide, dh eine der beiden Orientierungen, die die Hydroxylgruppe in der zyklischen Struktur in Bezug auf anomere Kohlenstoff haben kann.
Die Isomere haben unterschiedliche dreidimensionale Strukturen sowie unterschiedliche biologische Aktivitäten. Cellulose und Glykogen bestehen aus wiederholten Einheiten von D-Glucose, unterscheiden sich jedoch in Bezug auf die Art der glucosidischen Bindung (α1-4 für Glykogen und β1-4 für Cellulose) und haben daher unterschiedliche Eigenschaften und Funktionen.
So wie Polypeptide eine Polarität mit einem Ende n- und ein anderes C-und Polynukleotide 5 'und 3' Enden haben, haben Oligo-oder Polysaccharide eine Polarität, die durch Reduzieren von Enden definiert und nicht reduziert wird.
Das reduzierende Ende hat ein freies anomerisches Zentrum, das keine glycosidische Verbindung mit einem anderen Molekül bildet, daher behält es die chemische Reaktivität des Aldehyds bei.
Kann Ihnen dienen: externe BefruchtungDie glucosidische Bindung ist die flexibelste Region einer Oligo-oder Polysaccharid.
Glykosidbindungsbildung
Die glucosidische Bindung kann zwei Monosaccharidmoleküle durch einen und die Hydroxylgruppe der anderen verbinden. Das heißt.
Im Allgemeinen erfolgt die Bildung dieser Verbindungen durch Kondensationsreaktionen, bei denen ein Wassermolekül mit jedem gebildeten Glied freigesetzt wird.
Bei einigen Reaktionen verlässt Sauerstoff das Zuckermolekül jedoch nicht als Wasser, sondern als Teil der Diphosphatgruppe eines Diphosphat -Uridin -Nucleotids.
Die Reaktionen, die zu glucosidischen Verbindungen führen. Sie werden zwischen einem kovalent modifizierten Zucker durch Zugabe einer Phosphatgruppe oder eines Nukleotids (6-phosphat-Glucose, UDP-Galactose) gebildet.
Glykosidbindungshydrolyse
Glykosidbindungen können in leicht sauren Umgebungen leicht hydrolysieren, aber sie widerstehen recht alkalische Umgebungen.
Die enzymatische Hydrolyse von glucosidischen Bindungen wird durch Enzyme vermittelt, die als Glycosidasen bekannt sind. Viele Säugetiere besitzen diese Enzyme für den Zelluloseabbau nicht, sodass sie nicht in der Lage sind, Energie aus diesem Polysaccharid zu extrahieren, obwohl sie eine essentielle Faserquelle sind.
Wiederkäuer wie Kühe haben zum Beispiel Bakterien, die mit ihrem Darm assoziiert sind, die Enzyme produzieren, die die Cellulose, die sie essen.
Das glatte Enzym, das in den Tränen des Auges und durch einige bakterielle Viren hergestellt wird Bakterien.
Diversität
Oligosaccharide, Polysaccharide oder Glykane sind sehr unterschiedliche Moleküle, und dies ist auf die vielfältigen Möglichkeiten zurückzuführen.
Diese Vielfalt beginnt, wie oben erwähnt, dass Zucker Hydroxylgruppen haben, die unterschiedliche Gewerkschaftsregionen ermöglichen und dass die Bindungen zwischen den beiden möglichen Stereoisomeren in Bezug auf den anomeren Kohlenstoff von Zucker (α oder β) auftreten können.
Kann Ihnen dienen: BlastozoosEs können glycosidische Verbindungen zwischen einem Zucker und jeder hydroxylierten Verbindung wie Alkohol oder Aminosäuren gebildet werden.
Darüber hinaus kann ein Monosaccharid zwei glucosidische Bindungen bilden, sodass es als Zweigpunkt dienen kann, was eine mögliche Komplexität in der Struktur von Glykanen oder Polysacchariden in Zellen einführt.
Leute
In Bezug auf Arten von glucosidischen Bindungen können zwei Kategorien differenziert werden: die glucosidischen Bindungen zwischen Monosacchariden, die die Oligo- und Polysaccharide bilden, und die glucosidischen Bindungen, die in Glucoproteinen oder Glucolipiden auftreten, die Proteine oder Lipide mit Carbohyhhydrates sind, die Proteine oder Lipide mit Carbohydrates sind.
O-Glucosid-Links
Es treten o-glycosidische Verbindungen zwischen Monosacchariden auf, die durch die Reaktion zwischen der Hydroxylgruppe eines Zuckermoleküls und dem anomeren Kohlenstoff eines anderen gebildet werden.
Disaccharide stammen aus den häufigsten Oligosacchariden. Polysaccharide haben mehr als 20 Einheiten von Monosacchariden, die linear zusammengefügt sind und manchmal mehrere Auswirkungen haben.
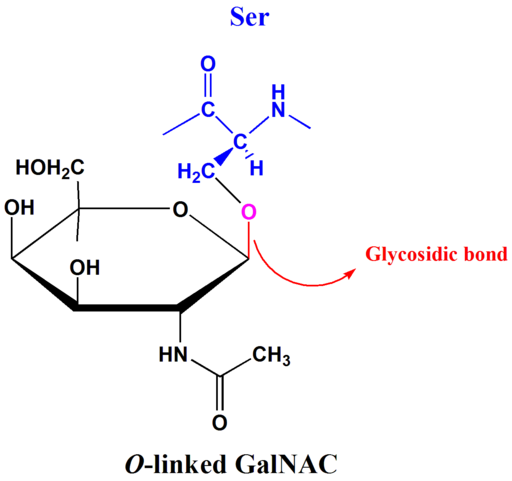 Beispiel für O-Glucosidic Link (Quelle: Tpirojsi [Public Domain] über Wikimedia Commons)
Beispiel für O-Glucosidic Link (Quelle: Tpirojsi [Public Domain] über Wikimedia Commons) In Disacchariden wie Maltose, Lactose und Saccharose ist die häufigste glucosidische Bindung der O-Glycosid-Typ. Diese Verbindungen können zwischen Kohlenstoffen und -OH von isomeren Formen α oder β auftreten.
Die Bildung von glucosidischen Bindungen in Oligo- und Polysacchariden hängt von der stereochemischen Natur der verbundenen Zucker sowie ihrer Anzahl von Kohlenstoffatomen ab. Im Allgemeinen treten für Zucker mit 6 Kohlenstücken lineare Bindungen zwischen den Kohlenstoff 1 und 4 oder 1 und 6 auf.
Es gibt zwei Hauptarten von o-Glykoside, die abhängig von der Nomenklatur als α und β oder 1,2 definiert sind-Cis und 1.2-trans-Glykoside.
Der Abfall 1.2-Cis Glykosylierte α-Glykoside für D-Glycose, D-Galactose, L-Fucosa, D-Xilosa oder β-Glycoside für die D-Manosa L-Yarabinosa; sowie 1.2-trans (β-Glycoside für D-Glucose, D-Galactose und α-Glycoside für D-Many usw.) sind für viele natürliche Komponenten von großer Bedeutung.
O-Glycosylierung
Eine der häufigsten Modifikationen nach post -translational ist die Glykosylierung, die in der Zugabe eines Glucid -Teils zu einem wachsenden Peptid oder Protein besteht. Mucine, Sekretionsproteine, können große Mengen von Oligosaccharidketten enthalten, die durch O-glucosidische Bindungen verbunden sind.
Der O -Glykosylierungsprozess tritt im Golgi -Komplex der Eukaryoten auf und besteht aus der Vereinigung von Proteinen zum glukidalen Teil durch eine glucosidische Bindung zwischen der -OH.
Kann Ihnen dienen: Glucolipids: Was sind, Klassifizierung, Struktur, FunktionenDie Bildung dieser Bindungen zwischen Kohlenhydraten und Hydroxylisin und Hydroxilisin sowie die phenolische Gruppe von Tyrosinabfällen wurde ebenfalls beobachtet.
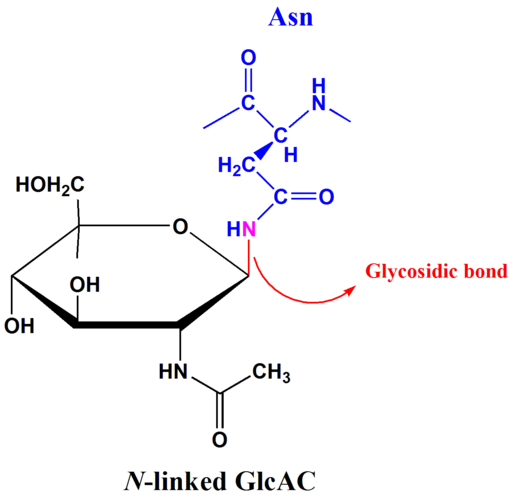
N-Glucosid-Links
N-Glycycosidische Verbindungen sind unter glykosylierten Proteinen am häufigsten. Die N-Glykosylierung tritt hauptsächlich im endoplasmatischen Retikulum von Eukaryoten auf, wobei nachfolgende Modifikationen im Golgi-Komplex auftreten können.
 Beispiel für N-Glucosidic Link (Quelle: Tpirojsi [Public Domain] über Wikimedia Commons)
Beispiel für N-Glucosidic Link (Quelle: Tpirojsi [Public Domain] über Wikimedia Commons) Die N-Glykosylierung hängt von der Vorhandensein der ASN-XXX-Serie/Thr-Konsensussequenz ab. Die glycosidische Bindung tritt zwischen dem inmitten Stickstoff der Seitenkette von Asparagin und anomerem Zuckerkohlenstoff auf, der an die Peptidkette bindet.
Die Bildung dieser Bindungen während der Glykosylierung hängt von einem Enzym ab.
Andere Arten von glucosidischen Verbindungen
S-glucosidische Verbindungen
Sie treten auch zwischen Proteinen und Kohlenhydraten auf, die zwischen Peptiden mit N-terminalen Cysteinen und Oligosacchariden beobachtet wurden. Peptide mit dieser Art von Verbindungen wurden anfänglich aus Protein im Urin isoliert und menschliche Erythrozyten, die mit Glucose -Oligosacchariden verbunden waren.
C-Glucosid-Verbindungen
Sie wurden zuerst als post -translationale Modifikation (Glykosylierung) in einem Tryptophanrest in RNASA 2 im menschlichen Urin und in der Erythrozyten 2 beobachtet. Eine Hand ist an Kohlenstoff aus Position 2 des Aminosäurernkerns mittels einer clucosidischen Bindung bindet.
Nomenklatur
Der Begriff Glykosid wird verwendet, um Zucker zu beschreiben, dessen anomere Gruppe durch eine Gruppe -OR (o -Glycoside), -sr (Tioglycoside), -ser (Selenoglucoside), -nr (n -Glykoside oder Glucosamine) oder sogar -CR ersetzt wird (C-Glucoside).
Sie können auf drei verschiedene Arten benannt werden:
(1) Ersetzen des "-O" -Anminals des Namens der entsprechenden zyklischen Form des Monosaccharid.
(2) Verwenden des Begriffs "Glycosyloxi" als Präfix des Namens des Monosaccharids.
(3) Verwenden des Begriffs ENTWEDER-Glycosil, N-Glycosil, S-Glycosil oder C-Glycosil als Präfix für den Namen der hydroxylierten Verbindung.
Verweise
- Nelson, d. L., & Cox, m. M. (2009). Lehninger Prinzipien der Biochemie. Omega -Ausgaben (5. Aufl.).
- Nomenklatur von Kohlenhydraten (Empfehlungen 1996). (neunzehn sechsundneunzig). Von www abgerufen.Qmul.AC.Vereinigtes Königreich
- « Branchiopoda Was ist, Eigenschaften, Reproduktion, Lebensmittel
- Pazifische Wüste Was ist, Eigenschaften, Klima, Flora, Fauna »

