Epoxy -Nomenklatur, erhalten, Anwendungen, Beispiele
- 2859
- 395
- Medine Kedzierski
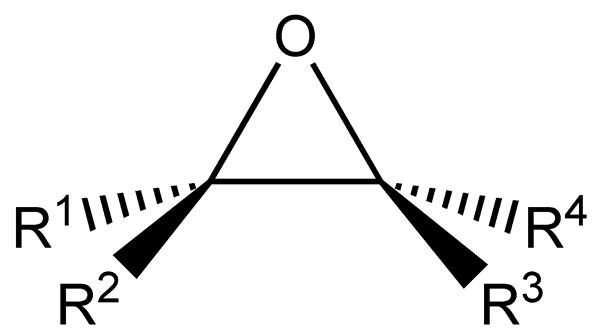
Der Epoxide Sie sind aliphatische oder zyklische Kohlenwasserstoffe mit einem Sauerstoffatom, das gleichzeitig mit zwei Kohlenstoffatomen in ihrer Struktur verbunden ist. Dieser Link zeigt, wie im unteren Bild, eine dreieckige Geometrie vorgestellt, die für alle Epoxide ziemlich charakteristisch ist.
Epoxide stammen aus Alkenen, die den Bruch einer Doppelbindung zur Bildung der Epoxidfunktionsgruppe leiden. Jedes der beiden mit Sauerstoff verbundenen Atome ist ebenfalls mit lateralen Gruppen verbunden r1, R2, R3 und r4, Alle Teile desselben Moleküls.
 Strukturelle und allgemeine Formel für Epoxide. Quelle: Tomas Kindahl / Public Domain.
Strukturelle und allgemeine Formel für Epoxide. Quelle: Tomas Kindahl / Public Domain. Die Epoxidfunktionsgruppe ist durch große Spannung gekennzeichnet, die eine größere Reaktivität als die eines nicht -cyclischen Ethers verleiht. Epoxidreaktionen werden normalerweise vom Bruch ihrer funktionellen Gruppe begleitet.
Das einfachste Epoxid entspricht Ethan -Epoxid, auch Ethylenoxid, Ethylenoxid oder Oxirano. Von allen ist dies das Epoxid von größerer kommerzieller Bedeutung.
Der größte Anteil der Epoxidproduktion ist für die Malerei bestimmt (Oberflächenbeschichtungen). Sie werden auch zur Herstellung von Tensiden, Klebstoffen, Plastizierern usw. verwendet.
[TOC]
Nomenklatur
Verbindungen mit der epoxidfunktionellen Gruppe können auf unterschiedliche Weise aufgerufen werden, wie z.
Epoxide mit einfacheren chemischen Strukturen werden normalerweise als Oxide bezeichnet. Auf diese Weise Probeno -Epoxid (C3H6) Es heißt Propeno Oxid (c3H6ENTWEDER).
Es ist üblich, als Epoxid bezeichnet zu werden, das Kohlenstoffe identifiziert, die in der Epoxidfunktionsgruppe vorhanden sind. Zum Beispiel: 2,3-Epoxyhexan, 1,2-Epoxychiclohexan und 1,2-Epoxipropan. Das heißt, das "Dreieck" befindet sich in den Kohlenstoffen 2 und 3 des Hexans und so weiter mit dem Cyclohexan und Propan.
Kann Ihnen dienen: EnthalpieErhalten
Katalytische Oxidation
Ethno- oder Ethylenoxid -Epoxid wird durch die katalytische Oxidation von Ethylen in heißer Luft oder Sauerstoff hergestellt, die als Metallsilberkatalysator verwendet wird:
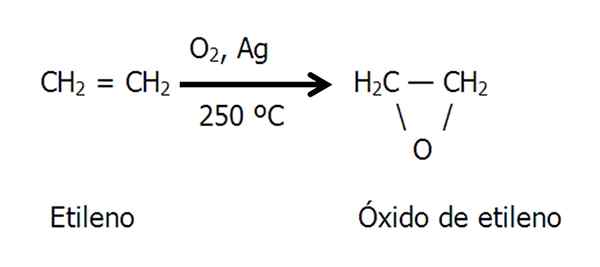 Gleichung für die Ethylenoxidsynthese. Quelle: Gabriel Bolívar.
Gleichung für die Ethylenoxidsynthese. Quelle: Gabriel Bolívar. Chlorhydrin -Methode
Diese Methode wird in zwei Stufen durchgeführt: a) Chlorhydrinbildung und b) Behandlung von Chlorhydrin mit einer Grundlage zur Eliminierung von Salzsäure.
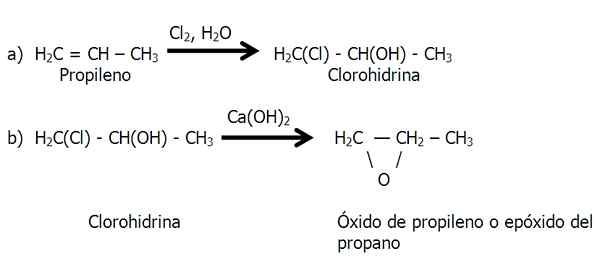 Stadien der Chlorhydrin -Methode zur Epoxidsynthese. Quelle: Gabriel Bolívar.
Stadien der Chlorhydrin -Methode zur Epoxidsynthese. Quelle: Gabriel Bolívar. In Stufe b) Ein HCL -Molekül ist verloren, dessen Wasserstoff aus der OH -Gruppe stammt.
Peroxidation von Doppelbindungskohlenstoff-Kohlenstoff-Kohlenstoffstoffe
Epoxide können auch durch Peroxidation von Alkenen gebildet werden, dh eine Oxidation, die durch einen Schläger verursacht wird, wie z. B. Peroxibenzoesäure:
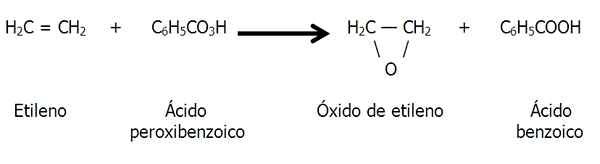 Peroxidation von Ethylen zur Bildung von Ethylenoxid oder Ethanepoxid. Quelle: Gabriel Bolívar.
Peroxidation von Ethylen zur Bildung von Ethylenoxid oder Ethanepoxid. Quelle: Gabriel Bolívar. Natürliches Vorhandensein von Epoxiden
Epoxide sind ungewöhnlicher Natur. Die Lebersynthese von Epoxiden wurde jedoch beobachtet, vermittelt durch Cytochrom P450. Zellen produzieren Epoxide als Oxidationsprodukte von Alquenos und aromatischen Verbindungen.
In der Natur wurden auch Verbindungen wie Epotylonas beobachtet, die als sekundärer Metaboliten der Sorangium cellosumischen Bakterien hergestellt wurden.
Anwendungen
Herstellung von Tensiden
Ethylenoxid wird häufig bei der Herstellung von Tensiden oder Tensiden, Alkohol- oder Phenolreaktionsprodukten mit Ethylenoxid verwendet. Tenside erfüllen unterschiedliche Funktionen, darunter: Feuchtigkeitscremes, Reinigungsmittel, Emulgatoren und Solubilizer.
Feuchtigkeitscremes erhöhen die Oberflächenhydratation durch Erleichterung des Wasserzugangs zu ihnen. Reinigungsmittel eliminieren Schmutz aus Kleidung. Emulsionen erlauben und stabilisieren Emulsionen. Und Solubilizer ermöglichen die Auflösung einiger mischbarer Verbindungen mit Wasser.
Kann Ihnen dienen: Fick LawKlebstoffe und Lösungsmittel
Die Reaktion von Epoxiden, einschließlich Ethylenoxid, mit Aminen ist die Grundlage für die Herstellung von Warteschlangen oder Zahnfleischpaste. Diese Klebstoffe werden verwendet, um die Vereinigung von Oberflächen sowie bei der Stabilisierung des PVC zu produzieren.
Ethylenoxid reagiert mit Natriumetoxid, um 2-Toxietanol zu produzieren, auch als Cellosolve bekannt. Diese chemische Verbindung löst Öle, Harze, Fette, Wachse, Nitrocellulose und Lacas auf.
Epoxidharze
Epoxid- oder Epoxidharze haben unter ihren Eigenschaften, sobald sie verstärkt wurden, hohe chemische, thermische und mechanische Resistenz. Diese Widerstände ermöglichen ihre Verwendung für die Ausarbeitung von Lacas und Emaille sowie für die Beschichtung von Metallen und Laborböden und Herstellung von elektrischen Teilen.
Einige Unternehmen verwenden diese Harze mit Silica -Füllstoffen, die Porzellan ersetzen, um Isolatoren für elektrische Linien herzustellen. Epoxidharze werden auch verwendet, um Blätter für gedruckte Schaltkreise und mit Glasfasern verstärkte Platten zuzubereiten.
Epoxidharze haben nur wenige Verwendungen getrennt, einschließlich der Vinylstabilität. Um ihre Nützlichkeit zu erhöhen, sind sie in einem Prozess, der als "gehärtet" bekannt ist, mit mehreren Verbindungen verbunden. Unter den für diesen Zweck verwendeten Wirkstoffen: Primär, sekundäre, tertiäre und Polyamide.
Aus Pflanzenölen erhaltene Epoxide werden für die Polio -Synthese verwendet, die in der Polyurethanindustrie verwendet werden.
Medizinische Anwendungen
Epotylonas sind metabolische Produkte der Sorangium -Cellulosum -Bakterien, die die Eigenschaft stabilisierender Mikrotubuli aufweisen und so eine Blockierung des Zellzyklus erzeugen.
Die Verwendung von Ixabepilon, einem Epotylonas, wurde zur Behandlung von fortgeschrittenem Brustkrebs zugelassen. Ebenso wurde die Verwendung des Epotylon D bei der Behandlung von Alzheimer untersucht.
Kann Ihnen dienen: Disulfursäure: Was ist, Struktur, Eigenschaften, verwendetAndere Verwendungen
Ethylenoxid interveniert die Ethylenglykolsynthese: Verbindung als Frostschutzmittel in Autoskühlsystemen verwendet. Ethylenoxid wird auch zur Sterilisation von medizinischen Materialien und Instrumenten verwendet.
Toxizität
Absorption durch Haut, Inhalation oder Epoxidaufnahme sind mit der Produktion toxischer Wirkungen sowohl bei Menschen als auch bei experimentellen Tieren verbunden. Dazu gehören: Reizung von Oberflächengeweben und Sensibilisierung. Veränderungen der Leberfunktion, Blutkörperchen und Knochenmark werden ebenfalls erzeugt.
Ebenso sind Epoxide mit Karzinogenität und Mutagenität mit Epoxiden zusammenhängen. Eporoxide wurden aufgrund ihrer hohen elektrophylischen Reaktivität und ihres Charakters von gemieteten Verbindungen als potenzielle krebserregende Wirkstoffe angesehen.
Beispiele für Epoxid
Schließlich werden einige andere Beispiele für Epoxids aufgelistet:
-1,2-Epoxipropan
-2,3-Epoxyhexan
-1,2-Epoxyclohexan
-Oxid strecken
-Isobutilenoxid
-3,4-Epoxi-1-Butno
Verweise
- Graham Solomons t.W., Craig b. Braten. (2011). Organische Chemie. (10th Auflage.). Wiley Plus.
- Carey f. (2008). Organische Chemie. (Sechste Ausgabe). Mc Graw Hill.
- Morrison und Boyd. (1987). Organische Chemie. (Fünfte Ausgabe). Addison-Wesley Iberoamericana.
- Wikipedia. (2020). Epoxid. Abgerufen von: in.Wikipedia.Org
- Leroy g. Waten. (2020). Epoxid. Encyclopædia Britannica. Erholt von: Britannica.com
- Manson m. M. (1980). Epoxide: Gibt es das Problem der menschlichen Gesundheit? British Journal of Industrial Medicine, 37(4), 317-336. doi.org/10.1136/OEM.37.4.317
- Chemikalien. (S.F.). Beispiele für Epoxid. Erholt von: Chemics.Netz
- W.G. Töpfer. (1963). Die Chemie und Verwendung von Epoxidharzen, Berufsmedizin, Band 13, Ausgabe 1, April 1963, Seiten 42-47, doi.org/10.1093/occmed/13.1.42
- Molinero Muñoz, María und Fernández Arberas, Nerea. (2016). Epotylonas, eine Alternative im Gebiet des Antitumors. Kompletense Madrid University.
- Alejandro Aguirre f. & Lesly Espinoza B. (2018). Verwendung und Anwendungen von Epoxids und Sulfiden. Zentral Universität von Ecuador. Erholt von: Akademie.Edu
- « Nitratseigenschaften, Struktur, Nomenklatur, Schulung
- Cannizzaro -Reaktionseigenschaften, Mechanismen, Beispiele »

