Kaliumphosphat (K3PO4) -Struktur, Eigenschaften, verwendet

- 3423
- 28
- Rieke Scheer
Er Kaliumphosphat Es ist eine anorganische Verbindung, die von drei Ionen Kalium k gebildet wird+ und ein Phosphat -Ionenpo43-. Seine chemische Formel ist k3Po4. Es ist ein farbloser Feststoff oder kristallines Weiß. Es ist sehr löslich in Wasser und bildet alkalische Lösungen, dh mit vielen OH -Ionen-, Daher grundlegender pH -Wert.
Das Phosphation hat eine wichtige Funktion in Zellen, die mit Energiespeicher zu tun hat. Kaliumphosphat wird häufig bei organischen Chemiereaktionen eingesetzt, bei denen es als Basis wirken kann, dh Protonen H+. Es kann auch als Katalysator oder Beschleuniger einiger Reaktionen fungieren.
 Kaliumphosphat k3Po4 solide. Xavier13540 bei chinesischer Wikipedia [Public Domain]. Quelle: Wikimedia Commons.
Kaliumphosphat k3Po4 solide. Xavier13540 bei chinesischer Wikipedia [Public Domain]. Quelle: Wikimedia Commons. Es wurde verwendet, um den Angriff bestimmter Insekten in Weizenpflanzen zu verringern. Es wurde jedoch beobachtet, dass es die Ablösung von Methan (CH) bevorzugt4) Ein Treibhausgas, Reismikrokulturen.
Es wurde als Abführmittel verwendet, um die Dauer einer Lokalanästhesie zu erhöhen, Karies zu stoppen und unter anderem Oberflächen abzudecken.
[TOC]
Struktur
Kaliumphosphat besteht aus drei Kationen Kalium k+ und ein Phosphatanionpo43-.
Die Phosphat -Ionenpo43- Es besteht.
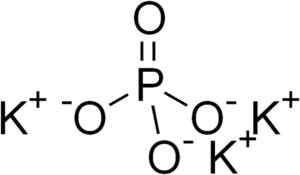 Kaliumphosphatstruktur k3Po4. Edgar181 [Public Domain]. Quelle: Wikimedia Commons.
Kaliumphosphatstruktur k3Po4. Edgar181 [Public Domain]. Quelle: Wikimedia Commons. Nomenklatur
- Kaliumphosphat
- Tripotasiumphosphat
- Kalium -Tribasic Phosphat
- Tripotasiumorthophosphat
Eigenschaften
Körperlicher Status
Farbloser fester oder kristalline Weiß.
Molekulargewicht
212.27 g/mol
Schmelzpunkt
1340 ºC
Dichte
2,564 g/cm3
Löslichkeit
Sehr löslich in Wasser: 106 g/100 g Wasser bei 25 ° C. Unlöslich in Ethanol.
pH
Eine Lösung mit 1% k3Po4 Es hat einen pH-Wert von 11,5-12,3.
Chemische Eigenschaften
Durch das Auflösen in Wasser wird Kaliumphosphat in die drei Kationen Kaliumk getrennt+ und die Phosphatanionpo43-. Das Phosphatanion nimmt ein Proton aus Wasser und das HPO -Wasserstoffhosephosphatanion wird gebildet42-. Letzteres nimmt wiederum ein anderes Wasserproton und wird zum Dihydrophosphat -H -Anion2Po4-.
Kann Ihnen dienen: Wie wird ein elastisches Material synthetisiert??Po43- + H2Oder ⇔ HPO42- + Oh-
HPO42- + H2Oder ⇔ h2Po4- + Oh-
Wenn Formionen oh- Die wässrige Lösung wird alkalisch.
Andere Eigenschaften
Zusätzlich zur wasserfreien Form (ohne Wasser) hat es mehrere hydratisierte Formen; Dies bedeutet, dass das K -Molekül3Po4 Es kann von einer oder mehreren Wassermolekülen innerhalb der kristallinen Struktur begleitet werden.
Aus diesem Grund können Sie sich zum Beispiel k Monohydrat bilden3Po4.H2Oder3Po4.3H2Oder Hepthydrat und Nicht -Dehydrat.
Phosphatfunktion im menschlichen Organismus
Die Phosphat -Ionenpo43- Es ist das am häufigsten vorkommende Anion in den Zellen und übt eine wichtige Funktion bei der Energiespeicherung aus.
Das Phosphation beteiligt sich auch an Bildungs- und Ernährungsaktivitäten von Knochen und Zähnen, da es die Calciumkonzentration auf Blutserum und in zahlreichen Energieübertragungsreaktionen in der Zelle reguliert.
Erhalten
Kaliumphosphat kann aus der Reaktion zwischen KCL -Kaliumchlorid und Ammoniumphosphat (NH) erhalten werden4)3Po4.
Kaliumchlorid + Ammoniumphosphat → Kaliumphosphat + Ammoniumchlorid
3 kcl + (NH4)3Po4 → k3Po4 + 3 NH4Cl
Anwendungen
Als Grundlage für organische Chemiereaktionen
Kaliumphosphat k3Po4 Es wurde in mehreren organischen Chemiereaktionen verwendet. Zum Beispiel dient es in der Synthese von Acetylenen basierend auf dibromierten Verbindungen.
In dieser Synthese tritt eine Dehydrromation (Eliminierung von Wasserstoff und Brom) auf, wobei das k3Po4 Ashidro -Feststoff (ohne Wasser) wirkt als weich.
C6H5-CHBR-CH2BR + 2 K3Po4 → c6H5-C≡CH + 2 kbr + 2 k2HPO4
 Autor: Clker-Free-Vektor-Images. Quelle: Pixabay.
Autor: Clker-Free-Vektor-Images. Quelle: Pixabay. Als Katalysator
Das K3Po4 Es dient als Katalysator in verschiedenen Reaktionen der organischen Chemie. Zum Beispiel wurde es als Feststoff zum Erhalten von Biodiesel aus gebrauchtem Bratöl verwendet.
Biodiesel ist ein Kraftstoff ähnlich wie Diesel, wird jedoch aus Fetten oder natürlichen Ölen erhalten oder nicht.
Kann Ihnen dienen: Coulombimetrie: Grundlagen, Typen, AnwendungenKaliumphosphat war als Katalysator oder Beschleuniger der Reaktion wirksamer als Natriumphosphat3Po4 und CAO Calciumoxid.
In der Landwirtschaft
Das K3Po4 Es wurde verwendet, um Weizenpflanzen zu behandeln und sie gegen bestimmte Schädlinge resistent zu machen.
 Weizenpflanzen können mit K behandelt werden3Po4 gegen einige Arten von Insekten resistent zu sein. Autor: Hans Braxmeier. Quelle: Pixabay.
Weizenpflanzen können mit K behandelt werden3Po4 gegen einige Arten von Insekten resistent zu sein. Autor: Hans Braxmeier. Quelle: Pixabay. Einige Forscher versuchten Weizensamen mit Kaliumphosphat und stellten sich heraus, dass diese Resistenz gegen Blattläuse Duraphis Noxia, Ein Insekt, das diese Pflanzen angreift.
Nach Anwendung einer verdünnten Lösung von k3Po4 Bei den Sämlingen gab.
 Autor: Hans Braxmeier. Quelle: Pixabay.
Autor: Hans Braxmeier. Quelle: Pixabay. In medizinischen Anwendungen
Kaliumphosphat wurde verwendet, um den Anästhesieffekt von Lidocain, einem Lokalanästhetikum, zu verändern. Ein Lokalanästhetikum ist ein Medikament, das in einem Bereich des Körpers in diesem Bereich Verlust der Schmerzempfindlichkeit erzeugt.
Es wurde festgestellt, dass k3Po4 Es ermöglicht die Verlängerung der Lokalanästhesie von Lidocain.
Wie Abführmittel
Kaliumphosphat erhöht die Fluidität des Darmgehalts, da es hilft.
In Veterinärmedizin
Das K3Po4 Es wird bei Tieren mit diabetischer Ketoacidose (eine Komplikation von Diabetes) zur Behandlung von Hypophospathie (geringe Menge an Phosphat im Blut) verwendet.
Wenn es jedoch übermäßig geliefert wird, kann es jedoch Hypokalzämie (wenig Kalzium im Blut), Hyperphospathie (überschüssiges Phosphat im Blut), unfreiwillige Kontraktion der Muskeln, Mineralisierung von Weichgeweben und Nierenversagen verursachen.
 Hunde mit Diabeticazidose können mit Kaliumphosphat behandelt werden. Autor: David Mark. Quelle: Pixabay.
Hunde mit Diabeticazidose können mit Kaliumphosphat behandelt werden. Autor: David Mark. Quelle: Pixabay. Bei der Erlangung von DNA
Kaliumphosphat wurde als Puffer verwendet, um DNA in den Genetiklabors zu reinigen.
DNA ist ein Protein in Zellen und enthält alle genetischen Informationen, die für die Entwicklung und Funktionsweise von Lebewesen erforderlich sind.
Es kann Ihnen dienen: fraktionelle Destillation: Prozess, Geräte, Anwendungen, BeispieleDurch die Isolierung der DNA befassen sich die Wissenschaftler in das Studium, wie erbliche Charaktere übertragen werden, sodass Kaliumphosphat sehr hilfreich ist.
 Zeichnen von DNA -Molekül. Autor: Public Domainpartures. Quelle: Pixabay.
Zeichnen von DNA -Molekül. Autor: Public Domainpartures. Quelle: Pixabay. In mehreren Anwendungen
Kaliumphosphat k3Po4 es dient:
- als Nahrungsergänzungsmittel,
- für den Elektrolytersatz,
- Als Puffer, das ist ein chemisches System, mit dem die OH -Ionenwerte kontrolliert werden können- oder Wasserstoff h+ In wässriger Lösung,
- Die Bildung von Zahnkaries stoppen oder hemmen,
- als Korrosionsinhibitor und Anti -Sniff -Mittel,
- Als Mittel zur Behandlung von Oberflächen und Beschichtungsmittel,
- als Frostschutzmittel,
- in Reinigungsprodukten.
 Korrodierte Röhrchen. Das K3Po4 Ermöglicht, Korrosion in den Rohren einiger Branchen oder Prozesse zu vermeiden. Autor: Michael Gaida. Quelle: Pixabay.
Korrodierte Röhrchen. Das K3Po4 Ermöglicht, Korrosion in den Rohren einiger Branchen oder Prozesse zu vermeiden. Autor: Michael Gaida. Quelle: Pixabay. Negativer Aspekt für die Verwendung in der Landwirtschaft
Bestimmte Forscher fanden das durch Hinzufügen von K3Po4 Eine Methanemission wird auf eine Reismikultur erhöht (wählen Sie4) zur Atmosphäre. Methan ist ein Gas, das zum Treibhauseffekt und zur Erhöhung der Temperatur unseres Planeten beiträgt.
Verweise
- ODER.S. Nationalbibliothek für Medizin. (2019). Kaliumphosphat. Aus Pubchem geborgen.NCBI.NLM.NIH.Regierung.
- Panciera, d.L. (2012). Fluidtherapie bei endokrinen und metabolischen Störungen. Phosphor -Supplementierung. In Fluid-, Elektrolyt- und Säure-Base-Störungen in der Praxis kleiner Tier (vierte Ausgabe). Von Scientedirect erholt.com.
- Shenawi-khalil, s. et al. (2012). Synthese von Acetylenen über Dehydrobromation unter Verwendung von fest wasserfreiem Kaliumphosphat als Base unter Phasentransferzustand. Tetraedron Letters, Band 53, Ausgabe 18, 2012, Seiten 2295-2297. Von Scientedirect erholt.com.
- Guan, g. et al. (2009). Tri-Passium-Phosphat als fester Katalysator für die Biodieselproduktion aus Abfallöl. Kraftstoffverarbeitungstechnologie, Volumen 90, Ausgabe 4, 2009, Seiten 520-524. Von Scientedirect erholt.com.
- Kulkami, m.ZU. (2012). Mechanistischer Ansatz für die Expansion und lösungsmittelfreie Synthese von α-Hydroxyphosphonaten unter Verwendung von Kaliumphosphat als Katalysator. COMPTES Rendus Chimie, Band 16, Ausgabe 2, 2013, Seiten 148-152. Von Scientedirect erholt.com.
- Venter, e. et al. (2014). Kaliumphhosphat induziert Toleranz -Anti -in -In -Stall der russischen Weizenblattlaus (Duraphis Noxia, Homoptera: Aphididae) in Weizen. Crop Protection Vol 61, Juli 2014, Seiten 43-50. Von Scientedirect erholt.com.
- Bonturi, n. et al. (2013). Natriumcitrat und Kaliumphosphat als alternative Adsorptionspuffer in hydrophoben und aromatischen thiophilen chromatographischen Reinigung von Plasmid -DNA aus neutralisiertem Lysat. Journal of Chromatography B, Volumes 919-920, 2013, Seiten 67-74. Von Scientedirect erholt.com.
- Conrad, r. und Kose, m. (2005). Wirkung von Kaliumphosphat -Fertilisation auf die Produktion und Emission von Methan und IHS 13C-stabile Isotopenzusammensetzung in Reismikrokosmos. Bodenbiologie und Biochemie, Vol 37, Ausgabe 11, 2005, Seiten 2099-2108. Von Scientedirect erholt.com.
- Blei, d.R. (Herausgeber) (2003). CRC -Handbuch für Chemie und Physik. 85th CRC Press.
- Rauchfuß. (2019). Tipotium -Phosphat. Abgerufen von.Wikipedia.Org
- « Merkmale Eingabegeräte, Wie verwendet man, Typen, Beispiele, Beispiele
- Struktur der Tumornekrosefaktor (TNF), Wirkungsmechanismus, Funktion »

