Oxidative Phosphorylierungsstadien, Funktionen und Inhibitoren
- 1434
- 112
- Frederike Birkemeyer
Der Oxidative Phosphorylierung Es ist ein Prozess, bei dem ATP -Moleküle von ADP und P synthetisiert werdenYo (Anorganisches Phosphat). Dieser Mechanismus wird von Bakterien und eukaryotischen Zellen durchgeführt. In eukaryotischen Zellen wird die Phosphorylierung in der mitochondrialen Matrix von nicht -photosynthetischen Zellen durchgeführt.
Die ATP -Produktion wird durch die Übertragung von Elektronen aus dem Nadh oder Fadh Coenzyme geleitet2 zu2. Dieser Prozess stellt die größte Energieerzeugung in der Zelle dar und wird aus dem Abbau von Kohlenhydraten und Fetten abgeleitet.
 Quelle: Robot8a [CC BY-SA 4.0 (https: // creativecommons.Org/lizenzen/by-sa/4.0)]]
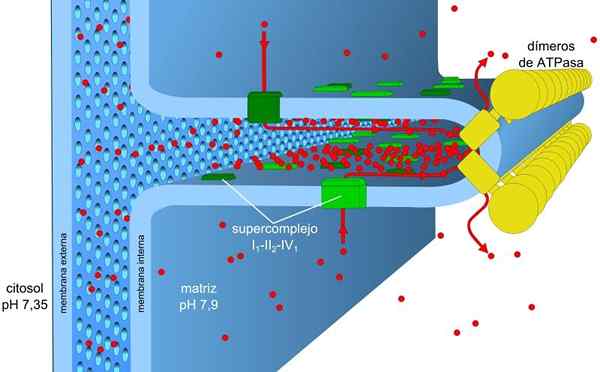
Quelle: Robot8a [CC BY-SA 4.0 (https: // creativecommons.Org/lizenzen/by-sa/4.0)]] Die Energie, die in der Last- und pH -Gradienten gespeichert ist, auch als protonische motorische Kraft bezeichnet, ermöglicht es, dass dieser Prozess durchgeführt werden kann. Der erzeugte Protonengradient führt dazu, dass der externe Teil der Membran aufgrund der Protonenkonzentration eine positive Belastung aufweist (H)+) und die Mitochondrienmatrix ist negativ.
[TOC]
Wo oxidative Phosphorylierung auftritt?
Elektronentransport und oxidative Phosphorylierungsprozesse sind mit einer Membran verbunden. In Prokaryoten werden diese Mechanismen durch die Plasmamembran durchgeführt. In eukaryotischen Zellen sind sie mit der Mitochondrienmembran assoziiert.
Die Anzahl der in den Zellen gefundenen Mitochondrien variiert je nach Zelltyp. Zum Beispiel fehlen bei Säugetieren Erythrozyten diese Organellen, während andere Zelltypen wie Muskelzellen Millionen von ihnen haben können.
Die Mitochondrienmembran besteht aus einer einfachen externen Membran, einer etwas komplexeren inneren Membran, und in der Mitte des intermembranalen Raums, in dem sich viele von ATP abhängige Enzyme befinden.
Die äußere Membran enthält ein Protein namens Porina, das die Kanäle für die einfache Diffusion kleiner Moleküle bildet. Diese Membran ist für die Aufrechterhaltung der Struktur und Form der Mitochondrien verantwortlich.
Die innere Membran hat eine größere Dichte und ist reich an Protein. Es ist auch wasserdicht für Moleküle und Ionen. Um es zu überqueren, brauchen sie intermembranale Proteine, die sie transportieren.
Innerhalb der Matrix erstrecken sich die Falten der internen Membran und bilden Kämme, die es ihm ermöglichen, einen großen Bereich in einem kleinen Volumen zu haben.
Zellergie zentral
Die Mitochondrien gilt als zelluläres Energiezentrum. Darin sind die Enzyme, die an den Prozessen des Zytrasäurzyklus, der Oxidation von Fettsäuren und Redoxenzymen und Proteinen des Elektronentransports und der Phosphorylierung von Redox beteiligt sind.
Der Konzentrationsgradient der Protonen (PH -Gradienten) und der Gradient von Lasten oder elektrisch. Die kleine Durchlässigkeit der inneren Membran für Ionen (außer h+) Ermöglicht den Mitochondrien einen stabilen Spannungsgradienten.
Elektronischer Transport, Protonenpumpen und ATP, die gleichzeitig in den Mitochondrien dank der protonischen Motorkraft erhalten. Der pH -Gradient behält saure Bedingungen in Intermembran- und Mitochondrienmatrix mit alkalischen Bedingungen bei.
Für zwei Elektronen, die auf die O übertragen wurden2 Etwa 10 Protonen werden von der Membran gepumpt, wodurch ein elektrochemischer Gradienten erzeugt wird. Die in diesem Prozess abgelöste Energie wird allmählich durch die Übergabe von Elektronen durch die Förderkette erzeugt.
Stufen
Die Energie, die während Oxid-Reduktionsreaktionen von NADH und FADH freigesetzt wurde2 Es ist erheblich hoch (ca. 53 kcal/mol für jedes Elektronenpaar), um bei der Herstellung von ATP.
Diese sind in vier Komplexen in der inneren mitochondrialen Membran organisiert. Die Kopplung dieser Reaktionen zur ATP -Synthese wird in einem fünften Komplex durchgeführt.
Kann Ihnen dienen: B -Lymphozyten: Eigenschaften, Struktur, Funktionen, TypenElektronentransportkette
NADH überträgt ein paar Elektronen, die in den Komplex I der Elektronentransportkette eintreten. Die Elektronen werden durch einen Eisen-Zuckerförderer auf das Mononukleotid von Flavina und dann auf das UbiKinon (Coenzym q) überführt. Dieser Prozess setzt eine große Menge an Energie frei (16,6 kcal/mol).
Ubiquinona transportiert Elektronen durch die Membran zum Komplex III. In diesem Komplex gehen die Elektronen Cytochrome B und C durch1 Vielen Dank an einen eisernen Zuckertransporter.
Aus Komplex III übertragen Elektronen zum IV -Komplex (Cytochrom -C -Oxidase), das durch Cytochrom C (peripheres Membranprotein) einen übertragen wurde. Im IV -Komplex gehen die Elektronen durch ein Paar Kupferionen (CuZu2+), dann nach Cytochrom cZu, dann zu einem anderen Paar Kupferionen (cuB2+) und von diesem zu Cytochrom zu3.
Schließlich werden Elektronen auf o übertragen2 Welches ist der letzte Akzeptor und bildet ein Wassermolekül (h2O) für jedes empfangene Elektronenpaar. Der Durchgang von Elektronen von Komplex IV nach o2 Es erzeugt auch viel freie Energie (25,8 kcal/mol).
Succinato Coq Reductase
Der II -Komplex (CoQ -Reduktase -Succinat) erhält aufgrund der Oxidation eines Succinat -Moleküls zu Fumarat ein Elektronenpaar aus dem Zitronensäurzyklus. Diese Elektronen werden in die Modeerscheinung überführt und dann durch eine Eisen-Azufre-Gruppe in die Ubiquinona gelangen. Aus diesem Coenzym gehen sie zu Komplex III und folgen der zuvor beschriebenen Route.
Die Energie, die in der Elektronentransferreaktion auf die Modeerscheinung freigesetzt wird+ als der Nadh.
Energiekopplung oder Transduktion
Die im zuvor beschriebene Elektronentransportprozess erzeugte Energie sollte für die ATP -Produktion verwendet werden, die durch die ATP -Synthase oder das Komplexenzym V katalysiert werden. Die Erhaltung solcher Energie wird als Energiekopplung bezeichnet, und der Mechanismus war schwer zu charakterisieren.
Es wurden mehrere Hypothesen beschrieben, um diese Energieübertragung zu beschreiben. Am besten akzeptiert ist die nachstehend beschriebene chemosmotische Kopplungshypothese.
Chemosmotische Kopplung
Dieser Mechanismus schlägt vor, dass die für die ATP -Synthese verwendete Energie von einem protonischen Gradienten in Zellmembranen stammt. Dieser Prozess steckt in Mitochondrien, Chloroplasten und Bakterien und ist mit dem Elektronentransport verbunden.
Die I- und IV -Komplexe des elektronischen Transports wirken als Protonenpumpen. Diese leiden unter Konformationsänderungen, die es ihnen ermöglichen, die Protonen in den intermembranalen Raum zu pumpen. Im IV -Komplex für jedes Elektronenpaar werden zwei Protonen außerhalb der Membran gepumpt und zwei weitere bleiben in der Matrix bilden H2ENTWEDER.
Ubiquinona im Komplex III akzeptiert Protonen der Komplexe I und II und befreit sie außerhalb der Membran. I und III -Komplexe ermöglichen jeweils den Durchgang von vier Protonen für jedes Paar transportierter Elektronen.
Die mitochondriale Matrix hat eine geringe Protonenkonzentration und ein negatives elektrisches Potential, während der intermembranale Raum die inversen Bedingungen darstellt. Der Protonenfluss durch diese Membran impliziert den elektrochemischen Gradienten, der die notwendige Energie (± 5 kcal/mol per Proton) für die ATP -Synthese speichert.
ATP -Synthese
Das ATP -Synthetase -Enzym ist der fünfte Komplex, der an der oxidativen Phosphorylierung beteiligt ist. Ist verantwortlich für die Nutzung der Energie des elektrochemischen Gradienten, um ATP zu bilden.
Dieses transmembraale Protein besteht aus zwei Komponenten: F0 und f1. Die Komponente f0 ermöglicht die Rückgabe der Protonen in die mitochondriale Matrix, die als Kanal und F funktionieren1 katalysiert die Synthese des ATP über ADP und pYo, Nutzung der Energie der genannten Rendite.
Kann Ihnen dienen: Membranfördererproteine: Funktionen und TypenDer ATP -Syntheseprozess erfordert eine strukturelle Veränderung in F1 und die Montage der Komponenten f0 und f1. Die Translokation von Protonen durch f0 Es verursacht Konformationsänderungen in drei Unterummen von f1, Dies als Rotationsmotor fungieren und die Bildung des ATP lenken.
Die Untereinheit, die für die Vereinigung von ADP mit P verantwortlich istYo geht von einem schwachen Zustand (l) zu einem aktiven (t). Wenn die ATP gebildet wird, übergeht eine zweite Untereinheit in einen offenen Zustand (O), der die Freisetzung dieses Moleküls ermöglicht. Nachdem die ATP veröffentlicht wurde, übergeht diese Untereinheit vom offenen Zustand in einen inaktiven Zustand (L).
Die ADP- und P -MoleküleYo Sie schließen sich einer Untereinheit an, die von einem Staat oder dem Staat gelaufen ist l.
Produkte
Die Elektronenförderkette und die Phosphorylierung produzieren ATP -Moleküle. Die NADH -Oxidation erzeugt etwa 52,12 kcal/mol (218 kJ/mol) freier Energie.
Die globale Reaktion für die NADH -Oxidation lautet:
Nadh+1⁄2 oder2 +H+ ↔ h2O+nad+
Die Übertragung von Elektronen aus Nadh und Fadh2 Es tritt in mehreren Komplexen auf, sodass die Änderung der freien Energie ΔG ° in kleinere „Pakete“ unterteilt werden kann, die mit der ATP -Synthese gekoppelt sind.
Die Oxidation eines NADH -Moleküls erzeugt die Synthese von drei ATP -Molekülen. Während die Oxidation eines Fadh -Moleküls2 Es ist an die Synthese von zwei ATP angeschlossen.
Diese Coenzyme stammen aus den Prozessen der Glykolyse und dem Zitronensäurezyklus. Für jedes abgebaute Glukosemolekül enden abhängig von der Position der Zellen 36 oder 38 ATP -Moleküle. Im Gehirn und im Skelettmuskel werden 36 ATP produziert, während 38 ATP im Muskelgewebe produziert werden.
Funktionen
Alle Einheiten, einzelligen und vielzelligen Organismen, benötigen eine minimale Energie in ihren Zellen, um die in ihnen befindlichen Prozesse durchzuführen und wiederum wichtige Funktionen im gesamten Körper beizubehalten.
Stoffwechselprozesse erfordern Energie, um Energie durchzuführen. Der größte Teil der nutzbaren Energie wird durch den Abbau von Kohlenhydraten und Fetten erhalten. Diese Energie leitet sich aus dem oxidativen Phosphorylierungsprozess ab.
Oxidative Phosphorylierungskontrolle
Die ATP -Verwendungsrate in den Zellen, steuert die Synthese derselben und reguliert wiederum aufgrund der Kopplung der oxidativen Phosphorylierung mit der Elektronentransportkette im Allgemeinen auch die elektronische Transportrate.
Die oxidative Phosphorylierung hat eine strikte Kontrolle, die sicherstellt. Es gibt bestimmte Schritte im Elektronentransportprozess und die gekoppelte Phosphorylierung, die die Energieerzeugungsrate regulieren.
Koordinierte Kontrolle der ATP -Produktion
Die wichtigsten Energieproduktionsrouten (Zell -ATP) sind Glykolyse, Zyklus von Zitronensäure und oxidativer Phosphorylierung. Die koordinierte Kontrolle dieser drei Prozesse reguliert die ATP -Synthese.
Die Phosphorylierungskontrolle durch das ATP -Massenwirkungsverhältnis hängt vom genauen Beitrag von Elektronen in der Übermittlungskette ab. Dies hängt wiederum von der Beziehung [NADH]/[NAD ab+] Das wird durch die Wirkung der Glykolyse und des Zitronensäurzyklus erhalten erhalten.
Diese koordinierte Kontrolle wird durch Regulierung der Glykolyse-Kontrollpunkte (Citrat inhibiertes PFK) und des Cytrysäurebetriebs (Dehydrogenase-Pyruvat, Creatase Citrat, Itchitrat-Dehydrogenase und α-Zetoglutarat-Dehydrogenase) durchgeführt.
Kontrolle durch Akzeptor
Der IV -Komplex (Cytochrom -C -Oxidase) ist ein Enzym, das von einem seiner Substrate reguliert wird, dh seine Aktivität wird durch das reduzierte Cytochrom C gesteuert (C2+), was wiederum im Gleichgewicht mit der Beziehung der Konzentrationen zwischen [Nadh]/[nad ist+] und das Massenaktionsverhältnis von [ATP]/[ADP] + [P. PYo].
Es kann Ihnen dienen: Ton: Eigenschaften und FunktionenJe höher die [Nadh]/[nad+] und senken Sie die [ATP]/[ADP]+[PYo], mehr Konzentration wird Cytochrom sein [C2+] und größer wird die Aktivität des Komplexes IV sein. Dies wird beispielsweise interpretiert, wenn wir Organismen mit unterschiedlichen Ruheaktivitäten und hohen Aktivitäten vergleichen.
Bei einer Person mit hoher körperlicher Aktivität den Verbrauch von ATP und damit seine Hydrolyse zu ADP + PYo Es wird sehr hoch sein und einen Unterschied in der Massenaktionsverhältnis erzeugt, die zu einer Zunahme von [C führt2+und daher eine Zunahme der ATP -Synthese. In einer ruhenden Person tritt die umgekehrte Situation auf.
Am Ende nimmt die Geschwindigkeit der oxidativen Phosphorylierung mit der Konzentration von ADP innerhalb der Mitochondrien zu. Diese Konzentration hängt von ADP-ATP-Translokatoren ab, die für den Transport von Adenin-Nukleotiden und p zuständig sindYo Vom Cytosol bis zur Mitochondrienmatrix.
Decakoplantien Agenten
Die oxidative Phosphorylierung wird durch bestimmte chemische Mittel beeinflusst, die es elektronischer Transport ohne die Phosphorylierung des ADP fortsetzen können, wodurch die Produktion und Konservierung von Energie entkoppelt wird.
Diese Mittel stimulieren die Sauerstoffverbrauchsgeschwindigkeit der Mitochondrien in Abwesenheit von ADP, was auch zu einer Zunahme der ATP -Hydrolyse führt. Sie handeln, indem sie einen Vermittler beseitigen oder einen Energiezustand aus der Elektronenförderkette brechen.
Das 2,4-Dinitrofenol, eine schwache Säure, die durch die mitochondrialen Membranen fließt, ist verantwortlich für die Ablassung des Protonen-Gradienten.
Diese Verbindung wurde als "Schlankpille" verwendet, da festgestellt wurde. Es wurde jedoch gezeigt, dass sein negativer Effekt sogar den Tod verursachen könnte.
Die Dissipation des protonischen Gradienten erzeugt Wärme. Braune Fettgewebezellen verwenden hormonell kontrolliert, um Wärme zu erzeugen. Hibernate -Säugetiere und Neugeborene, denen das Haar fehlt.
Inhibitoren
Inhibitorische Verbindungen oder Wirkstoffe verhindern sowohl den Verbrauch von oder2 (elektronischer Transport) wie assoziierte oxidative Phosphorylierung. Diese Wirkstoffe vermeiden die Bildung von ATP durch die Nutzung von Energie, die im elektronischen Transport erzeugt werden. Daher ist die Transportkette, da der Energieverbrauch nicht angeordnet ist.
Oligomicin -Antibiotika arbeitet in vielen Bakterien als Phosphorylierungsinhibitor und verhindert die ADP -Stimulation aus der ATP -Synthese.
Es gibt auch ionophorische Wirkstoffe, die mit Kationen wie K fettlösliche Komplexe ausmachen+ und na+, und durch die Mitochondrienmembran mit diesen Kationen durchlaufen. Die Mitochondrien nutzt dann Energie, die im elektronischen Transport erzeugt werden, um Kationen zu pumpen, anstatt ATP zu synthetisieren.
Verweise
- Alberts, geb., Bray, d., Hopkin, k., Johnson, a., Lewis, J., Raff, m., Roberts, k. & Walter, p. (2004). Essentielle Zellbiologie. New York: Garlandwissenschaft.
- Cooper, g. M., Hausman, r. UND. & Wright, n. (2010). Die Zelle. (pp. 397-402). Marbán.
- Devlin, t. M. (1992). Lehrbuch der Biochemie: mit klinischen Korrelationen. John Wiley & Sons, Inc.
- Garrett, r. H., & Grisham, C. M. (2008). Biochemie. Thomson Brooks/Cole.
- Lodisch, h., Darnell, J. UND., Berk, a., Kaiser, c. ZU., Krieger, m., Scott, m. P., & Matsudaira, p. (2008). Mollekularzellbiologie. Macmillan.
- Nelson, d. L., & Cox, m. M. (2006). Lehninger Prinzipien der Biochemie 4. Ausgabe. Ed Omega. Barcelona.
- Voet, d., & Voet, j. G. (2006). Biochemie. Ed. Pan -American Medical.
- « Euglenophyta -Eigenschaften, Reproduktion, Ernährung, Klassifizierung
- Glucosides Training, Funktion und Typen/Gruppen »

