Quecksilberfulminatstruktur, Eigenschaften, erhalten, verwendet, verwendet
- 690
- 92
- Ibrahim Steuk
Er Quecksilberfulmin Es ist eine anorganische Verbindung, die durch Quecksilber (Hg), Kohlenstoff (C), Stickstoff (N) und Sauerstoff (O) (O) gebildet wird (O). Seine chemische Formel ist HG (CNO)2. Es sollte nicht mit Quecksilber Cyanato verwechselt werden, denn obwohl beide Verbindungen die gleichen Elemente haben, binden die Atome in letzteren unterschiedlich.
Es wurde 1800 vom englischen Chemiker Edward Howard entdeckt. Fast 200 Jahre bevor es jedoch versehentlich vom deutschen Alchemisten Johannes Kurckel synthetisiert worden war, der für die Explosion sie nicht isoliert hatte, aber schriftliche Aufzeichnungen über die verwendeten Zutaten hinterließ.
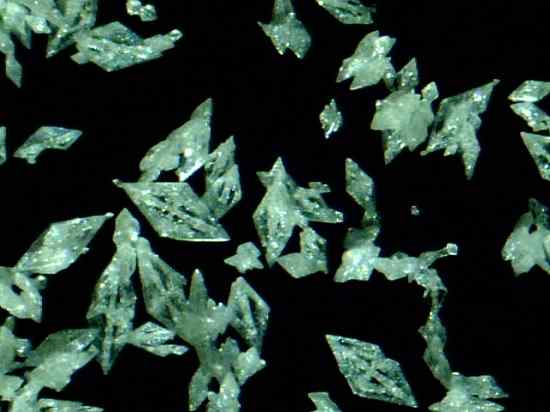
 Quecksilber -Fulminat -Kristalle HG (CNO)2. Daniel Grohmann/CC BY-SA (https: // creativecommons.Org/lizenzen/by-sa/3.0). Quelle: Wikimedia Commons.
Quecksilber -Fulminat -Kristalle HG (CNO)2. Daniel Grohmann/CC BY-SA (https: // creativecommons.Org/lizenzen/by-sa/3.0). Quelle: Wikimedia Commons. Es ist ein primärer Explosiv. Obwohl seine Vorbereitung und Erhaltung äußerst gefährlich sind.
Es wird derzeit zur Detonation starker Dynamitlasten beim Bau von Tunneln und Straßen und Bergbau verwendet.
Es ist eindeutig eine extrem gefährliche Verbindung, die nur von Menschen mit tiefem Wissen über den Umgang mit Sprengstoff manipuliert werden kann.
[TOC]
Struktur
Der HG (CNO)2 Es ist ein HCNO -Fulminsäuresalz. Enthält Quecksilber in Oxidation +2 und zwei cno -fulminierte Einheiten-.
Laut einer 2007 in Deutschland durchgeführten Röntgenstudie (2008 in englischer Sprache) haben Quecksilberfulminatmoleküle die ONC-HG-CNO.
Die C-HG-C-Union ist linear; bildet einen Winkel von 180 ° und die Fulminat-Gruppe (CNO) hat eine kurze Kohlenstoff-Stickstoffbindung und eine längere Stickstoff-Sauerstoffbindung.
Die Länge der C-N-Verbindung beträgt 1,14-1,17 Å (Angstrome), was einer dreifachen schwachen Verbindung entspricht. Die N-O-Verbindung beträgt 1,20-1.25 Å, die eine schwache Doppelbindung anzeigen. Ein Angstrom (Å) ist ein Längenmaß und der zehn -Melonen -Teil eines Messgeräts.
Es kann Ihnen dienen: Methoden zur Trennung homogener Gemische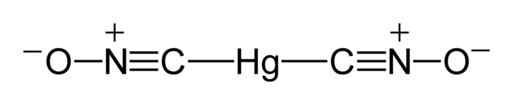 Lewis -Struktur von Quecksilber Fulminat. Benjah-BMM27 / Public Domain. Quelle: Wikimedia Commons.
Lewis -Struktur von Quecksilber Fulminat. Benjah-BMM27 / Public Domain. Quelle: Wikimedia Commons. In festem Zustand, obwohl die C-Hg-C-Union linear ist und die CNO-Gruppe auch die N-C-HG-Gewerkschaft ist, weicht die Linearität in 11 ° ab, dh einen Winkel von 169 ° hat.
 HG -Molekül (CNO)2 Im Feststaat. Grau = Quecksilber; Schwarz = carbon; Blau = Stickstoff; Rot = Sauerstoff. Benjah-BMM27 / Public Domain. Quelle: Wikimedia Commons.
HG -Molekül (CNO)2 Im Feststaat. Grau = Quecksilber; Schwarz = carbon; Blau = Stickstoff; Rot = Sauerstoff. Benjah-BMM27 / Public Domain. Quelle: Wikimedia Commons. Nach der oben genannten Studie ist das vollständige Molekül jedoch in gasförmiger Zustand völlig linear.
Nomenklatur
- Quecksilberfulmin
- Mercuric Fulminat
- Quecksilberdifferenzierung
- Quecksilber bisfulminat
- Fulminsäure -Quecksilbersalz
- Fulminant Quecksilber
- Explosives Quecksilber
Eigenschaften
Körperlicher Status
Weiß bis orange massiv.
 HG (CNO)2 Feucht fest angefeuchtet. Daniel Grohmann/CC BY-SA (https: // creativecommons.Org/lizenzen/by-sa/3.0). Quelle: Wikimedia Commons.
HG (CNO)2 Feucht fest angefeuchtet. Daniel Grohmann/CC BY-SA (https: // creativecommons.Org/lizenzen/by-sa/3.0). Quelle: Wikimedia Commons. Molekulargewicht
284,63 g/mol
Schmelzpunkt
Es schmilzt nicht. Bei mehr als 100 ° C -Heldentaten erhitzt werden.
Dichte
4,42 g/cm3
Löslichkeit
Etwas löslich im Wasser. Löslich in Ethanol (C2H5OH) und Ammoniumhydroxid (NH4OH).
Chemische Eigenschaften
Es ist eine sehr explosive Verbindung und hochempfindlich gegenüber Schlägen, Auswirkungen oder Reibung. Sie können leicht mit Funken und Flammen detonieren. Wenn es für Form Quecksilbergase (HG), Kohlenmonoxid (CO) und Stickstoff (N) zersetzt2).
Mit Schwefelsäure (h2SW4) Konzentrat tritt auch eine gewalttätige Detonation auf. Die Salzsäure löst sie teilweise auf und Mercuric Chlorid tritt auf.
Laut einer Studie, die 1981 durchgeführt wurde, wenn sie unter einer inerten argonischen Atmosphäre kontrolliert und sehr langsam erwärmt wird, tritt bei 120 ° C eine nicht explosive Zersetzung auf, und fest.
Es ist eine Verbindung, die von seltenen Zeiten wegen seiner Gefahr und solchen Studienmöglichkeiten untersucht wurde. Sie müssen im Dunkeln arbeiten, um Explosionen zu vermeiden. Seine Proben sollten unter Wasser und ohne Licht gehalten werden.
 Hg fest (CNO)2 Unter Wasser halten. Daniel Grohmann/CC BY-SA (https: // creativecommons.Org/lizenzen/by-sa/3.0). Quelle: Wikimedia Commons.
Hg fest (CNO)2 Unter Wasser halten. Daniel Grohmann/CC BY-SA (https: // creativecommons.Org/lizenzen/by-sa/3.0). Quelle: Wikimedia Commons. Erhalten
Nach seiner Entdeckung gab es kommerziell durch die Reaktionen zwischen Ethanol (Cho3CH2OH), Quecksilber (Hg) und Salpetersäure (HNO3).
Es kann Ihnen dienen: Clausius-Clapeyron-Gleichung: Wofür es, Beispiele, ÜbungenIn einer der wichtigsten Studien zur Struktur dieser Verbindung schlagen die Forscher vor, dass die erste Hälfte des Gesamtvolumens an Ethanol in die HG- und HNO -Mischung hinzugefügt werden muss, um eine größere Leistung während ihrer Vorbereitung zu erzielen3 Bevor braune Gase verschwinden.
Mit anderen Worten, es ist wichtig, dass Stickoxide vorhanden sind, damit die Reaktion fortgesetzt wird.
Was zuerst passiert, ist die Umwandlung von Ethanol in Acetaldehyd. Nach bestimmten Studien folgt dann mehr Oxidation, Nitrierung, Decarboxylierung und Eliminierung von Lachsäure, damit sich das Fulminat gebildet hat.
Ich benutze als detonierender Agent anderer Sprengstoff
Kriegsanträge
Die ersten Versuche, Quecksilberfulminat als explosive Staub gegen Schusswaffen zu verwenden, waren frustriert über die außergewöhnliche Geschwindigkeit und Gewalt ihrer Detonation.
Die Waffen und Schrotflinten wurden durch kleine Ladungen dieser Verbindung zerstört. Es geschah auch mit Artillerie- und Granatenstücken in Militärtests.
1822 benutzte der englische Wright es jedoch zum ersten Mal als Feuerwehrmann in seinen Sportjagdgewehren. Anschließend wurde in der Bretagne seine Verwendung in Infanterie -Musketen und dann in ganz Europa umgesetzt.
 Im neunzehnten Jahrhundert wurde die Fulminatin des Merkur als Zünder vieler Arten von Kriegswaffen verwendet. Autor: Vetsikas Dimitris. Quelle: Pixabay.
Im neunzehnten Jahrhundert wurde die Fulminatin des Merkur als Zünder vieler Arten von Kriegswaffen verwendet. Autor: Vetsikas Dimitris. Quelle: Pixabay. Bis zum frühen 20. Jahrhundert war es der einzige Zünder, der für das Schießen von Projektilen jeglicher Art verwendet wurde, bis andere Alternativen mit sichereren und zugänglichen Verbindungen umgesetzt wurden.
Friedliche Bewerbungen
Diese Verbindung hat eine wichtige Rolle bei der Entwicklung von Sprengstoff für friedliche Zwecke gespielt.
Seine Rolle bei der Erfindung von Dynamit durch Alfred Nobel war sehr bedeutsam. Dieser Wissenschaftler kombinierte Nitroglycerin, ein starker Sprengstoff mit einem porösen Material, der Erde der Kieselalgen. Aber die Detonation dieser Mischung ist bei Funken oder Dochts schwierig.
Nobel hat diese Schwierigkeit über die Fulminat -Fulminat -Patronen von Quecksilber übertroffen, die in ihrer Anwendung zuverlässig waren. Diese Kombination ermöglicht derzeit ihre Verwendung in Bergbau, Ausbeutung, Tunnelbau und Bauingenieurwesen für Straßenbau, Eisenbahnen, Häfen usw.
Es kann Ihnen dienen: Buteno Es wurde häufig als Zünder von Explosionen im Bergbau und Straßenbau verwendet. Autor: Nyamdorj. Quelle: Pixabay.
Es wurde häufig als Zünder von Explosionen im Bergbau und Straßenbau verwendet. Autor: Nyamdorj. Quelle: Pixabay. Alfred Nobel selbst betonte die grundlegende Bedeutung von Mercury Fulminat in den Entwicklungen für Bauingenieurwesen, die Dynamit förderten.
Risiken
Es ist eine sehr instabile und extrem explosive Verbindung.
 Autor: Clker-Free-Vektor-Images. Quelle: Pixabay.
Autor: Clker-Free-Vektor-Images. Quelle: Pixabay. Es erzeugt akute Toxizität. Es ist giftig, wenn es aufgenommen, eingeatmet wird oder wenn es mit der Haut in Kontakt kommt. Produziert leicht Kontaktdermatitis. Es verursacht Schäden an inneren Organen, wenn die Person sich wiederholt ausgesetzt oder verlängert hat.
Sehr giftig für Wasser- und terrestrisches Leben mit kontinuierlicher langfristiger Gefahr.
Verweise
- Blei, d.R. (Herausgeber) (2003). CRC -Handbuch für Chemie und Physik. 85th CRC Press.
- ODER.S. Nationalbibliothek für Medizin. (2019). Quecksilberdifferenzierung. Aus Pubchem geborgen.NCBI.NLM.NIH.Regierung.
- Munroe, c.UND. (1912). Hinweis zur Herstellung von Quecksilberfulminat. Journal of Industrial & Engineering Chemistry 1912, 4, 2, 152-153. Aus Pubs geborgen.ACS.Org.
- Kurzer, f. (2000). Fulminsäure in der Geschichte der organischen Chemie. J Chem. Bildung. 2000, 77, 7, 851. Aus Pubs geborgen.ACS.Org.
- Beck, w. und Klapötke, T.M. (2008). Quecksilberfulminat: ONC-HG-CNO oder CNO-HG-CER-A DFT-Studie. Journal of Molekularstruktur: Theochem 848 (2008) 94-97. Von Scientedirect erholt.com.
- Wilson, e. (2007). Merkur fulminated Reveared. Archiv Chemical & Engineering News 2007, 85, 36, 10. Aus Pubs geborgen.ACS.Org.
- Brown, m.UND. und Swallowe, G.M. (1981). Die thermische Zersetzung des Silbers (i) und Quecksilbers (ii) Salze von 5-Nitrotetrazol und Quecksilber (ii) fulminieren. Thermochimica Acta, 49 (1981) 333-349. Von Scientedirect erholt.com.
- Alderson, h.UND. (1910). Zur neuen Berufungsdermatose. Dermatitis aufgrund der trockenen Fulmination des Quecksilbers. Cal State J Med 1910 AP; 8 (4): 114. NCBI erholte sich.NLM.NIH.Regierung.
- Wikimedia Foundation (2020). Quecksilber (ii) fulminatieren. Abgerufen von.Wikipedia.Org.
- « Quecksilberchlorid (ii) Struktur, Eigenschaften, erhalten, verwendet, verwendet
- Merkmal und Beiträge der landwirtschaftlichen Zivilisationen »

