Gilbert Newton Lewis
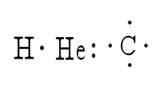
- 4428
- 1352
- Joe Hartwig
 Gilbert Newton Lewis
Gilbert Newton Lewis Gilbert Newton Lewis (1875-1946) war einer der wichtigsten amerikanischen Wissenschaftler des 20. Jahrhunderts. Seine Arbeit führte zu einer strukturellen Revolution in chemischen Studien, dank der zahlreichen Beiträge, die er seines gesamten Lebens für die Entwicklung der Wissenschaft geleistet hat.
Zu den Beiträgen dieser physikalisch -chemischen Stufe stammt aus der Formel, die seinen Namen trägt, mit dem die Elektronenpaare grafisch dargestellt sind. Lewis 'Forschungsarbeit war sehr breit, obwohl sein Ruhm im Grunde auf die Theorie der chemischen Bindungen und die Definition von Säure-Base-Säure im Jahr 1923 zurückzuführen war.
Lewis hatte großen Einfluss auf die wissenschaftliche und akademische Welt der Vereinigten Staaten, insbesondere an der Harvard University, wo der Vorsitzende gegründet und diktiert wurde. Seine Arbeit für die US -Armee während des Ersten Weltkrieg.
Es wurde an den Universitäten von Nebraska, Harvard, Leipzig und Gontinga in Deutschland gegründet. Er arbeitete am Massachusetts Institute (MIT), an der Harvard University und an der University of California, wo er arbeitete.
Während seines gesamten Lebens erhielt er unzählige Anerkennung und Auszeichnungen, darunter mehrere Promotionen in Chicago, Madrid, Liverpool, Wisconsin und Pennsylvania hervorzuheben. Er war Ehrenmitglied mehrerer wissenschaftlicher Institutionen in England, Indien, Schweden, Dänemark und den Vereinigten Staaten.
Biografie
Geburt und frühe Jahre
Gilbert Newton Lewis wurde am 23. Oktober 1875 in Weymouth, Massachusetts, geboren. Seine Eltern waren Frank Wesley Lewis und Mary Burr White Lewis. In seinen frühen Jahren erhielt er Lehren in seinem eigenen Zuhause und trat um 10 in die öffentliche Schule ein, wo er 1889 ihren Abschluss machte.
1884 musste sich Lewis mit seiner Familie in Lincoln, Nebraska, niederlassen. Mit 13 Jahren wurde er in die High School der University of Nebraska aufgenommen.
Kann Ihnen dienen: Beryllium Hydrid (Beh2)Studien
Als er ihren Abschluss machte, fuhr er zwei Jahre lang mit seinem Universitätsstudium fort und schrieb sich dann 1893 an der Harvard University ein.
Zunächst interessierte er sich für die Wirtschaft, entschied sich aber schließlich für Physik und Chemie. Gilbert erhielt 1896 seinen Titel in Chemie und unterrichtete für ein Jahr an der Phillips Academy, einer Privatschule für Andover.
Er kehrte nach Harvard zurück, um den Postgraduiertenjob zu erledigen und 1898 den Master -Abschluss mit seiner These zu erhalten Das Elektron und ein Molekül. Ein Jahr später wurde der Promotion und seine These den Titel " Einige elektrochemische und thermochemische Beziehungen von Zink- und Cadmiumamalgamen".
In Harvard diente er als Ausbilder für ein Jahr und reiste dann mit einem Stipendium nach Europa. Er studierte mit den großen Physikochemikalien der Zeit.
1899 reiste er nach Deutschland, um mit Wilhelm Ostwald Leipzig und dann mit Walter Nernst an der Universität von Gontinga zu studieren. Dann arbeitete er für die philippinische Regierung.
Akademische Arbeit und Teilnahme am Krieg
Zwischen 1999 und 1906 stellte er einen Chemievorsitzenden an der Harvard University aus und dann vom Massachusetts Institute of Technology, wo er von 1907 bis 1912 war.
Später wurde er Professor für physikalische Chemie an der University of California (Berkeley), wo er den Abschluss des Dekans der School of Chemistry erhielt.
1908 veröffentlichte er seinen ersten Artikel über die Theorie der Relativitätstheorie parallel mit Albert Einstein. Darin legt es fest, dass es einen Zusammenhang zwischen der Energiemasa gibt, jedoch in eine andere Richtung als die von Einstein verwendet wird.
Am 21. Juni 1912 heiratete Lewis Mary Fanckley Sheldon, mit der er drei Kinder hatte: Margery s. Lewis, Edward S. Lewis und Richard Newton Lewis.
Es kann Ihnen dienen: Giberélsäure: Eigenschaften, Synthese, FunktionenSeine Arbeit in Kalifornien wurde durch den Ausbruch des Ersten Weltkriegs unterbrochen. 1917 wurde er beauftragt, für die US -Armee zu arbeiten, wo er Leiter der Abteilung für die Verteidigung des Chemischen Krieges wurde.
Lewis 'Liefer- und Arbeitskapazität ermöglichte der Armee. Am Ende des Krieges wurde er für seine Dienste mit den höchsten Auszeichnungen verliehen.
Tod im Labor
Gilbert n. Lewis starb im Alter von 70 Jahren für einen Herzinfarkt, als er am 23. März 1946 in seinem Labor an der Universität von Berkeley arbeitete.
Vielleicht aufgrund seiner introvertierten Persönlichkeit erhielt dieser bedeutende Wissenschaftler den Nobelpreis nie. Fast am Ende seiner Karriere gelang es ihm zu beweisen, dass die Phosphoreszenz organischer Moleküle von einem aufgeregten Triplettstaat bestimmt wird, und sogar seine magnetischen Eigenschaften berechnet.
Beiträge zur Wissenschaft
Einige der wichtigsten Beiträge von Gilbert Newton Lewis zur Wissenschaft sind die folgenden:
Lewis -Strukturen
Sie sind verschiedene Methoden, die die Struktur eines Moleküls darstellen. In diesen stellen die Symbole der Elemente Atome dar, während die Punkte die Elektronen darstellen, die sie umgeben. Ein Beispiel hierfür ist die Darstellung von Wasserstoff, Helium und Kohlenstoff:
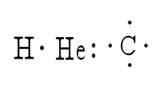
Lewis war der erste, der die Idee vorschlug, dass Atome durch Vergleich von Elektronenpaaren vereint bleiben könnten. Deshalb schuf er die Symbolik der Strukturen.
Die von Lewis vorgeschlagene Wide -Link. Auf diese Weise wurden die Beziehungen zwischen ionischen, molekularen, kovalenten und metallischen Substanzen nachgewiesen. Bis dahin hatten diese Elemente keine konzeptionelle Verbindung.
Kann Ihnen dienen: Art der Verbindung von 02Kovalente Bindung
Konzeptualisierte die kovalente Bindung, die zwischen zwei Atomen bildet, wenn sie sich anschließen, um ein stabiles Oktett zu erreichen und Elektronen des letzten Levels zu teilen, mit Ausnahme von Wasserstoff, das es schafft, Stabilität durch 2 Elektronen zu erreichen.
Oktettstheorie
Es wurde von Lewis im Jahr 1916 angegeben. Dies legt fest, dass die zu den Elementen des Periodensystems gehörenden Ionen mit einer Reihe von 8 Elektronen ihre neuesten Energieniveaus tendieren. Dadurch können sie eine sehr stabile Konfiguration erwerben.
Photon
Es war der Schöpfer im Jahr 1926 des Begriffs Photon, um die kleinste Lichtergieeinheit zu bezeichnen. Dieses Energiepartikel überträgt alle vorhandenen Formen der elektromagnetischen Strahlung (X -Strahlen, Infrarot, Gamma, Ultraviolett, Mikrowellen, Funkwellen usw.).
Chemische Anziehung und Valencia
Zusammen mit seinem chemischen Kollegen Irwing Langmir entwickelte er die Theorie der Anziehung und der chemischen Valenz, die als Langmuir-Lewis-Theorie bekannt ist. Dafür basierte es auf der Atomstruktur von Substanzen.
Schweres Wasser
Lewis war auch der erste Wissenschaftler, der schweres Wasser (Deuterium) in seiner reinsten Form studierte und produzierte. Er war auch der erste, der die Prinzipien der Thermodynamik in der Untersuchung chemischer Probleme anwand.
Auflösungstheorie
Ebenso wird Lewis seine Arbeit über die Theorie der Lösungen anerkannt; Das heißt. Diese als Komponenten bezeichneten Substanzen gehen in Anteile ein, die variieren.

