Zyklisches GMP -Training und -abbau, Struktur, Funktionen
- 1280
- 157
- Tizian Liebich
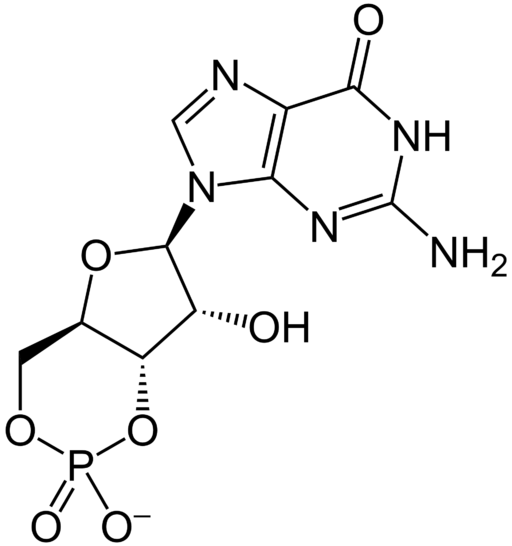
Er Cyclic GMP, Auch als Guanosin cyclischer Monophosphat bekannt, cyclisches Monophosphat von Guanosin oder Guanosin 3 ', 5'-monophosphat, ist ein cyclisches Nukleotid, das an zahlreichen zellulären Prozessen beteiligt ist, insbesondere solche, die mit Signalen und intrazellulären Kommunikation zusammenhängen.
Es wurde vor mehr als 40 Jahren kurz nach der Entdeckung seines Analogon, dem cyclischen Amp, das sich in Bezug auf die stickstoffhaltige Basis davon unterscheidet.
 Chemische Struktur von Guanosín Cyclic Monophosphat oder GMP (Quelle: In: Benutzer: Diberri [CC BY-SA 3.0 (http: // creativecommons.Org/lizenzen/by-sa/3.0/)] über Wikimedia Commons)
Chemische Struktur von Guanosín Cyclic Monophosphat oder GMP (Quelle: In: Benutzer: Diberri [CC BY-SA 3.0 (http: // creativecommons.Org/lizenzen/by-sa/3.0/)] über Wikimedia Commons) Wie andere zyklische Nukleotide wie der oben genannte cyclische Amp oder wie z.
Dieses Nukleotid wird durch ein als Guanilil Ciclasa bekanntes Enzym produziert und kann Protein-Signalstoffe cyclisch abhängige Kinasen in ähnlicher Weise wie zum cyclischen Amp abgeben.
Es wurde nicht nur bei Säugetieren beschrieben, die Tiere von großer Komplexität, sondern auch in den einfachsten Prokaryoten sind, die in den Königreichen von Eubakterien und Bögen enthalten sind. Seine Präsenz in Pflanzen ist immer noch ein Diskussionsgrund, aber die Beweise deuten darauf hin, dass es in diesen Organismen fehlt.
[TOC]
Training und Verschlechterung
Die intrazelluläre Konzentration der cyclischen Nukleotide von Guanina sowie der von Adenin ist extrem niedrig, insbesondere im Vergleich zu den nicht-cyclischen Analoga, die mono-, di- oder trifatisiert sind.
Die Spiegel dieses Nukleotids können jedoch in Gegenwart bestimmter hormoneller Reize und anderer Faktoren selektiv verändert werden, die sich als Primärboten verhalten.
Kann Ihnen dienen: Nukleoid: Eigenschaften, Struktur, Zusammensetzung, FunktionenDer zyklische GMP -Metabolismus ist teilweise unabhängig vom cyclischen Amp -Metabolismus und anderen analogen Nukleotiden. Dies wird von GTP durch ein enzymatisches System, das als Guanilil Ciclassa oder Guanilaato Ciclasa bekannt ist, produziert, das in den meisten Geweben ein teilweise lösliches Enzym ist.
Die Guanilato -Zylaseenzyme sind für die „Zyklation“ der Phosphatgruppe in Position 5 'des zuckerhaltigen Rückstands (Ribose) verantwortlich, was die Vereinigung desselben Phosphats zu zwei verschiedenen OH -Gruppen im selben Molekül verursacht.
Dieses Enzym ist im Dünndarm und im Säugetierlunge sehr häufig und die aktivste Quelle ist im Sperma einer Art Seeigel. In allen untersuchten Organismen hängt es von teile Manganionen ab, die es vom Cyclasas -Adenilat unterscheiden, die von Magnesium oder Zink abhängen.
Der cyclische GMP.
Sowohl Prozesse, Schulung und Abbau werden sorgfältig intrazellulär kontrolliert.
Struktur
Die Struktur des cyclischen GMP verteilt die anderer cyclischer Nukleotide nicht erheblich erheblich. Wie der Name schon sagt (Guanosina 3 ', 5'-monophosphat), hat eine Sauerstoff-Phosphatgruppe im Kohlenstoff der 5' Position eines Riemiszucker.
Dieser Ribosezucker ist gleichzeitig mit der Stickstoffbasis des heterocyclischen Guanin -Guanin -Rings verbunden.
Kann Ihnen dienen: DiposomeDie Phosphatgruppe, die am Sauerstoffatom in der 5' -Riboseposition befestigt ist trans Durch eine Phosphodiéster-Bindung, die zwischen derselben Phosphatgruppe und dem Sauerstoff des Kohlenstoffs in Position 3 'der Ribose auftritt, wodurch ein 3'-5'-Phosphat gebildet wirdTrans-Fusado " (Aus Englisch 3'-5 '-trans-verschmolzenes Phosphat).
Die Fusion der Phosphatgruppe oder ihrer "Zyklation" führt zu einer Zunahme der Steifheit des Moleküls.
Wie für zyklische Amp auch gilt die glucosidische Bindung zwischen dem Guaninring und der Ribose und ihrer Rotationsfreiheit, sind wichtige Strukturparameter für die spezifische Erkennung des cyclischen GMP.
Funktionen
Im Gegensatz zu den vielfältigen und unterschiedlichen Funktionen, die andere analoge cyclische Nukleotide wie z. B. cyclischer AMP aufweisen, ist die cyclische GMP -Funktion etwas eingeschränkter:
1-teilern in Signalverfahren als Reaktion auf die Lichtstimulation von visuellen Pigmenten. Seine Konzentration wird aufgrund der Aktivierung eines G -Proteins modifiziert, das den Lichtstimulus wahrnimmt und mit einer abhängigen cyclischen GMP -Phosphodiesterase interagiert.
Veränderungen in den Nukleotidniveaus verändern sich.
2-it hat Funktionen im Zyklus der Kontraktion und der Muskelrelaxation des glatten Muskels als Reaktion auf Stickoxid und andere chemische Verbindungen verschiedener Natur.
Kann Ihnen dienen: Zelldifferenzierung3-a Die Zunahme seiner Konzentration aufgrund der Reaktion gegen natürliche Peptide hängt mit der Regulation der Bewegung von Natrium- und Wasserionen durch Zellmembranen zusammen.
4-in einige Organismen, der cyclische GMP kann durch cyclische Nukleotidphosphodiesterase mit cyclischer Amp konkurrieren.
5-Bakterien als UND. coli Sie erhöhen ihre cyclischen GMP-Spiegel, wenn sie Chemio-Atraientes ausgesetzt sind, was darauf hinweist.
6-it wurde festgestellt, dass Cyclic GMP auch wichtige Auswirkungen auf die Vasodilatations- und Erektionsprozesse bei Säugetieren hat.
7-viele-Ion-Gate-Kanäle (Calcium und Natrium) werden durch intrazelluläre Liganden reguliert, die spezifisch cyclische GMP verwenden.
Verweise
- Botsford, j. L. (1981). Zyklische Nukleotide in Prokaryoten. Mikrobiologische Bewertungen, Vier fünf(4), 620-642.
- Garrett, r., & Grisham, C. (2010). Biochemie (4. Aufl.). Boston, USA: Brooks/Cole. Cengage Lernen.
- Hardman, j., Robison, a., & Sutherland und. (1971). Zyklische Nukleotide. Jährliche Überprüfungen in Physiologie, 33, 311-336.
- Nelson, d. L., & Cox, m. M. (2009). Lehninger Prinzipien der Biochemie. Omega -Ausgaben (5. Aufl.).
- Newton, r. P., & Smith, C. J. (2004). Zyklische Nukleotide. Phytochemie, 65, 2423-2437.

