- 2099
- 280
- René Riediger
Er Heptano Es ist eine organische Verbindung, deren chemische Formel C ist7H16 und umfasst neun strukturelle Isomere, von denen das Linear der bekannteste ist. Es handelt.
Im Gegensatz zu anderen paraffinenlöslichen Lösungsmitteln hat der Heptano eine geringere Volatilität, was seine relativ sicherere Verwendung macht. Immer wenn es keine Wärmequelle gibt, die Ihre Dämpfe umgibt und sie in einer Extraktorglocke bearbeitet wird. .
 .
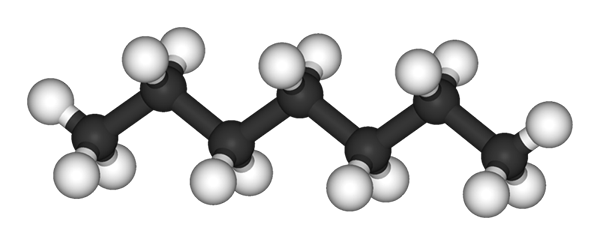
. Im oberen Bild haben Sie die Struktur der N-Heptano, das lineare Isomer aller Heptanen. N-Heptano; wenn nicht anders angegeben.
In den Flaschen dieser flüssigen Verbindung wird jedoch angegeben, dass sie enthält N-Heptano. Sie müssen in einer Extraktorglocke aufdecken und die Messungen sorgfältig durchführen.
.
[TOC]
Struktur
N-Heptan und seine intermolekularen Wechselwirkungen
N-Heptano ist linear, und aufgrund der chemischen Hybridisierung ihrer Kohlenstoffatome nimmt die Kette eine Zickzagueada -Form an. Dieses Molekül ist dynamisch, da sich seine C-C-Bindungen drehen können, wodurch die Kette in verschiedenen Winkeln leicht gefallen ist. Dies trägt zu seinen intermolekularen Wechselwirkungen bei.
Es kann Ihnen dienen: PI LinkEr N-Heptano ist ein apolares, hydrophobe Molekül, und daher basieren seine Wechselwirkungen auf den dispersiven Kräften von London; Dies sind diejenigen, die von der Molekülmasse der Verbindung und ihrer Kontaktfläche abhängen. Zwei Moleküle von N-.
Diese Wechselwirkungen sind wirksam genug, um die Moleküle von aufrechtzuerhalten N-.
Isomere
 Die neun Isomere von Heptan. Quelle: Steffen 962 [Public Domain]
Die neun Isomere von Heptan. Quelle: Steffen 962 [Public Domain] Zuerst wurde gesagt, dass die Formel c7H16 stellte insgesamt neun strukturelle Isomere dar, die die sind N-Heptane der relevanteste (1). Die anderen acht Isomere sind im oberen Bild gezeigt. Beachten Sie mit dem bloßen Auge, dass einige mehr verzweigt sind als andere.
(3): 3-methylhexan, das aus einem Paar Enantiomere (a und b) besteht
(4): 2,2-Dimethylpentano, auch bekannt als Neoheptano
(5): 2,3-Dimethylpentano, wieder mit einem Paar Enantiomeren
(6): 2,4-Dimethylpentano
(7): 3,3-Dimethylpentano
(8): 3-Ethylpentan
(9): 2,2,3-Trimethylbutane.
Jeder dieser Isomere hat unabhängige Eigenschaften und Anwendungen der N-.
Aussehen
Farblose Flüssigkeit mit einem ähnlichen Geruch wie Benzin.
Molmasse
100.205 g/mol
Schmelzpunkt
-90.549 ° C und werden zu einem molekularen Kristall.
Siedepunkt
98,38 ºC.
Dampfdruck
52,60 atm bei 20 ° C. Beachten Sie, wie hoch Ihr Dampfdruck ist, obwohl es weniger volatil ist als andere paraffinische Lösungsmittel wie Hexano und Pentan.
Dichte
3. Andererseits sind Heptano -Dämpfe 3,45 -mal dicht als Luft, was bedeutet.
Kann Ihnen dienen: Ameisensäure (HCOOH)Wasserlöslichkeit
.
Löslichkeit in anderen Lösungsmitteln
Hepthan ist mit Kohlenstoff -Tetrachlorid, Ethanol, Aceton, Ölether und Chloroform mischbar.
Brechungsindex (ND)
.
Schmiere
0,389 MPa · s
Wärmekapazität
224.64 j/k · mol
Zündungspunkt
-4 ºC
Selbstdirektionstemperatur
223 ºC
Oberflächenspannung
19,66 Mn/m A 25 ºC
Verbrennungswärme
.
Reaktivität
C7H16 + 2 => 7CO2 + 2ENTWEDER
Außerhalb der Verbrennungsreaktion ist Heptan jedoch eine ziemlich stabile Flüssigkeit. Sein mangelnder Reaktivität ist auf die Tatsache zurückzuführen, dass ihre C-H-Verbindungen schwer zu brechen sind, daher ist sie nicht anfällig für Er Substitutionen. .
Die größte Gefahr von Heptano ist durch ihre hohe Volatilität und Entflammbarkeit, daher besteht ein Brandrisiko, wenn es in heißen Standorten verschüttet wird.
Anwendungen
Lösungsmitteleinhalb der Reaktion
 Hepthan ist ein ausgezeichnetes Lösungsmittel, um Öle und Fette aufzulösen. Quelle: pxhere.
Hepthan ist ein ausgezeichnetes Lösungsmittel, um Öle und Fette aufzulösen. Quelle: pxhere. Der hydrophobe Charakter von Heptano ist ein ausgezeichnetes Lösungsmittel, um Öle und Fette aufzulösen. . Die größte Anwendung liegt jedoch darin, als Extraktorenlösungsmittel verwendet zu werden, da sie die Lipidkomponenten sowie die anderen organischen Verbindungen einer Probe auflöst.
Wenn Sie beispielsweise alle Komponenten des gemahlenen Kaffees extrahieren möchten, wird es in Heptan anstelle von Wasser mazeriert. Diese Methode und ihre Variationen wurden mit allen Arten von Samen implementiert, dank welcher Pflanzenessenzen und anderer Naturprodukte wurden erhalten.
Das Heptan, das von Natur aus farblos ist, wird aus der Farbe des extrahierten Öls gefärbt sein. Dann wird dies gedreht, um endlich ein Volumen des Öls so rein wie möglich zu haben.
Andererseits ermöglicht es Ihnen auch die geringe Reaktivität des Heptan. Als gutes Lösungsmittel für organische Verbindungen garantiert es, dass die Reagenzien in Lösung bleiben und miteinander interagieren, wenn sie reagieren.
In der Ölchemie ist es eine übliche Praxis, durch Zugabe von Heptano Asphaltenen einer rohen Probe auszurüsten. .
Oktan
Der Heptan wurde aufgrund der großen Menge an Wärme als Kraftstoff verwendet, die er anbietet, wenn er brennt. In Bezug auf Automotoren wäre es jedoch nachteilig für seinen Betrieb, wenn es nur verwendet würde. Da es sehr explosionsartig brennt, definiert es die 0 auf der Oktanzkala von Benzin.
Benzin enthält einen hohen Prozentsatz an Heptano und anderen Kohlenwasserstoffen, um Oktan auf bekannte Werte zu bewerten (91, 95, 87, 89 usw.).
Verweise
- Morrison, r. T. und Boyd, r, n. (1987). Organische Chemie. 5. Ausgabe. Editorial Addison-Wesley Interamerikaner.
- Carey f. (2008). Organische Chemie. (Sechste Ausgabe). Mc Graw Hill.
- Graham Solomons t.W., Craig b. Braten. (2011). Organische Chemie. (10. Ausgabe.). Wiley Plus.
- Wikipedia. (2020). Heptane. Abgerufen von: in.Wikipedia.Org
- Nationales Zentrum für Biotechnologie Information. (2020). Heptane Pubchem -Datenbank. CID = 8900. Erholt von: Pubchem.NCBI.NLM.NIH.Regierung
- Elsevier b.V. (2020). Heptanen. Scientedirect. Abgerufen von: Scientedirect.com
- Bell Chem Corp. (7. September 2018). Industrielle Verwendung von Heptan. Geborgen von: bellchem.com
- Andrea Kropp. (2020). Heptane: Struktur, Verwendung und Formel. Lernen. Erholt von: Studium.com
- « Kondensierte Formel Was ist und Beispiele (Methan, Ethan, Glukose ...)
- Mechanische Energieformeln, Konzept, Typen, Beispiele, Übungen »

