Ungesättigte Kohlenwasserstoffe
- 1251
- 201
- Said Ganzmann
Wir erklären, welche ungesättigten Kohlenwasserstoffe, ihre Klassifizierung, Eigenschaften, Nomenklatur und einige Beispiele geben
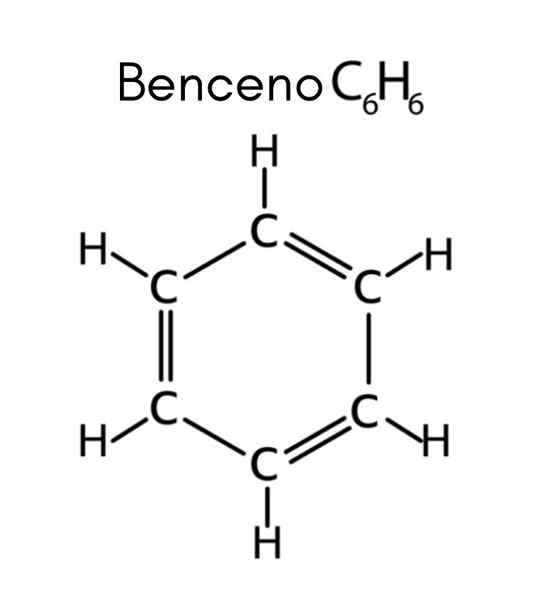
 Benzol ist ein Beispiel für ungesättigte Kohlenwasserstoff
Benzol ist ein Beispiel für ungesättigte Kohlenwasserstoff Was sind ungesättigte Kohlenwasserstoffe?
Der ungesättigte Kohlenwasserstoffe Sie sind organische Verbindungen, die nur durch Kohlenstoff und Wasserstoff gebildet werden, die eine oder mehrere mehrere Bindungen zwischen Kohlenstoffatomen haben. Dies bedeutet, dass jede Formel -C -VerbindungXHUnd Das ist ein Doppel- oder Dreifachbindung ist ein ungesättigter Kohlenwasserstoff.
Ungesättigte Kohlenwasserstoffe werden durch Alkene und Alkine sowie aromatische Verbindungen gebildet. Der Grund, warum sie ungesättigt sind.
Ungesättigte Kohlenwasserstoffe werden durch weniger als 2n+2 -Wasserstoffe (was die maximale Anzahl von Wasserstücken, die Kohlenstoff sein können) erkannt, wobei n die Anzahl der Kohlenstoffatome in der molekularen Formel ist.
Ein Beispiel für ungesättigte Kohlenwasserstoff ist der Buten, dessen molekulare Formel c ist4H8. Die maximale Anzahl von Wasserstoffen für 4 Karbons wäre 2 (4) +2 = 10 Hydringen. Dies entspricht der Anzahl der Wasserdauer eines gesättigten Kohlenwasserstoffs. Da der Buten nur 8 Wasserstoffe hat, was weniger als 10 ist, ist es ein ungesättigter Kohlenwasserstoff.
Die Anzahl der Ungesättigungen
Ungesättigte Kohlenwasserstoffe sind durch die Anzahl der Ungesättigungen gekennzeichnet. Dies zeigt an, dass die Anzahl der Wasserstoffpaare weniger als ein ungesättigter Kohlenwasserstoff mit einer gesättigten, die die gleiche Anzahl von Kohlenstoff besitzt.
Die Anzahl der Unsättigungen kann für jede ungesättigte Verbindung mittels der folgenden Formel berechnet werden:
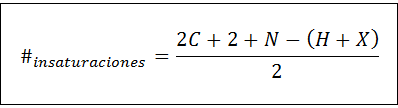
Wobei C, N, H und X die Anzahl der Kohlenstoffe, Nitrogene, Hydrogene und Halogene in der molekularen Formel darstellen. Diese Zahl gibt uns eine Vorstellung davon, wie viele Doppel- oder Dreifachbindungen eine Verbindung haben, angesichts ihrer molekularen Formel, obwohl darauf geachtet werden muss, dass Zyklen (die keine Ungesättigung sind) auch zur Anzahl der Ungesättigungen beitragen:

Beispiel
Benzol hat Formel C6H6, Die Anzahl der Unsättigung ist also:
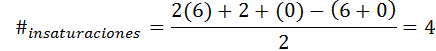
In diesem Fall entspricht die 4 Unsättigung drei Doppelverbindungen und einem Zyklus.
Klassifizierung ungesättigter Kohlenwasserstoffe
Gemäß der Art des Kohlenwasserstoffs
- Alkene: Sie sind diejenigen, die mindestens eine Doppelverbindung in ihrer Struktur haben.
- Alkine: Sie sind diejenigen, die mindestens eine dreifache Verbindung in ihrer Struktur haben.
- Aromatisch: Es handelt sich.
Nach der Kohlenstoffkette
- Linear: ungesättigte Verbindungen, bei denen alle Kohlenstoffatome in einer einzelnen Kette miteinander verbunden sind.
- Verzweigt: Sie sind diejenigen, die eine Hauptkette und auch mehrere Seitenketten haben, die Auswirkungen auffordern.
- Zyklisch: Sie sind solche, in denen ein geschlossener Zyklus von Kohlenstoffatomen vorgestellt wird, bei dem mindestens eine Doppel- oder Dreifachbindung vorgestellt wird (Cycloalquenos, Cycloalquinos und aromatisch).
Gemäß der Anzahl der Unsättigung
- Monoons 'ungesättigt: Wenn sie nur einen mehrfachen Link haben, ist es eine einzige Doppelbindung oder ein einzelner Triple -Link.
- Polynsättigiert: Wenn die Struktur mehr als ein mehrfaches Link hat, wie im Fall von Alkian, Alkian, Alkeninen usw.
Eigenschaften ungesättigter Kohlenwasserstoffe
Die Eigenschaften ungesättigter Kohlenwasserstoffe hängen stark von der jeweiligen Art des fraglichen Kohlenwasserstoffs ab:
Fusion und Siedepunkte
Im Allgemeinen haben ungesättigte Kohlenwasserstoffe niedrige Fusions- und Siedepunkte. Im Vergleich zu Alkanen haben Alkene mit der gleichen Anzahl von Kohlenstücken und einer ähnlichen Hauptkette normalerweise einen niedrigeren Siedepunkt, während Alkine tendenziell größere Siedepunkte aufweisen.
Gleiches gilt für Fusionspunkte. In der folgenden Tabelle ist ersichtlich, dass sowohl der Fusionspunkt als auch das Kochen von 1-Penten niedriger sind als die des Pentan.

Körperlicher Status
Aufgrund seiner niedrigen Schmelz- und Siedepunkte sind ungesättigte niedrig molekulare Kohlenwasserstoffe bei Raumtemperatur tendenziell gasförmig. Viele sind auch flüssig und diejenigen mit größerem Molekulargewicht sind fest. In vielen Fällen sind Feststoffe amorphe Feststoffe statt kristalliner.
Polarität
Alle Kohlenwasserstoffe, einschließlich ungesättigter, sind apolare Verbindungen, da Kohlenstoffelektronegativität und Wasserstoff sehr ähnlich sind. Die einzige Ausnahme ist bei terminalen Alkinen2 und sp3.
Löslichkeit
Apolare, ungesättigte Kohlenwasserstoffe sind in Wasser und anderen polaren Lösungsmitteln unlöslich, aber sie sind in apolaren Lösungsmitteln wie Kohlenstofftetrachlor, Cyclohexan und anderen sehr löslich. Tatsächlich sind viele dieser Verbindungen an sich apolare Lösungsmittel.
Es kann Ihnen dienen: Disposio: Struktur, Eigenschaften, erhalten, verwendet, verwendetSie sind Kraftstoffe
Ein Merkmal aller Kohlenwasserstoffe, einschließlich ungesättigter, ist, dass sie in Gegenwart von Sauerstoff verbrennen, um Kohlendioxid und Wasser freizusetzen, in Form von Licht und Wärme.
Sie können polymerisieren
Durch verschiedene chemische Reaktionen können Alkene und Alkine sich gegenseitig zusammenschließen, um Polymere wie im Fall von Polyethylen und Polypropylen zu bilden, um nur einige zu erwähnen. So sind ungesättigte Kohlenwasserstoffe das Ausgangsmaterial vieler häufiger Kunststoffe.
Chemische Reaktivität
Die Reaktivität hängt stark von der Art der funktionellen Gruppe ab, die ein Molekül hat. Bei Alkenen und Alkinen sind diese normalerweise sehr reaktiv und können Reaktionen auf Hydrierung, Hydratation, Hydrohalogenierung und andere Arten von Additionsreaktionen leiden.
Andererseits sind aromatische Verbindungen normalerweise ziemlich inert, weil sie sehr stabil sind. Die charakteristischen Reaktionen dieser Verbindungen sind die aromatischen elektrophilen Substitutionsreaktionen.
Nomenklatur ungesättigter Kohlenwasserstoffe
Nomenklatur von Alkenen
Lineare Alkene
Der Name der linearen Alkene wird durch Platzieren eines Präfixes erstellt, das die Anzahl der Kohlenstoffatome in der Kette anzeigt, gefolgt vom Kohlenstoff -Locator, bei dem die separate Doppelbindung mit Skripten aus dem Rest des Namens beginnt und mit dem Suffix _eno fertig ist:
Präfix-Localizer
- Beispiel:
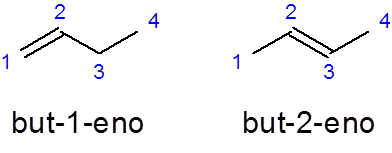
Er Aber -1 -no Es ist der Name des linearen Butens mit einer Doppelbindung im ersten Kohlenstoff, während der Aber 2-neun Es hat die Doppelbindung im zweiten Kohlenstoff.
Verzweigte Alkene
Bei verzweigten Alkenen wird die längste Hauptkette mit beiden Doppelbindungskohlenstücken zuerst ausgewählt, und die Priorität der Doppelbindung ist nummeriert. Der Name wird zuerst erstellt, indem die Auswirkungen in alphabetischer Reihenfolge vorgesehen sind, die den Lokatoren vorangegangen sind, gefolgt vom Namen der Hauptkette, wie oben angegeben.
- Beispiel:
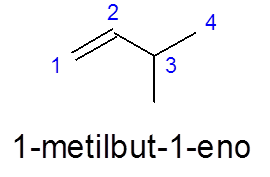
Im 3-Methylbut-1 -en erfolgt die Nummerierung von links nach rechts, um der Doppelbindung Priorität zu geben, anstatt der Verzweigung Priorität zu geben (die Methylgruppe).
Polyene
Im Fall von polyunschöpften oder polienischen Alkenen, die mehr als eine Doppelbindung enthalten, wird die größtmögliche Anzahl von Doppelbindungen als Hauptkette ausgewählt, unabhängig davon, ob es andere längere Ketten gibt.
Im Namen der Hauptkette wird ein Locator für jede Doppelbindung und das Präfix DI, Tri, Tetra usw. hinzugefügt. vor der Beendigung -eno, um die Anzahl der doppelten Links anzugeben, die Sie haben.
- Beispiel:
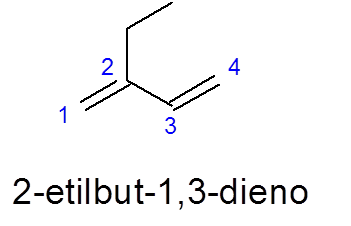
In diesem Fall beachten.
Nomenklatur der Alquinos
Die Alkine werden den Alkenen sehr ähnlich genannt, wobei der einzige Unterschied, den der Name in -ino anstelle von -eno endet. In Fällen, in denen mehr als eine dreifache Verbindung vorhanden ist.
- Beispiel:
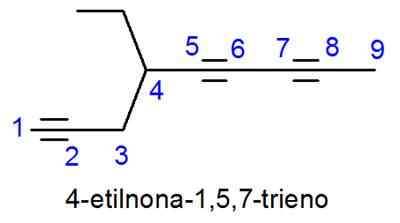
Nomenklatur von aromatischen Verbindungen
Aromatische Kohlenwasserstoffe werden als Benzolderivate ernannt, und sowohl die Nummerierung als auch die Art und Weise, sie zu benennen, hängt davon ab, wie viele Substituenten der Ring hat.
Aromatische Ringe mit einem einzigen Substituenten
In diesem Fall ist es nicht notwendig. Der Name besteht aus dem Namen des Zweigs, gefolgt vom Wort Benzol.
- Beispiel:
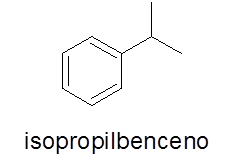
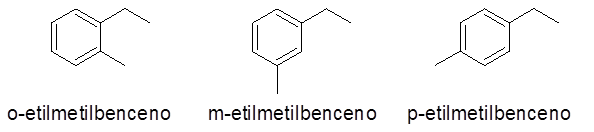
Aromatische Ringe mit zwei Substituenten
In diesem Fall können 3 Zahlen oder Ersatzmuster angegeben werden (1,2), (1,3) und (1,4). Da es gleichgültig ist, anzugeben, welcher Ersatz in Kohlenstoff 1 ist und welche in den anderen ortho-Präfixen (O-), Meta- (M-) bzw. Para- (p-) sich auf dieselbe beziehen.
- Beispiele:
Aromatische Ringe mit mehr als 2 Substituenten
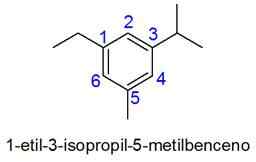
In diesem Fall wird die Nummerierung der kleinsten Kombination von Lokatoren ausgewählt. Wenn zwei Zahlen gleich sind, wird der Substituenten gemäß der alphabetischen Reihenfolge die Substituenten vor Priorität gegeben.
- Beispiele:
Beispiele für ungesättigte Kohlenwasserstoffe
Als nächstes werden zusätzliche Beispiele für ungesättigte Kohlenwasserstoffe den bereits erwähnten vorgestellt.
Acetylen (c2H2)
Acetylen ist der gebräuchliche Name des Etino, des einfachsten Alchemins. Diese Verbindung hat aufgrund ihres dreifachen Glieds 2 Ungesättigte und wird unter anderem in der Stahl- und Schweißgeräte verwendet.
Cyclohexen (c6H10)
6 -Kohlenstoff -zyklisches Alken mit zwei Ungesättigungen: eine aufgrund des Zyklus und der andere aufgrund der Doppelbindung.
Dehnung (c8H8)
Diese Verbindung wird üblicherweise bei der Herstellung von Polymeren verwendet. Es ist ein aromatisches Alken mit 5 Unsättigung.

