Kupferhydroxid (ii) Struktur, Eigenschaften, Nomenklatur, verwendet

- 4131
- 272
- Luca Holdt
Er Kupferhydroxid (II) o Cupric Hydroxid ist ein grünlichblau oder blau kristalliner anorganischer Feststoff, dessen chemische Formel Cu (OH) ist2. Es wird als blauer voluminöser Niederschlag erhalten, indem Cupric -Lösungen ein alkalisches Hydroxid hinzugefügt werden (dies bedeutet, dass sie Ionen cu enthalten2+). Es ist eine instabile Verbindung.
Um seine Stabilität zu erhöhen, wird es in Gegenwart von Ammoniak (NH3) oder Phosphate.Wenn Sie sich in Gegenwart von Ammoniak vorbereiten, gibt es ein Material mit guter Stabilität und großer Partikelgröße.
 Cupric Hydroxid Probe, CU (OH)2. Samzane in italienischer Wikipedia [Public Domain] Quelle: Wikipedia Commons
Cupric Hydroxid Probe, CU (OH)2. Samzane in italienischer Wikipedia [Public Domain] Quelle: Wikipedia Commons Bei der Vorbereitung mit Kupferphosphat (II), Cu3(Po4)2, Eine feinere Partikelgröße und eine größere Oberfläche werden erhalten. CUPRIC -Hydroxid wird in der Landwirtschaft und zur Behandlung von Holz häufig als Fungizid und Bakterizid eingesetzt, wodurch seine Nutzungsdauer verlängert wird.
Es wird auch als Tierfutter -Ergänzung verwendet. Es wird als Rohstoff verwendet, um andere Kupfer (ii) Salze und in Galvanoplastik zu erhalten, um Oberflächen abzudecken.
Studien werden durchgeführt, um ihr Potenzial zur Bekämpfung von Bakterien- und Pilzinfektionen beim Menschen abzuschätzen.
[TOC]
Struktur
Kupferhydroxid (ii) enthält unendliche Kupferionen (Cu2+) United für Hydroxylgruppen (OH-).
Die Ketten sind so verpackt, dass 2 Sauerstoffatome aus anderen Ketten über und unter jedem Kupferatom liegen und dann eine verzerrte oktaedrische Konfiguration annehmen, die in den meisten Kupferverbindungen üblich ist (ii).
In seiner Struktur befinden sich vier Sauerstoffatome in einer Entfernung von 1,93 a; Zwei Sauerstoffatome sind 2,63 a; Und die Cu-Cu-Entfernung beträgt 2,95 bis.
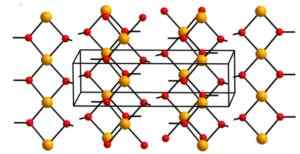 Kristalline Struktur des Cupric -Hydroxids. Aleksandar Kondinski [CC BY-SA.0 (https: // creativecommons.Org/lizenzen/by-sa/4.0)]]. Quelle: Wikipedia Commons
Kristalline Struktur des Cupric -Hydroxids. Aleksandar Kondinski [CC BY-SA.0 (https: // creativecommons.Org/lizenzen/by-sa/4.0)]]. Quelle: Wikipedia Commons Nomenklatur
- Kupferhydroxid (II).
- CUPRIC HYDROXID.
- Kupfer Dihydroxid.
Eigenschaften
Körperlicher Status
Kristalline Feststoff.
Molekulargewicht
99,58 g/mol.
Schmelzpunkt
Es bricht zusammen, bevor es schmilzt. Abbaupunkt 229 ºC.
Kann Ihnen dienen: 25 Beispiele für Löslichkeit im AlltagDichte
3,37 g/cm3
Löslichkeit
Es ist praktisch unlöslich in Wasser: 2,9 Mikrogramm/l a 25 ºC. Schnell löslich in Säuren, in konzentrierten alkalischen Lösungen und Ammoniumhydroxid. Unlöslich in organischen Lösungsmitteln. In heißem Wasser zersetzt es, was Kupferoxid (II) erzeugt, was stabiler ist.
Andere Eigenschaften
Es ist leicht löslich in starken Säuren und auch in alkalisch -konzentrierten Lösungen von Hydroxiden, um tiefe blaue Anionen zu ergeben, wahrscheinlich den Typ [CuN(OH)2n+2]2-.
Die Stabilität hängt von der Vorbereitungsmethode ab.
Es kann abgebaut werden, indem Kupferoxid (ii) schwarz (cuo) verleiht, wenn es einige Tage oder eine niedrige Erwärmung in Ruhe bleibt.
In Gegenwart eines Alkali -Überschusses bricht über 50 ° C ab.
Anwendungen
In der Landwirtschaft
Kupferhydroxid (ii) hat eine breite Anwendung als Fungizid und antibakteriell in landwirtschaftlichen Pflanzen. Hier sind einige Beispiele:
- Es dient gegen bakterielle Flecken ( Erwinia) In Salat als Blattbehandlung anwenden.
- Gegen Bakterienflecken (von Xanthomonas Pruni) In Pfirsichen, für die eine latente und Blattbehandlung angewendet wird.
- Es wird gegen das Blatt und den Stamm der Blaubeeren durch latente Anwendungen verwendet.
- Gegen Fäulnis während der Lagerung der Blaubeeren durch verursacht durch Monilinia oxycocci, durch latente Anwendung.
Für die Anwendung in der Landwirtschaft wird Kupferhydroxid (II) verwendet, das in Gegenwart von Phosphaten aufgrund seiner geringen Partikelgröße hergestellt wird.
 Salatanbau. Quelle: Pixabay
Salatanbau. Quelle: Pixabay In der Erhaltung von Holz
Holz ist aufgrund der organischen Natur empfindlich gegenüber dem Angriff von Insekten und Mikroorganismen. Kupferhydroxid (II) wird als Biozid für Pilze verwendet, die Holz angreifen.
Es wird normalerweise neben einer quaternären Ammoniumverbindung (NH4+). Kupferhydroxid fungiert als Fungizid und die quaternäre Ammoniumverbindung wirkt als Insektizid.
Auf diese Weise kann behandeltes Holz den Servicebedingungen ertragen oder widersteht, was das erforderliche Leistungsniveau des Benutzers erreicht hat. Das mit diesen Verbindungen behandelte Holz hat jedoch ein hohes Kupfergehalt und ist für gemeinsame Stahl sehr korrosiv, sodass eine Art Edelstahl erforderlich ist, der die Verarbeitung von behandeltem Holz ertragen kann.
Kann Ihnen dienen: reversible Reaktion: Eigenschaften und BeispieleTrotz seiner Nützlichkeit wird Kupferhydroxid (II) als etwas gefährlicher Biozid angesehen.
Aus diesem Grund besteht die Bedenken, dass es aus dem Holz entlassen wird, das in Mengen in Mengen behandelt wird, die für die Mikroorganismen schädlich sein können.
In Rayóns Herstellung
Seit dem neunzehnten Jahrhundert wurden ammoniale Lösungen von Kupferhydroxid (II) verwendet, um Cellulose aufzulösen. Dies ist einer der ersten Schritte, um die Faser namens Rayón durch die von Bemberg in Deutschland entwickelte Technologie zu erhalten.
Kupferhydroxid (II) löst sich in einer Ammoniaklösung (NH3), bilden ein komplexes Salz.
Die ammoniakalische Kupferlösung, die Kupferhydroxid (II) enthält, werden kurze raffinierte Baumwollfasern zugesetzt.
Baumwollcellulose bildet einen Komplex mit Tetra-Ammonium-Kupferhydroxid, der sich in der Lösung auflöst.
Anschließend ist diese Lösung Koagula beim Durchlaufen eines Extrusionsgeräts.
Aufgrund ihrer hohen Kosten wurde diese Technologie bereits von der von Viscosa überwunden. Die Technologie von Bemberg wird derzeit nur in Japan eingesetzt.
In der Tierfutterindustrie
Es wird als Spuren im Tierfutter verwendet, da es eine der Substanzen ist, die als Mikronährstoffe für die vollständige Ernährung von Tieren erforderlich sind.
 Konzentrierte Lebensmittel für Rinder. Thamizhpparithi Maari [CC BY-SA 3.0 (https: // creativecommons.Org/lizenzen/by-sa/3.0)]]. Quelle: Wikipedia Commons
Konzentrierte Lebensmittel für Rinder. Thamizhpparithi Maari [CC BY-SA 3.0 (https: // creativecommons.Org/lizenzen/by-sa/3.0)]]. Quelle: Wikipedia Commons Dies liegt daran.
Zum Beispiel ist es in dem Enzym enthalten, das an der Produktion von Kollagen und dem für die Melaninsynthese erforderlichen Enzym beteiligt ist.
Kann Ihnen dienen: AmineEs ist eine Verbindung, die allgemein als Versicherung anerkannt ist, wenn sie zu einem Niveau zugesetzt werden, der mit einer guten Nahrungsmittelpraxis übereinstimmt.
 Milchige Kühe. Quelle: Pixabay
Milchige Kühe. Quelle: Pixabay Bei der Herstellung anderer Kupferverbindungen (II)
Vorläufer aktiv in der Produktion der folgenden Kupferverbindungen (II): Kupfer (II), 2-Otylhexanoat Kupfer (II) und Kupferseifen und Kupferseifen. In diesen Fällen wird Kupferhydroxid (II) verwendet, das in Gegenwart von Ammoniak synthetisiert wird.
Andere Verwendungen
Es wird in der Nylonstabilisierung in Batterieelektroden verwendet. als Farbfixer in Färbenbetrieb; als Pigment; in Insektiziden; in Papierbehandlung und Färbung; in Katalysatoren als Katalysator bei der Vulkanisierung von Polysulfidkautschuk; als Anti -Sniffing -Pigment; und in der Elektrolyse in Galvanoplastik.
Zukünftige medizinische Anwendungen
Kupferhydroxid (II) ist Teil von Kupferverbindungen, die in Form von Nanopartikeln zur Eliminierung von Bakterien wie z UND. coli, K. Pneumoniae, p. Aeruginosa, Salmonella sppp., unter anderem Ursachen von Krankheiten im menschlichen Wesen.
Es wurde auch festgestellt, dass Kupfer -Nanopartikel dagegen wirksam sein können Candida albicans, Ein Pilz, der häufige Ursache für menschliche Pathologien ist.
Dies weist darauf hin, dass Kupfernanotechnologie eine wichtige Rolle gegen Bakterien und Pilze spielen kann, die menschliche Infektionen verursachen, und Kupferhydroxid (II) könnte in diesen Bereichen sehr nützlich sein.
Verweise
- Baumwolle, f. Albert und Wilkinson, Geoffrey. (1980). Fortgeschrittene anorganische Chemie. Vierte Edition. John Wiley & Söhne.
- Kirk-Othmer (1994). Enzyklopädie der chemischen Technologie. Band 7. Vierte Edition. John Wiley & Söhne.
- Ullmanns Enzyklopädie der industriellen Chemie. (1990). FÜNFTE AUSGABE. Band A7. VCH Verlagsgellschaft MBH.
- Tanz, j.C.; Emeléus, h.J.; Sir Ronald Nyholm und Trotman-Deckenson, um.F. (1973). Umfassende anorganische Chemie. Band 3. Pergamon Press.
- Nationalbibliothek für Medizin. (2019). Kupfer (ii) Hydroxyde. Erholt von: Pubchem.NCBI.NLM.NIH.Regierung
- Schiopu, n. und Tiruta-Brean, l. (2012). Holzkonservierungsmittel. In Toxizität von Puffermaterialien. Kapitel 6. Von Scientedirect erholt.com.
- Mordorski, geb. und Friedman zu. (2017). Metallnanopartikel für mikrobielle Infektionen. In funktionalisierten Nanomaterialien zur Behandlung von mikrobieller Infektionen. Kapitel 4. Von Scientedirect erholt.com.
- Takashi Tsurumi. (1994). Lösung drehen. In fortschrittlicher Faser -Spinntechnologie. Kapitel 3. Von Scientedirect erholt.com.
- « Histochemistry Foundation, Verarbeitung, Färbung
- Ceriooxid (iv) Struktur, Eigenschaften, verwendet »

