Strontiumhydroxid (SR (OH) ₂)

- 4069
- 47
- René Riediger
 Strontiumhydroxid
Strontiumhydroxid Was ist Strontiumhydroxid?
Er Strontiumhydroxid (Sr (OH) ₂) ist eine anorganische chemische Verbindung, die durch ein Strontiumion (SR) und zwei Hydroxidionen (OH) gebildet wird (OH). Diese Verbindung wird erhalten, indem ein Strol -Salz mit einer starken Basis kombiniert wird, was zu einer Verbindung von alkalischer Natur führt, deren chemische Formel SR (OH) ist2.
Im Allgemeinen wird zur Herstellung von Strontiumhydroxid, Natriumhydroxid (NaOH) oder Kaliumhydroxid (KOH) als starke Basis verwendet. Andererseits ist Strontiumsalz (oder Strontiumion), das mit der starken Basis reagiert3)2 Und der Prozess wird durch die folgende chemische Reaktion beschrieben:
2koh + sr (nein3)2 → 2kno3 + SR (OH)2
In Lösung das Strontium -Kation (SR+) Er setzt sich mit Hydroxidanion in Verbindung (OH-) Bildung eines grundlegenden ionischen Strontiumsalzes. Da Strontium ein alkalisches Metall ist, wird Strontiumhydroxid als ätzende Alkali -Verbindung angesehen.
Erhalten von Strontiumhydroxid
Zusätzlich zu dem zuvor erklärten Prozess kann gesagt werden, dass SR (OH), sobald die Reaktion durchgeführt wurde, nach der Ausführung der Reaktion2 Niederschlag in die Lösung. Dann wird dies dem Wasch- und Trocknungsprozess ausgesetzt, der schließlich ein sehr feines weißes Pulver erhält.
Eine alternative Methode zum Erhalten von Strontiumhydroxid ist die Erwärmung von Strontiumcarbonat (SRCO3) oder Strontiumsulfat (SRSO4) mit Dampf bei einer Temperatur zwischen 500 ° C und 600 ° C. Die chemische Reaktion tritt wie unten gezeigt auf:
SRCO3 + H2O → sr (OH)2 + CO2
SRS + 2H2O → sr (OH)2 + H2S
Kann Ihnen dienen: SchwefelsäureChemische Struktur und physikalisch -chemische Eigenschaften
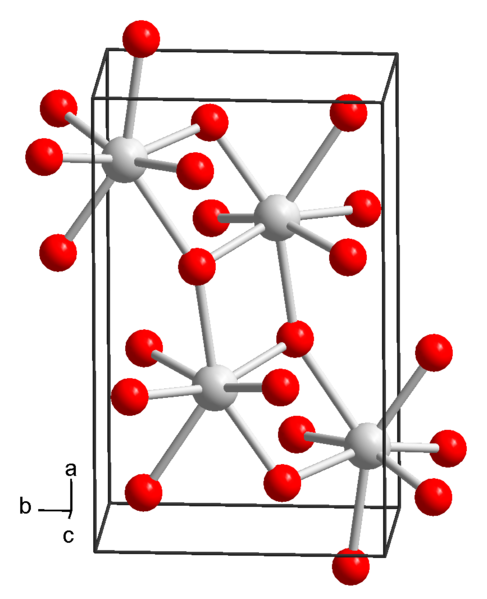 Chemische Struktur des Strontiumhydroxids. Quelle: Wikimedia Commons
Chemische Struktur des Strontiumhydroxids. Quelle: Wikimedia Commons Gegenwärtig sind 3 Formen von Strontiumhydroxid bekannt: Oktahydrat, Monohydrat und wasserfrei.
Oktoniertes Strontiumhydroxid
Aus Lösungen bei normalen Temperatur- und Druckbedingungen (25 ° C und 1 atm) fällt Strontiumhydroxid auf oktahydratische Weise aus, deren chemische Formel SR (OH) ist2∙ 8h2ENTWEDER.
Diese Verbindung hat eine Molmasse von 265,76 g/mol, eine Dichte von 1,90 g/cm und fällt als tetragonale Kristalle (mit räumlicher Gruppe p4/ncc) von quadrangulärem prismatischem Erscheinungsbild und farblos aus.
Ebenso hat das octonisierte Strontiumhydroxid die Fähigkeit, atmosphärische Feuchtigkeit zu absorbieren, da es eine leicht köstliche Verbindung ist.
Monohydratisiertes Strontiumhydroxid
Gemäß optischen Mikroskopiestudien (durchgeführt durch die X -Strahlenbeugungstechnik) durch Anheben der Temperatur auf etwa 210 ° C - ein konstanter atmosphärischer Druck - der SR (OH)2∙ 8h2O Es ist dehydriert und in monohydratisiertes Strontiumhydroxid (SR (OH) umgewandelt)2∙ h2ENTWEDER).
Diese Form der Verbindung hat eine Molmasse von 139,65 g/mol und ihre Schmelztemperatur beträgt -73,15 ° C (375 K). Aufgrund seiner Atomkonfiguration zeigt dies weniger Löslichkeit in Wasser als in seiner Okta -Formularform.
Wasserfreies Strontiumhydroxid
Durch Fortsetzung der Systemtemperatursteigerung auf etwa 480 ° C wird die Dehydration bis zu einem wasserfreien Stretchhydroxid verlängert.
Im Gegensatz zu seinen hydratisierten Formen hat es eine Molmasse von 121,63 g/mol und eine Dichte von 3,625 g/cm3. Sein Siedepunkt ist bei 710 ° C (1.310 ° F oder 983 K) erreicht, während der Schmelzpunkt bei 535 ° C (995 ° F oder 808 K) liegt.
Kann Ihnen dienen: Ididio 192Löslichkeit
Strontium octahydrathydroxid hat eine Wasserlöslichkeit von 0,91 Gramm pro 100 Milliliter (gemessen bei 0 ° C), während seine wasserfreie Form bei ähnlichen Temperaturbedingungen eine Löslichkeit von 0,41 Gramm pro 100 Milliliter aufweist.
In ähnlicher Weise wird diese Substanz in Aceton als unlöslich und in Säuren und Ammoniumchlorid völlig löslich angesehen.
Chemische Reaktivität
Strontiumhydroxid ist nicht brennbar, seine chemische Reaktivität bleibt bei mittelschweren Temperaturen und Drücken stabil und kann Kohlendioxid aus atmosphärischer Luft absorbieren und es in Strontium -Carbonat umwandeln.
Darüber hinaus ist es eine stark irritierende Verbindung, wenn Sie sich mit der Haut, dem Atemweg oder anderen Schleimhäuten in Verbindung setzen.
Strontiumhydroxid verwendet
Aufgrund seiner hygroskopischen Eigenschaften und grundlegenden Eigenschaften wird Strontiumhydroxid für verschiedene Anwendungen in der Branche verwendet:
- Moice -Extraktion und Zuckerverfeinerung aus Rüben.
- Plastikstabilisator.
- Fette und Schmiermittel.
Moice -Extraktion und Rübenzuckerverfeinerung
Zu Beginn des 21. Jahrhunderts in Deutschland wurde Stretchhydroxid für die Verfeinerung von Rüben aus Rüben durch den patentierten Prozess von Carl Scheibler im Jahr 1882 verwendet.
Dieses Verfahren besteht in der Mischung aus Strontiumhydroxid und der zuckerhaltigen Rübenzulpa, was zu einem unlöslichen Disaccharid führt. Diese Lösung wird durch Dekantation getrennt und sobald der Raffinerierungsprozess durchgeführt wird, wird Zucker als Endprodukt erhalten.
Obwohl dieses Verfahren noch angewendet wird, gibt es andere Methoden mit viel mehr Nachfrage nach billigeren, die in der überwiegenden Mehrheit der Zuckerraffinerien der Welt verwendet werden. Zum Beispiel die Barsil -Methode, die Bariumsilikat verwendet, oder die Steffen -Methode, die Lime als Extraktormittel verwendet.
Kann Ihnen dienen: anomerer Kohlenstoff: Was ist, Merkmale, BeispieleStrontiumfette
Sie sind Schmierfette, die Strontiumhydroxid enthalten. Diese sind in der Lage, sich stark an Oberflächen mit Metalleigenschaften zu halten, sind wasserfest und plötzlichen Temperaturänderungen zu unterstützen.
Aufgrund ihrer guten physikalischen und chemischen Stabilität werden diese Fette als industrielle Schmiermittel verwendet.
Plastikstabilisator
Die überwiegende Mehrheit der Kunststoffe, die klimatischen Faktoren wie Sonne, Regen und atmosphärischer Sauerstoff ausgesetzt sind, modifizieren ihre Eigenschaften und degradieren.
Aufgrund seiner beträchtlichen Wasserbeständigkeit wird diese Polymere während der Fusionsphase als Stabilisator bei der Herstellung von Kunststoffprodukten zur Verlängerung seiner Nutzungsdauer zugesetzt, da diese Polymere als Stabilisator fungieren.
Andere Apps
- In der Lackbranche wird es als wesentlicher Zusatz verwendet, um den Trocknungsprozess in kommerziellen und industriellen Gemälden zu beschleunigen.
- Aus Strontiumhydroxid werden Salz oder Strontiumionen erhalten, die als Rohstoff für die Herstellung von Pyrotechnikern Artikeln verwendet werden.
Verweise
- Wikipedia (n.D.). Strontiumhydroxid. Abgerufen von.Wikipedia.Org
- Pubchem (s.F.). Strontiumhydroxid. Aus Pubchem erhalten.NCBI.NLM.NIH.Regierung
- Honeywell (s.F.). Stontiumhydroxid Octahydrat. Aus Honeywell abgerufen.com

