Holmio

- 2055
- 84
- Rieke Scheer
 Metallic Holm Ultrapure Probe. Quelle: Hi-Res-Bilder von chemischen Elementen [CC von 3.0 (https: // creativecommons.Org/lizenzen/bis/3.0)]]
Metallic Holm Ultrapure Probe. Quelle: Hi-Res-Bilder von chemischen Elementen [CC von 3.0 (https: // creativecommons.Org/lizenzen/bis/3.0)]] Was ist der Holmio?
Er Holmio Es ist ein metallisches Element, das zum Block gehört F der Periodenkabelle, insbesondere bis zur Zeit der Lantaniden. Es ist daher ein Mitglied der Seltenen Erden neben dem Erbio, Itrio, Disposio und Iterbio. All diese bilden eine Reihe von Mineralien (Xenotima oder Gadolinita), die durch konventionelle chemische Methoden schwer zu trennen sind.
Sein chemisches Symbol ist das HO, eine atomare Anzahl von 67 und weniger reichlich als seine Nachbarn Disposio (Disposio (66Dy) und erbio (68Ähm). Es wird dann gesagt, dass Oddo-Harkins-Herrschaft folgen. Holmius ist einer dieser seltenen Metalle, die fast niemand seine Existenz kennt oder vermutet; Auch bei Chemikalien wird es normalerweise nicht sehr häufig erwähnt.
In den Gebieten der Medizin ist Holmio für die Verwendung seines Lasers in Operationen zur Bekämpfung von Prostata -Pathologien bekannt. Es repräsentiert auch das vielversprechende Material für die Herstellung von Elektromagneten und Quantencomputern aufgrund seiner ungewöhnlichen magnetischen Eigenschaften.
Holmiumverbindungen, dreifach, HO3+, Sie präsentieren die Besonderheit, eine farblich abhängige von dem Licht abzubauen, mit dem sie bestraft sind. Wenn dies fluoreszierend ist, ändert sich die Farbe dieser Verbindungen von gelb nach rosa. Ebenso passiert es mit seinen Lösungen.
Geschichte
Die Entdeckung des Holmio wird zwei Schweizer Chemikalien, Marc DeFontaine und Jacques-Louis Soret, zugeschrieben, die 1878 spektroskopisch nachgewiesen wurden, während er in Genfer Mineralien von Seltenerden analysierte. Sie nannten ihn Element x.
Nur ein Jahr später, 1879, verwaltete der schwedische Chemiker pro Teodor Cleve2ENTWEDER3). Dieses durch andere Verunreinigungen kontaminierte Oxid zeigte eine braune Färbung, die er "Holmia" nannte, was einen Schlaganfall in Latein bedeutet.
Kann Ihnen dienen: Exergonische Reaktion: Merkmale und BeispieleAußerdem erhielt Cleve ein weiteres grünes Material: 'Thulia', das zu Tuliooxid wird. Das Problem dieser Entdeckung ist, dass keiner der drei Chemikalien eine ausreichende Probe des Holmoxids erhalten kann.
Nicht. Dieses Oxid wurde anschließend chemische Reaktionen zur Herstellung von Holmiosalzen unterzogen, die 1911 vom schwedischen Chemiker Otto Holmberg reduziert wurden; Und so erschien die ersten metallischen Holm -Proben.
Derzeit die Ionen von Holmios, Hol3+, Sie werden durch Ionenaustauschchromatographie extrahiert, anstatt auf herkömmliche Reaktionen zurückzugreifen.
Holm -Eigenschaften
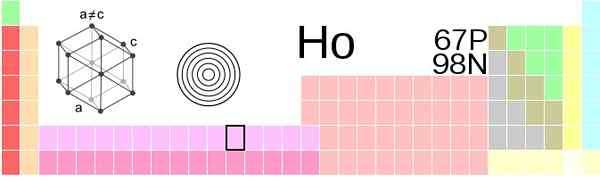 Holmio -Standort in der Periodenzüchtertabelle. Quelle: Vektorisierung: Sushant Savla 05:51, 9. Juni 2019 (UTC), CC BY-SA 4.0, über Wikimedia Commons
Holmio -Standort in der Periodenzüchtertabelle. Quelle: Vektorisierung: Sushant Savla 05:51, 9. Juni 2019 (UTC), CC BY-SA 4.0, über Wikimedia Commons Aussehen
Silber, Weich, duktile und formbares Metall.
Ordnungszahl
67 (67HO)
Molmasse
164,93 g/mol
Schmelzpunkt
1461 ºC
Siedepunkt
2600 ºC
Dichte
Bei Raumtemperatur: 8,79 g/cm3
Gerade wenn schmelzen oder schmelzen: 8,34 g/cm3
Fusionshitze
17 kJ/mol
Verdampfungswärme
251 kJ/mol
Molarenwärmekapazität
27.15 J/(mol · k)
Elektronegativität
1.23 auf der Paulingskala
Ionisationsenergien
Erstens: 581.0 kJ/mol (Ho+ gasförmig)
Zweitens: 1140 kJ/mol (Ho2+ gasförmig)
Dritter: 2204 kJ/mol (Ho3+ gasförmig)
Wärmeleitfähigkeit
16,2 w/(m · k)
Elektrischer widerstand
814 nω · m
Oxidationszahlen
Das HolM kann in seinen Verbindungen mit den folgenden Zahlen oder Oxidationszuständen dargestellt werden: 0, +1 (HO)+), +2 (Ho2+) und +3 (Ho3+). Von allen von ihnen ist +3 bei weitem das häufigste und stabilste und stabilste. Daher ist das HolM ein dreifaches Metall, das Verbindungen (ionisch oder teilweise ionisch) bildet, an denen es als Ho -Ion teilnimmt3+.
Kann Ihnen dienen: EthylacetatZum Beispiel wird in den folgenden Verbindungen das HolM mit +3 Oxidationszahl gefunden: HO2ENTWEDER3 (Ho23+ENTWEDER32-), Ho (oh)3, Hoi3 (Ho3+Yo3-) und ho2(SW4)3.
Das Ho3+ Und seine elektronischen Übergänge sind für die Verbindungen dieses Metalls verantwortlich. Wenn sie jedoch mit fluoreszierendem Licht strahlen, werden sie rosa. Gleiches gilt für ihre Lösungen.
Isotope
Holmio wird in der Natur als einzelnes stabiles Isotop dargestellt: 165HO (100% Häufigkeit). Es gibt jedoch künstliche Radioisotope mit beträchtlichen Halbzeitzeiten. Zwischen ihnen haben wir:
-163Ho (T1/2 = 4570 Jahre)
-164Ho (T1/2 = 29 Minuten)
-166Ho (T1/2 = 26.763 Stunden)
-167Ho (T1/2 = 3,1 Stunden)
Magnetische Ordnung und Moment
Das Holm ist ein paramagnetisches Metall, kann aber bei einer Temperatur von 19 K ferromagnetisch werden, was sehr starke magnetische Eigenschaften aufweist. Es ist gekennzeichnet durch das magnetische Moment (10,6 μB) größer unter allen chemischen Elementen sowie eine ungewöhnliche magnetische Durchlässigkeit.
Reaktivität
Das Holm ist ein Metall, das unter normalen Bedingungen nicht zu schnell ist, so dass es braucht, um seine Helligkeit zu verlieren. Wenn er jedoch mit einem Leichter erhitzt wird, wird es gelblich, Produkt der Bildung einer Oxidschicht:
4 Ho + 3 o2 → 2 Ho2ENTWEDER3
Reagiert mit verdünnten oder konzentrierten Säuren, um ihre jeweiligen Salze zu verursachen (Nitrate, Sulfate usw.). Und überraschenderweise reagiert es jedoch nicht mit Fluorhorsäure, da eine HoF -Schicht3 schützt es vor seiner Verschlechterung.
Das Holmio reagiert auch mit allen Halogenen, um ihre jeweiligen Halogenuros zu produzieren (HoF3, Hocl3, Hobr3 und hoi3).
Chemische Struktur
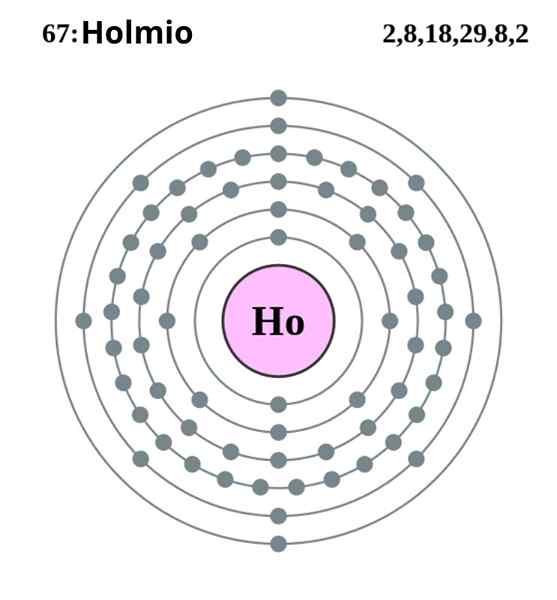 Holmio Electronic Configuration. Quelle: Pumba (Originalarbeit von Greg Robson) Creative Commons Recognition-Share unter derselben Lizenz 2.0 England und Land Wales
Holmio Electronic Configuration. Quelle: Pumba (Originalarbeit von Greg Robson) Creative Commons Recognition-Share unter derselben Lizenz 2.0 England und Land Wales Der Holmio kristallisiert in einer kompakten hexagonalen Struktur, HCP (für sein Akronym in Englisch: Close-Packed Hexagonal). Theoretisch bleiben HO -Atome dank der Metallbindung, die durch die Elektronen ihrer 4F -Orbitale gebildet wird, gemäß ihrer elektronischen Konfiguration zusammen
Kann Ihnen dienen: Verdünnung: Konzept, wie es gemacht wird, Beispiele, Übungen[Xe] 4felf 6s2
Solche Wechselwirkungen sowie das Energiesystem seiner Elektronen definieren die physikalischen Eigenschaften des Holmio. Dieses Metall ist kein anderes Alotrope oder Polymorph bekannt, auch unter hohen Drücken.
Anwendungen
Kernreaktionen
Das Holmio -Atom ist ein guter Neutronenabsorption.
Spektroskopie
Holmiooxidlösungen werden verwendet, um Spektrophotometer zu kalibrieren. Es zeigt auch sehr charakteristische akute Banden, die mit dem Holmio -Atom assoziiert sind, und nicht mit seinen Verbindungen.
Farbton
Holmio -Atome sind in der Lage, Glas und künstlichen Edelsteinen des Kubikumfangs rötliche Farben zu verleihen.
Magnete
Bei extrem niedrigen Temperaturen (30 K oder weniger) weist der Holmius interessante magnetische Eigenschaften auf.
Solche magnetischen Materialien sind für die nukleare Magnetresonanz bestimmt. für die Entwicklung von Festplatten mit Erinnerungen, die in der Reihenfolge der Petabyte oder Terabyte schwingen; und möglicherweise Quantencomputer herzustellen.
Holmio Laser
Ein Ititrio-Aluminium-Granatkristall (YAG) kann mit Holmio-Atomen dotieren, um eine Strahlung zu emittieren, deren Wellenlänge 2 μm beträgt; Das heißt, wir haben einen Holm -Laser. Dank ihm kann Tumorgewebe genau geschnitten werden, ohne Blutungen zu verursachen, da die Energie die Wunden sofort entlastet hat.
Dieser Laser wurde derzeit in Prostata- und Zahnarztpraxen sowie zur Beseitigung von Krebszellen und Nierensteinen eingesetzt.

