Trägheit chemische Trägheit

- 3676
- 1142
- Ibrahim Steuk
Was ist chemische Trägheit?
Chemische Trägheit ist die Eigenschaft, die einen Substanz oder ein Material hat, um dem durch externen Mittel verursachten Verschlechterungen standzuhalten. In diesem Sinne bleiben seine physikalischen Eigenschaften und insbesondere die Chemikalien unverändert. Es gibt keine Link -Pausen oder die Bildung neuer.
Jetzt ist chemische Trägheit relativ. Einige Substanzen oder Materialien sind stärker als andere, was auf die Art und Stärke ihrer Wechselwirkungen zurückzuführen ist. Wie es im Prinzip die Phänomene des Wandels kontrastieren konnte, unverzichtbar, damit sich die Materie in verschiedenen Produkten weiterentwickelt, um sich weiterzuentwickeln.
 Ein goldener Blick. Gold ist korrosion resistenteres Metall
Ein goldener Blick. Gold ist korrosion resistenteres Metall Aus diesem Grund wird es immer in der Lage, dass es sich um eine Substanz oder ein Material handelt, es wird immer eine Erkrankung geben, unter der es reaktiv wird. Zum Beispiel ist Gold der edelste Metalle und wird als inert angesehen. Es wird jedoch durch königliches Wasser angegriffen und gelöst, eine Lösung, für die es sehr reaktiv ist.
Vielleicht und bis heute ist das einzige chemische Element, das eine absolute chemische Trägheit gezeigt hat, das Neon. Es ist keine Verbindung bekannt, nicht einmal unter ultramierenden Bedingungen, wie beispielsweise in den Kernen der Planeten oder Monde.
Eigenschaften der chemischen Trägheit
Mangel an Oxidation
Damit ein Material oder eine Substanz in den Prinzip inert sind, sollte es nicht mit der umgebenden Luft reagieren. Dies bedeutet, dass es keine Verbindungen mit Sauerstoff- oder Stickstoffmolekülen bildet, die seine Oberfläche umgeben. Mit anderen Worten: Oxidieren Sie die Luftbelastung nicht.
Lebensmittel und alle fraglichen organischen Substanzen tendieren dazu, zu oxidieren. Es wird daher gesagt, dass sie nicht träge sind.
Mangel an Oxidation bei chemischen Trägheit sollte bei Temperaturen von mehr als 100 ° C gehalten werden. Je höher die Temperatur, die Substanzen oder Materialien werden schneller oxidieren und mit dem Sauerstoff oder dem Stickstoff der Luft reagieren, um Oxide bzw. Nituros zu bilden.
Säurebeständigkeit oder Alkalis
Ein weiteres Merkmal bei chemischer Trägheit ist die Resistenz gegen Säuren oder Basen. Dies bedeutet, dass eine inerte Substanz oder ein inerter Material dem Angriff von Säuren widerstehen sollte, ohne dass sich die Akzeptanz von H -Ionen verschlechtern+ oder sehr starke Elektrophile; oder der Angriff der Basen, ohne sich wegen der OH -Ionen zu verschlechtern-.
Es kann Ihnen dienen: Perbromensäure (Hbro4): Eigenschaften, Risiken und VerwendungAuch dies ist relativ, da es verschiedene Arten von Säuren und Basen gibt. Einige inerte Substanzen können sehr resistent gegen Schwefelsäure sein, aber sie werden anstelle des unteren Tropfens von Fluorhoridsäure abgebaut. Dies ist der Fall von Glasflaschen, wenn sie mit HF reagieren.
Elektronische Stabilität
Die obigen Eigenschaften haben mit der thermodynamischen Stabilität zu tun, die sich aus der Natur intermolekularer Wechselwirkungen sowie anderen Faktoren ergibt. Andererseits wird die chemische Trägheit auch in den elektronischen Eigenschaften derselben Atome erscheint.
Je stabiler die elektronische Konfiguration eines Atoms ist, desto niedriger ist seine Tendenz, Elektronen zu gewinnen oder zu verlieren. Daher wird es eine größere Trägheit chemische Trägheit aufweisen. Dies ist der Fall von edlen Gasen, die im nächsten Abschnitt zu sehen sind.
Bioinaktivität
In der Medizin ist eine Substanz oder ein Material inert, wenn es keine Bioaktivität gibt. Das heißt, es kann sich in einem Organismus befinden, ohne während seines Stoffwechsels assimiliert zu werden. Dieses Merkmal ist in Knochenprothesen oder bei Geweberekonstruktion sehr wünschenswert.
Strahlungswiderstand
Schließlich sollten inerte Substanzen oder Materialien auch gegen Strahlung resistent sein, ultraviolett oder nuklear sein.
Beispiele für chemische Trägheit
Glas
 Glas ist ein relativ inertes Material
Glas ist ein relativ inertes Material Unter den Beispielen für Materialien, die chemische Trägheit aufweisen, haben wir das Glas. Wenn sie nicht träge wären, würden sie nicht für die Ausarbeitung von Behältern oder Behältern dienen, da sie mit ihrem Inhalt reagieren würden. Abhängig von ihrer Zusammensetzung wie Borosilikat können sie sehr resistent gegen Korrosion und Temperatur werden.
Wie zu Beginn erwähnt, ist Glas jedoch nicht gegen alle Substanzen immun: Es reagiert mit dem HF, sogar verdünnt, heiße Alkalis wie Naoh und H3Po4 Sehr konzentriert und heiß.
Kann Ihnen dienen: PyrolyseKunststoff
 Wenn Teflons Pfanne nicht träge wäre, würde sie alle Lebensmittel verderben, die wir darin gekocht haben. Quelle: Mdevicente, CC0, über Wikimedia Commons
Wenn Teflons Pfanne nicht träge wäre, würde sie alle Lebensmittel verderben, die wir darin gekocht haben. Quelle: Mdevicente, CC0, über Wikimedia Commons Kunststoffe erfüllen auch Funktionen, die denen von Glas ähneln, aber es gibt viel mehr vielseitige (sie brechen nicht so leicht). Einige Kunststoff wie Teflon (Polytetrafluorethylen), Kynar (Polyvinylidenfluorid) und Telen (Polydiccyclopentadien) sind extrem resistent gegen den Angriff von Säuren und Korrosion.
Keramik
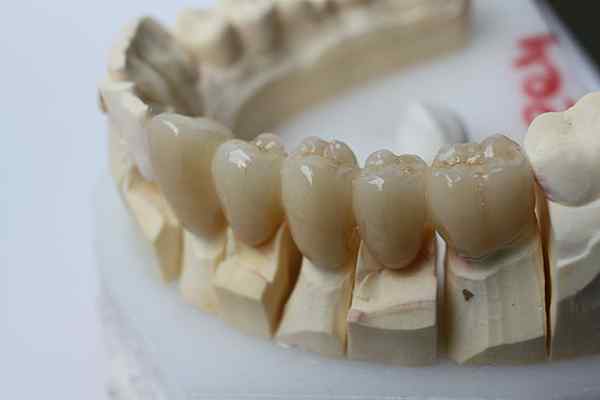 Die chemische Trägheit der Zirkonia ermöglicht es, für Zahnprothesen verwendet zu werden. Quelle: bin im Garten über Wikipedia.
Die chemische Trägheit der Zirkonia ermöglicht es, für Zahnprothesen verwendet zu werden. Quelle: bin im Garten über Wikipedia. Die inerte Keramik geht einen Schritt weiter als Kunststoff. Sie sind für Anwendungen gedacht, bei denen hohe Temperaturen vorherrschen, was in der Automobil- und Luft- und Raumfahrtindustrie üblich ist. oder in biochemischen Systemen, wie in der pharmazeutischen Industrie und in der Umsetzung von Knochenprothesen.
Unter einigen dieser Keramik mit großer chemischer Trägheit haben wir: Aluminiumoxid (zu2ENTWEDER3, Anwesend im Corindon und Saphir), The Silicates (Spezialglas), Siliciumcarbid (sic, hart und hartnäckig) und Zirkonia (Zio2).
Inertgase
Wenn wir die inerten Materialien beiseite lassen, haben wir jetzt inerte Substanzen. Inerte Gase sind nicht sehr reaktiv, so dass ihre Anwesenheit in der Luft kein Reaktionsrisiko unter normalen Bedingungen impliziert.
Unter diesen Gasen haben wir den CO2, Co und n2. Stickstoff ist der inerteste aller dieser Gase; Und doch kann er mit einigen Metallen heiß reagieren, um Nituros zu bilden, m3NN, Sein N Valencia- oder Metalloxidationszustand.
Die co2 Es ist relativ inert; Außer wenn es auf alkalische Lösungen trifft, wo es in Carbonate oder in Gegenwart von Kohleanhydraic -Enzymen umgewandelt wird.
Der CO bleibt bei Raumtemperatur inert; Bei hohen Temperaturen reagiert es jedoch unter anderem mit Kohle, Wasserdampf, Metalloxiden, Olefinen.
Kann Ihnen dienen: Chemisches Gleichgewicht: Erklärung, Faktoren, Typen, BeispieleSolche Reaktionen können in Gegenwart von Metallkatalysatoren fortgesetzt werden. Ebenso kann CO auch ohne seine kovalenten Bindungen zu neutralen Metallatomen koordinieren.
Edle Metalle
Edelmetalle sind am beständigsten gegen Korrosion und Angriff von Säuren und Alkalien. Jedes bei hohen Temperaturen oder im Staubformat reagiert mit Sauerstoff oder Fluorid. Daher ist die chemische Trägheit dieser Elemente ziemlich relativ.
Unter den edlen Metallen, die wir haben: Gold (AU), Ruthenio (Ru), Platinum (PT), Paladio (PD), Osmio (OS) und Iridido (Ir). Von allen von ihnen ist Gold das edelste, auch in einem metallischen Zustand in der Erdkruste zu sein.
Edelgase
Und schließlich haben wir auf dem höchsten Sitz der chemischen Trägheit edle Gase: Helium (He), Neon (NE), Argon (AR), Crypton (KR), Xenon (XE) und Radon (RN). Alle von ihnen sind extrem träge. Viele Verbindungen des Xenon wurden jedoch synthetisiert, einschließlich Salze, die als Perxenatos bekannt sind, mit dem Xeo -Anion64-.
 Neonlichter entsprechen den inertesten chemischen Elementen der Natur
Neonlichter entsprechen den inertesten chemischen Elementen der Natur Seine chemische Trägheit liegt daran, dass ihre Atome ihre Energie und Umlaufschichten voll von Elektronen enthalten. Aus dem Argon ist es möglich, dass sie unter Ulträume mit leeren Orbital- oder mehr Energieschichten (zum Beispiel 3D und 4S) zu Zugang zu Elektronen zugreifen. Ding, das für Helium oder Neon unmöglich ist.
Genaue Gase genau Helium und Neon sind am inertesten. Das Helium kann Verbindungen mit Natrium bis sehr hoher Drücke bilden (Hena).
In der Zwischenzeit ist überhaupt keine Verbindung bekannt, die aufgrund seiner größeren wirksamen Kernbelastung noch inerter ist als Helium.
Verweise
- Whitten, Davis, Peck & Stanley. (2008). Chemie. (8. Aufl.). Cengage Lernen.
- Shiver & Atkins. (2008). Inorgán ChemieICA. (Vierte Edition). Mc Graw Hill.
- Wikipedia. (2020). Chemisch inert. Abgerufen von: in.Wikipedia.Org
- DR. Doug Stewart. (2020). Definition von Inert. Erholt von: Chemicoolool.com
- Elsevier b.V. (2020). Chemische Trägheit. Scientedirect. Abgerufen von: Scientedirect.com
- Clara Moskowitz. (20. März 2018). Eine edle Gasüberraschung: Helium kann seltsame Verbindungen bilden. Erholt von: Scientific American.com
- Coorstek. (2020). Chemische Eigenschaften der technischen Keramik. Erholt von: Coorstek.com
- Osborne Industries. (2020). Die 3 säurebeständigen Kunststoffe. Erholt von: Osbornindustries.com

