Isoprenostruktur, Eigenschaften, Anwendungen
- 2851
- 64
- Medine Kedzierski
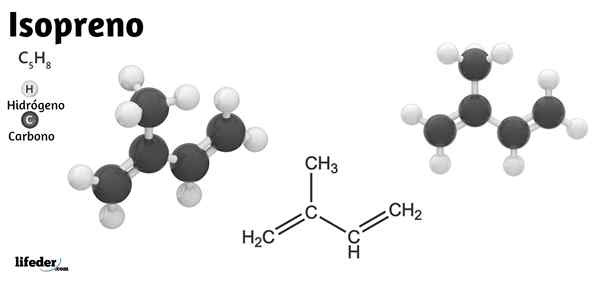
Er Isopren oder 2-Methyl-1,3-Butadien ist eine organische Verbindung, die aus einem Kohlenwasserstoff besteht, dessen molekulare Formel C ist5H8. Trotz seiner offensichtlichen Einfachheit stellt es die strukturelle Grundlage von Naturkautschuk und vor allem das Skelett der biologischen Einheiten dar, mit denen Isoprenoide oder Terpene enzymatisch synthetisiert werden.
Daher hält das Isopren die Bedeutung nicht nur in der organischen Chemie, sondern auch in der Biochemie. Im unteren Bild ist seine strukturelle Formel zu sehen, die linear als Cho abgebaut werden kann2= C (ch (ch)3) −ch = cho2. Aus dieser Formel wird verstanden, warum sein Name IUPAC 2-Methyl-1,3-Butadien ist, da sich die beiden Doppelbindungen in Carbons 1 und 3 befinden.
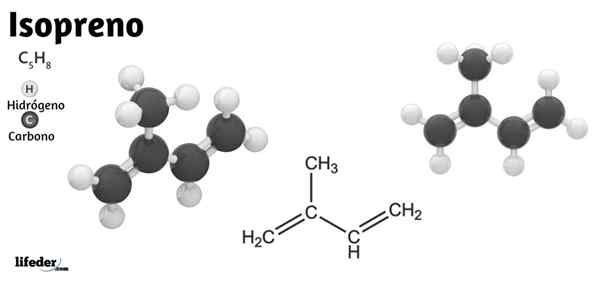
Isopren ist ein wesentlich häufiger Kohlenwasserstoff in der Umwelt. Pflanzen, Algen, Bakterien und Tiere können sie synthetisieren und ausgeben und sogar den am häufigsten vorkommenden Teil unserer Ausatmen bilden. Gemüsemassen sind die Hauptproduzenten und Isoprenemitter, die sie in Mechanismen verwenden, um der äußeren Hitze standzuhalten.
Biochemisch wird das Isopren in seiner biologischen Einheit von Organismen verwendet, um verschiedene Arten von Terpenen zu synthetisieren, von denen Waschsalon und die Komponenten von ätherischen Ölen hervorstechen. Organisch dient es für die Synthese von synthetischen Gummi und anderen verwandten Polymeren.
[TOC]
Isoprenstruktur
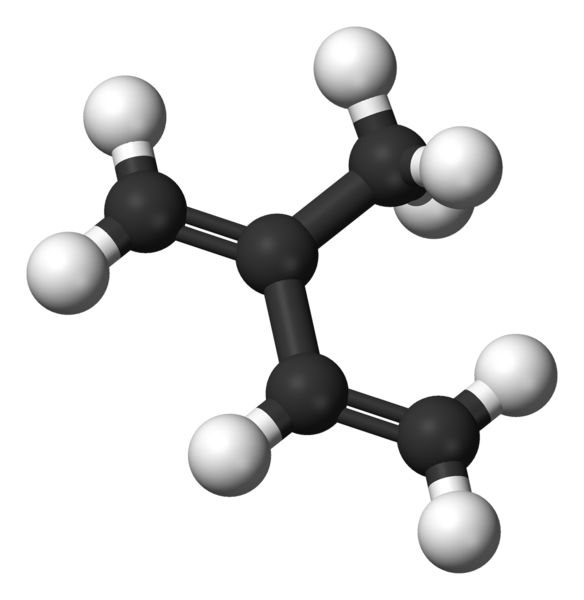 Isoprenmolekül dargestellt durch ein Modell von Kugeln und Balken
Isoprenmolekül dargestellt durch ein Modell von Kugeln und Balken Im überlegenen Bild haben wir die molekulare Struktur des Isoprens. Wie gesehen, entsprechen die schwarzen Kugeln Kohlenstoffatomen, während Weiß Wasserstoffatome sind.
Das Molekül zeigt eine flache Geometrie, dh alle seine Atome sind in derselben Ebene angeordnet, mit Ausnahme der Hydringen der Gruppe -ch3 Kohlenstoff verknüpft 2. Diese Geometrie ist darauf zurückzuführen, dass Kohlenstoffatome des 1,3-Butadien-Skelettons SP-Hybrater2, während der Kohlenstoff von -ch3 Es hat sp3.
Kann Ihnen dienen: Brom: Geschichte, Struktur, elektronische Konfiguration, Eigenschaften, verwendetIsoprenmoleküle interagieren durch dispersive Londoner Kräfte, die aufgrund ihrer niedrigen Molekülmassen erheblich schwach sind. Sie üben jedoch eine ausreichende Kohäsion aus, damit das Isopren unter normalen Bedingungen als flüchtige Flüssigkeit existiert.
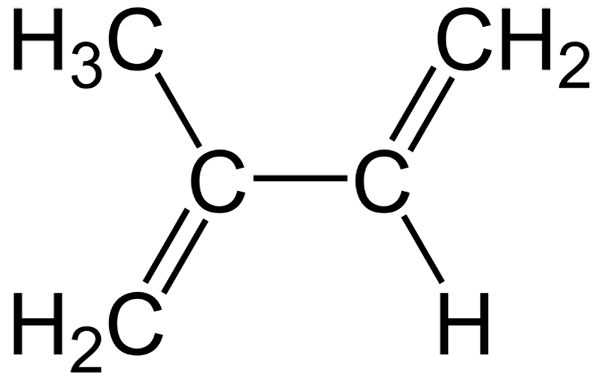 Strukturformel des Isoprens
Strukturformel des Isoprens Die Tatsache, dass ihre Moleküle flach sind, erleichtert ihre Einführung zwischen Zellmembranen und trägt zu ihren Verstärkungen in dem Mechanismus bei, mit dem Pflanzen plötzliche Temperaturänderungen gepolstert werden (40 ° C oder mehr).
Isoprenmoleküle können Kristalle bilden. Es geschieht jedoch nicht auf die gleiche Weise mit ihren Polymeren, dem Polyapren, das dazu neigen.
Isopreneigenschaften
Die hier genannten Eigenschaften entsprechen denen des Isoprens und nicht denen des Naturkautschuks, das aus dem Polymer cis-1,4-Polisopren besteht. Einige bibliografische Quellen können sogar die Eigenschaften des Latex verwenden, die frisch aus den Bäumen extrahiert wurden, um das Isopren zu charakterisieren, und ein schwerwiegender Fehler, um sie zu verwirren.
Aussehen
Farblose und flüchtige Flüssigkeit mit einem ähnlichen Geruch wie Öl.
Molmasse
68.12 g/mol
Schmelzpunkt
-143.95 ºC
Siedepunkt
3. 4.067 ºC. Daher ist es eine ziemlich volatile Flüssigkeit.
Flammpunkt
-54 ºC (geschlossener Tasse)
Selbstdirektionstemperatur
395 ºC
Dichte
0.681 g/cm3
Dampfdichte
2.35 in Bezug auf Luft.
Dampfdruck
550 mmHg bei 25 ° C, was seiner großen Volatilität entspricht.
Löslichkeit
Ein Kohlenwasserstoff zu sein, ist mit Wasser nicht mischbar, das sich in seinen Gemischen darüber befindet, weil es weniger dicht ist. Es ist jedoch mit Aceton, Benzol, Ölether, Kohlenstoffdisulfid, Dichlormethan und praktisch mit jedem anderen aromatischen oder chlorierten Lösungsmittel praktisch.
Kann Ihnen dienen: Art der Verbindung von 02Oberflächenspannung
16.9 Dins/cm.
Reaktivität
Das Isopren kann durch ihre Kohlenstoffe 1 und 4 nukleophil (angegriffen von elektronenreichen Spezies angegriffen) reagieren. Somit kann es an den Enden seines Kohlenstoffskeletts ein Polymer sein, was zu Polyapren führt. Diese Polymerisationsreaktion ist exotherm, so dass sie in Kontakt mit einigen Substanzen explosiv werden kann.
Biologische Einheiten
Das Isopren ist zwar intrinsisch in den Strukturen der Terpenen vorhanden, aber nicht das Ausgangsmaterial, das von Enzymen verwendet wird, um sie zu synthetisieren. Stattdessen verwenden sie metabolische Produkte, die als Substrate (DMApp, Rot) Isopentenyl (IPP, Blau) und Dimethylalil -Pyrophosphat (DMApp, Rot) Pyrophosphatprodukte bezeichnet werden (DMApp, Rot).
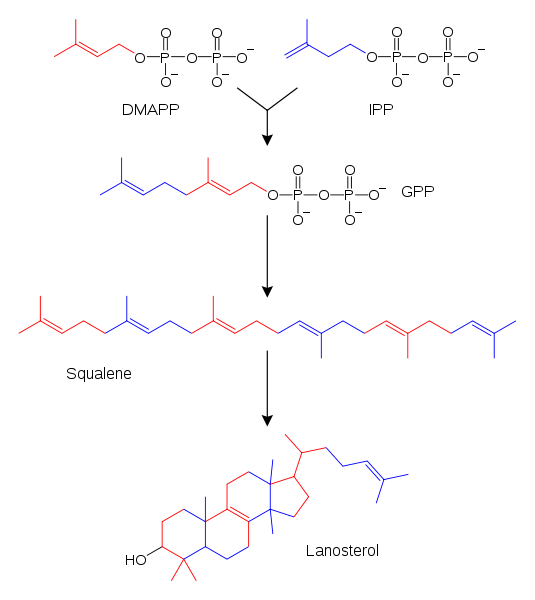 Loosterol -Synthese aus den biologischen Einheiten des Isoprens. Quelle: fvasconcellos, Original von Tim Vickers / Public Domain
Loosterol -Synthese aus den biologischen Einheiten des Isoprens. Quelle: fvasconcellos, Original von Tim Vickers / Public Domain Im überlegenen Bild ein Beispiel für das oben erwähnte oben. Sowohl die IPP als auch die DMApp reagieren dank der enzymatischen Intervention miteinander, um Geranilo -Pyrophosphat (GPP) zu verursachen.
Letzteres enthält wiederum andere molekulare Fragmente von IPP oder DMApp (siehe Farben), bis es zum Escualene wird, ein wertvoller Vorläufer für die Synthese der Wolle.
Dann beteiligt sich das Isopren in seiner biologischen Einheit (IPP oder DMAPP) an der Biosynthese von Sterolen und anderen Lipiden. Wir haben auch Terpene wie Limonen (von Zitronen- und Orangenölen) und Mizeno (Arrayán -Öl), die ätherische Öle bilden und durch chemische Prozesse und strukturell ähnlich ähnlich synthetisiert werden.
In diesem Sinne ist die Isopreneinheit, die in den Terpenen oder Isoprenoiden manchmal deutlich erkennbar ist.
Kann Ihnen dienen: LegierungIsoprenanwendungen
 Eine der wichtigsten Isopren -Gummianwendungen ist die Produktion von Autorreifen
Eine der wichtigsten Isopren -Gummianwendungen ist die Produktion von Autorreifen Das Isopren ist in Naturkautschuk polymerisiert, sodass alle seine Anwendungen auf indirekte Weise auf diese Verbindung zurückzuführen sind. Es ist Teil des Darmpapiers, elastisches Material aus einer Mischung aus cis- und transpolymeren 1,4-polisopren, die einst für die Herstellung von Golfkugeln verwendet wurden.
Der Gummi dient zur Ausarbeitung von Bällen, Schläuchen, Handschuhen, Kondomen, Stiefeln, Zubehör von elektrischen Instrumenten, Klebstoffen, Tauchanzügen, Flaschen für Flaschen, Beschichtungen, die Vibrationen neutralisieren; Und vor allem wird es zusammen mit seiner synthetischen Version, dem Isoprengummi, zur Massenproduktion von Reifen verwendet.
Das Isopren kann wie Polygrene mit anderen Polymeren wie Stretch-Butadien- oder Butadien-Rubbing-Gummi gemischt werden, um noch widerstandsfähigere und langlebigere Materialien zu erzeugen. Das heißt, es wird für die Synthese mehrerer elastischer Copolymere verwendet.
Außerhalb der Gummiindustrie ist das Isopren als Ausgangsmaterial für die Synthese von Vitaminen, Aromen, Steroiden, Duftstoffen und anderer Isopren -Substanzen bestimmt, die es lebensfähig sind, es zu synthetisieren, als es aus natürlichen Quellen aus Quellen zu erhalten.
Verweise
- Graham Solomons t.W., Craig b. Braten. (2011). Organische Chemie. (10th Auflage.). Wiley Plus.
- Carey f. (2008). Organische Chemie. (Sechste Ausgabe). Mc Graw Hill.
- Morrison und Boyd. (1987). Organische Chemie. (Fünfte Ausgabe). Addison-Wesley Iberoamericana.
- Wikipedia. (2020). Isopren. Abgerufen von: in.Wikipedia.Org
- Nationales Zentrum für Biotechnologie Information. (2020). Isopren. Pubchem Comunund -Zusammenfassung für CID 6557. Erholt von: Pubchem.NCBI.NLM.NIH.Regierung
- Elsevier b.V. (2020). Isopren. Scientedirect. Abgerufen von: Scientedirect.com
- Polymereigenschaften Datenbank. (2020). Isoprengummi: Eigenschaften und Anwendungen. Erholt von: Polymerdatabase.com
- « Einheiten Ionische Kraft, wie man sie berechnet, Beispiele
- Dihydroxyacetonstruktur, Eigenschaften, erhalten, verwendet, verwendet »

