Boyle Law
- 2374
- 737
- Luca Holdt
Was ist Boyles Gesetz??
Der Gesetz für Boyle oder Boyle-Maleotte-Gesetz Es ist eines, das die Beziehung zwischen dem von oder auf einem Gas ausgeübten Druck und dem Volumen, das dies besetzt, ausdrückt; ständig sowohl die Gastemperatur als auch die Menge (Anzahl der Maulwürfe) ständig aufbewahren.
Dieses Gesetz beschreibt zusammen mit dem von Charles, Gay-Lussac, Charles und Avogadro das Verhalten eines idealen Gases; Insbesondere in einem geschlossenen Behälter, der Volumenänderungen unterliegt, die von einer mechanischen Kraft ausgeübt werden.
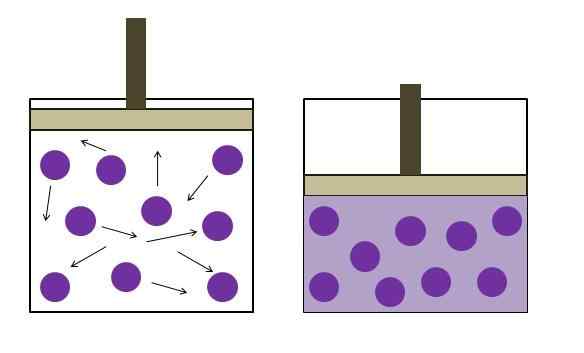
 Erhöhter Druckreduzierungsdruck. Quelle: Gabriel Bolívar
Erhöhter Druckreduzierungsdruck. Quelle: Gabriel Bolívar Das obere Bild fasst das Boyle -Gesetz kurz zusammen. Lila Punkte repräsentieren Moleküle oder Gasatome, die mit den inneren Wänden des Behälters kollidieren (links). Durch die Verringerung des verfügbaren Raums oder des verfügbaren Volumens des von diesem Gas besetzten Behälters werden die Kollisionen erhöht, was zu einer Erhöhung des Drucks (rechts) führt, was zu einer Erhöhung des Drucks führt (rechts).
Dies zeigt, dass der Druck von P und Volumen V des Gases umgekehrt proportional ist, wenn der Behälter fest geschlossen ist. Andernfalls wäre ein höherer Druck gleich einer stärkeren Dilatation des Behälters.
Wenn ein Diagramm V gegen P mit den Daten von V und P an den Achsen bzw. x beobachtet wird, würde eine asymptotische Kurve beobachtet. Je niedriger V, desto größer ist die Zunahme von p; Das heißt, die Kurve erstreckt sich auf hohe Werte von p auf der x -Achse.
Natürlich bleibt die Temperatur konstant; Wenn das gleiche Experiment bei unterschiedlichen Temperaturen durchgeführt wurde, würden sich die relativen Positionen dieser Kurven V gegenüber P auf der kartesischen Achse ändern. Die Änderung wäre noch deutlicher, wenn es sich um Graphen einer dreidimensionalen Achse mit konstanter T auf der Z -Achse handelt.
Geschichte des Boyle -Gesetzes
Hintergrund
Da der Wissenschaftler Galileo Galilei seinen Glauben an die Existenz der Leere (1638) zum Ausdruck brachte, begannen Wissenschaftler, die Eigenschaften von Luft- und Teillücken zu untersuchen.
Der angloirlandische Chemiker, Robert Boyle, begann 1638 mit dem Studium der Lufteigenschaften, als er erfuhr, dass Otto von Guericke, ein deutscher Ingenieur und physischer Ingenieur, eine Luftbombe gebaut hatte.
Kann Ihnen dienen: Brom: Geschichte, Struktur, elektronische Konfiguration, Eigenschaften, verwendetQuecksilberexperiment
Um seine Luftdruckstudien durchzuführen, verwendete Boyle ein "J" -Formrohr, dessen Konstruktion Robert Hooke, einem Boyle -Assistenten, zugeschrieben wurde. Die kurze Armende wurde versiegelt, während die lange Armende des Rohrs offen war, um das Quecksilber zu platzieren.
Boyle wollte von Anfang an die Elastizität der Luft qualitativ und quantitativ untersuchen. Als Quecksilber in Form von "J" durch das offene Ende des Rohrs strömte, ließ Boyle ab.
Ergebnisse
Je größer die Menge an Quecksilber, die dem Rohr hinzugefügt wurde, desto größer wird der auf die Luft ausgeübte Druck und desto niedriger sein Volumen. Boyle erhielt je nach Druck ein negatives exponentielles Diagramm des Luftvolumens.
Wenn das Volumen der Luft gegen den umgekehrten Druck aufgetragen wird, gibt es eine gerade Linie positiver Steigung.
1662 veröffentlichte Boyle das erste physische Gesetz, das in Form einer Gleichung gegeben wurde, die die funktionale Abhängigkeit von zwei Variablen anzeigte. In diesem Fall Druck und Volumen.
Boyle sagte. Die meisten Gase verhalten sich als ideale Gase zu mäßigen Drücken und Temperaturen.
Wenn höhere Drücke und niedrigere Temperaturen auftreten, wurden Abweichungen vom Verhalten der realen Gase der Ideale bemerkenswerter.
Edme Mariotte
Der französische Physiker Edme Mariotte (1620-1684) entdeckte 1679 unabhängig das gleiche Gesetz. Aber er hatte den Verdienst, zu zeigen, dass das Volumen mit der Temperatur variiert. Deshalb heißt Mariotte's Law oder Law von Boyle und Mariotte.
Verstärkung des Gesetzes
Daniel Bernoulli (1737) verstärkte das Boylesche Gesetz, indem er darauf hinwies, dass der Druck eines Gases durch die Auswirkungen von Gaspartikeln auf die Wände des Behälters erzeugt wird, die es enthalten.
Es kann Ihnen dienen: Nucleophil: nucleophiler Angriff, Typen, Beispiele, Nucleophilie1845 veröffentlichte John Waterston einen wissenschaftlichen Artikel, der sich auf die Hauptprinzipien der kinetischen Theorie der Gase konzentriert.
Anschließend konsolidierten Rudolf Clausius, James Maxwell und Ludqwig Boltzmann die kinetische Theorie von Gasen, die den Druck in Bezug.
Je niedriger das Volumen des Behälters, das ein Gas enthält, desto größer ist die Frequenz der Auswirkungen der Partikel, die es gegen die Wände des Behälters bilden. Und daher desto größer ist der vom Gas ausgeübte Druck.
Was ist dieses Gesetz??
Die von Boyle durchgeführten Experimente weisen darauf hin, dass eine umgekehrte Beziehung zwischen dem von einem Gas besetzten Volumen und dem darauf ausgeübten Druck besteht. Die oben erwähnte Beziehung ist jedoch nicht vollständig linear, wie durch ein Volumenvariationsdiagramm gemäß dem Druck, der Boyle zugeschrieben wird.
In Boyle's Law wird angegeben, dass das von einem Gas besetzte Volumen umgekehrt proportional zum Druck ist. Es wird auch angezeigt, dass das Produkt des Drucks eines Gases nach seinem Volumen konstant ist.
Mathematischer Ausdruck
Um zum mathematischen Ausdruck des Boyle -Gesetzes zu gelangen, beginnt es aus:
V ∝ 1/p
Wo es anzeigt, dass das von einem Gas besetzte Volumen umgekehrt proportional zu seinem Druck ist. Es gibt jedoch eine Konstante, die bestimmt, wie umgekehrt proportional diese Beziehung ist.
V = k/p
Wobei K die Verhältnismäßigkeitskonstante ist. Clearing k haben: Sie haben:
Vp = k
Das Produkt des Drucks eines Gases durch sein Volumen ist konstant. So:
V1P1 = K und v2P2 = k
Und dies kann abgeleitet werden, dass:
V1P1 = V2P2
Letzteres ist Ausdruck oder endgültige Gleichung für Boyle's Gesetz.
Wofür ist das? Welche Probleme lösen das Boyle's Law??
Dampfmaschinen
Boyle-Maleotte-Gesetz wird im Betrieb von Dampfmaschinen angewendet. Es ist ein externer Verbrennungsmotor, der die Umwandlung der thermischen Energie einer Menge Wasser in mechanische Energie nutzt.
Wasser wird in einem dicht geschlossenen Kessel erhitzt, und der erzeugte Dampf wird nach dem Boyle -Gesetz Druck ausgeübt, das eine Ausdehnung eines Zylindervolumens durch Drücken eines Kolben.
Kann Ihnen dienen: VerdünnungsfaktorDie lineare Bewegung des Kolben.
Schluckgetränke
Die Wirkung, ein Soda oder einen Saft einer Flasche durch ein Plastikrohr aufzuhalten, hängt mit dem Boyle -Gesetz zusammen. Wenn die Luft des Rohrs mit dem Mund vorgeschlagen wird, nimmt der Druck im Röhrchen ab.
Dieser Druckabfall erleichtert die aufsteigende Bewegung der Flüssigkeit im Röhrchen und ermöglicht die Aufnahme. Das gleiche Prinzip funktioniert in der Blutgewinnung durch Verwendung einer Spritze.
Atmungssystem
Das Boyle -Gesetz ist eng mit der Funktionsweise des Atmungssystems verbunden. Während der Inspirationsphase tritt die Kontraktion des Zwerchfells und anderer Muskeln auf; Zum Beispiel externe Interkostale, die eine Expansion des Brustkorbs erzeugen.
Dies führt zu einer Abnahme des intrapleuralen Drucks, was zu einer Lungenexpansion führt, die zu einem Anstieg des Lungenvolumens führt. Daher nimmt der intrapulmonale Druck entsprechend dem ab, was im Boyle -Gesetz aufgewachsen ist.
Indem die atmosphärische Luft in der Lunge subatose wird, wird der intrapulmonale Druck in die Lunge fließt, was zu einem Druckerhöhung in der Lunge führt; somit seinen Druck auf den atmosphärischen Druck übereinstimmen und die Inspirationsphase abschließen.
Anschließend entspannen sich die Inspirationsmuskeln und die expiratorischen Muskeln verziehen sich. Darüber hinaus wird eine elastische Lungenretraktion erzeugt, ein Phänomen, das zu einer Abnahme des Lungenvolumens führt, wobei der intrapulmonale Druck zu einer Erklärung durch Boyle's Law erklärt wird.
Durch Erhöhen des intrapulmonalen Drucks und durch den größeren atmosphärischen Druck fließen die Luft in die Lunge zur Atmosphäre. Dies geschieht, bis die Drucke gleich sind, was die Ablaufphase abschließt.
Verweise
- Boyles Gesetz. Encyclopædia Britannica. Erholt von: Britannica.com
- Die Formel für Boyle's Law. Erholt von: thoughtco.com

