Metalle
- 1712
- 255
- Rieke Scheer
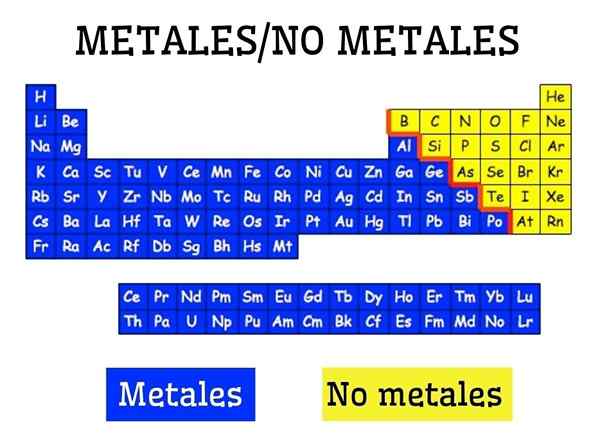
 Metalle und Nicht -Metalle in der Periodenzüchttabelle der Elemente
Metalle und Nicht -Metalle in der Periodenzüchttabelle der Elemente Was sind Metalle?
Metalle werden durch eine Gruppe von Elementen gebildet, die sich auf der linken Seite befinden, mit Ausnahme des nicht -metalischen Wasserstoff. Metalle machen etwa 75 % der chemischen Elemente aus, so dass ein Großteil der Natur metallisch ist.
Die Metalle, die der Mensch ursprünglich in der Vorgeschichte verfolgt wurde, waren Folgendes: Gold, Silber, Kupfer, Zinn, Blei und Eisen. Dies lag an der Tatsache, dass sie einheimisch waren oder die Leichtigkeit ihrer Verarbeitung zur Durchführung von Versorgungsobjekten ausführen.
Es scheint eine Frage der Magie, dass viele Felsen und Mineralien glänzende und silberne Körper extrahiert werden können (mit bestimmten wichtigen und herausragenden Ausnahmen). So wie.
Metalle sind der Rahmen der Branchen; Ihre Kabel, Reaktoren, Einheiten, Behälter, auf die eine oder andere Weise bestehen aus Metallen und ihren Legierungen.
Mit Metallen wurden die ersten Münzen, Waffen, Werkzeuge, Rüstung hergestellt und dann unter anderem in Fahrzeugherstellern, Fahrrädern, Schiffen, Flugzeugen und Computern verwendet, unter anderem unverzichtbare Objekte im modernen Leben.
Geschichte
Kupferzeitalter
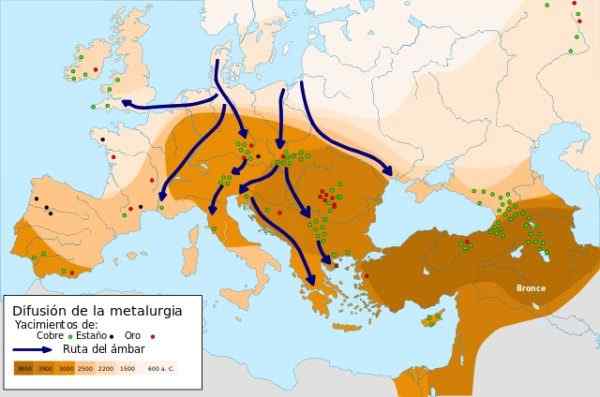 Metallurgie -Expansion - Quelle: Metallurgische Diffusion.SVG unter der Creative Commons Attribution-Compartyrigual 4 Lizenz 4.0 International
Metallurgie -Expansion - Quelle: Metallurgische Diffusion.SVG unter der Creative Commons Attribution-Compartyrigual 4 Lizenz 4.0 International In 9000 a.C. Die ersten im Nahen Osten geschmiedeten Kupferobjekte wurden ausgearbeitet, als der Mann entdeckte, dass er beim Hämmern des Kupfers seine Stärke und seinen Widerstand erhöhte, wobei er für die Herstellung von Messern verwendet wurde. Dies ist das Alter von Kupfer.
Es wurde festgestellt, dass Kupfer durch die Erwärmung von blauen Mineralien wie Corvellita und Malachit (4000-3000 bis.C.).
Die Kalkolithikum ist eine Zeitspanne, die der Bronzezeit vorausgeht, die 5000-3000 bis entspricht.C. Der Mann begann mit der Fusion und Gießerei von Kupfer zu experimentieren, um Kupfer aus Kupferoxid zu erhalten.
Bronzezeit (3000-1500 a.C.)
 Materialien der Bronzezeit - Quelle: Gaguilella unter der Creative Commons Attribution -Shareigual 4 Lizenz 4.0 International.
Materialien der Bronzezeit - Quelle: Gaguilella unter der Creative Commons Attribution -Shareigual 4 Lizenz 4.0 International. Der Mann begann versehentlich mit der Ausarbeitung von Legierungen, zunächst aus Kupfer und Arsen und dann mit Kupfer und Zinn, um im Nahen Osten Bronze zu erhalten.
Bronzeartikel, die dieser Zeit entsprechen, hatten 87 % Kupfer, 11 % Zinn und kleine Mengen Eisen, Arsen, Nickel, Blei und Antimon.
Eisenzeit (700 a.C.)
Der Mann nutzte seine Erfahrung in der Herstellung von gefälschtem Kupfer für die Herstellung von Schmiedeeisen im Nahen Osten. Im gleichen Zeitraum gab es die Granulation von Etrusco Dust, Italien.
Die erste bekannte Stahlproduktion, eine Eisen- und Kohlenstofflegierung, manifestierte sich in Metallstücken in einer archäologischen Stelle in Anatolia (1800 bis.C.)
Kann Ihnen dienen: Gravimetrie: Gravimetrische Analyse, Methoden, Verwendungen und BeispieleGegen 1122 d.C., An einem unbekannten Datum und Ort wird Gusseisen vorgestellt. 1440 d.C. Pekings große Glocke wird produziert, China. Fast drei Jahrhunderte später im Jahr 1709 d.C., Gusseisen wird mit Cola als brennbares Material hergestellt.
1779 wurde Gusseisen in England als architektonisches Material verwendet. Im Jahr 1855 verwendete Henry Bessenir Arrabio als Rohstoff, um Weichstahl zu erhalten. Das englische Clark und Wood (1872) Patent an eine Legierung, die derzeit als Edelstahl angesehen wird.
Physikalische Eigenschaften von Metallen
 Die Bronze dieser alten Glocken zeigt die Nützlichkeit von Metallen für dekorative oder religiöse Zwecke. Quelle: pxhere.
Die Bronze dieser alten Glocken zeigt die Nützlichkeit von Metallen für dekorative oder religiöse Zwecke. Quelle: pxhere. Unter einigen physikalischen Eigenschaften von Metallen haben wir:
-Metalle sind brillant und können das Licht reflektieren.
-Im Allgemeinen sind sie gute Leiter von Strom und Wärme.
-Sie haben hohe Verschmelzungs- und Siedepunkte.
-Sie sind formbar, das heißt, sie können gehämmert werden, um niedrig dicke Blätter zu produzieren.

-Sie sind duktil, mit ihnen können Sie Drähte oder Fasern mit sehr geringem Durchmesser herstellen.
-Sie werden in einem festen Zustand präsentiert, mit Ausnahme des Quecksilber. Im folgenden Bild sehen Sie einen Quecksilberbehälter:

-Sie sind undurchsichtige Körper, ihre dünnen Blätter werden vom Licht nicht gekreuzt.
-Sie haben große Härte, bis auf Natrium und Kalium, die von einem Messer geschnitten werden können.
-Sie haben eine hohe Dichte, die Osmium und Iridium des höchsten und das Lithium der niedrigsten Dichte sind.
Chemische Eigenschaften von Metallen
Unter einigen chemischen Eigenschaften von Metallen haben wir:
-Sie neigen dazu, Elektronen zu verlieren und Metallkationen zu bilden, mN+, wobei n seine Oxidationszahl angibt, die nur für alkalische und alkalistische Metalle mit seiner Valenzzahl zusammenfällt.
-Seine Elektronegativitäten sind niedrig.
-Sie rennen und erleben Oxidationsschäden.
-Sie bilden Basisoxide, wenn sie mit Sauerstoff reagieren. Diese Oxide in Kombination mit Wasser bilden Metallhydroxide. Metalloxide reagieren mit Säuren, um Salze und Wasser zu bilden.
-Sie sind gut reduzierende Wirkstoffe, da sie ihre Elektronen ergeben.
Arten von Metallen
Metalle werden als Folgendes eingestuft: alkalische, alkalische, posttransitageische, transitions- und sogenannte seltene Erden.
Alkali Metalle

Sie befinden sich normalerweise nicht frei in der Natur, weil sie leicht oxidieren. Habe ein suborbitales s1 In seiner externen Orbitalschicht haben sie einen Oxidationszustand +1. Sie sind Metalle, die exotherm mit Wasser reagieren und stark reduzieren.
Alkaline-Térreos-Metalle
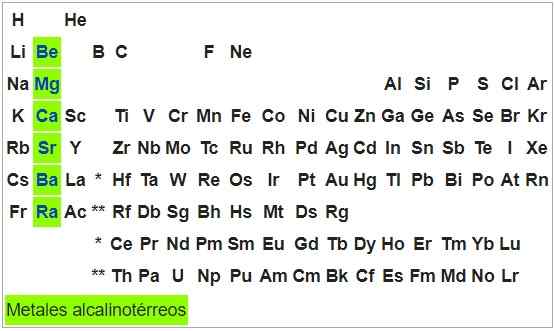
Sie sind formbare und duktile Metalle. Die Atome der Elemente dieser Gruppe haben eine S -Konfiguration2, Sie können also zwei Elektronen ergeben und ihr Oxidationsstatus beträgt +2. Mit Ausnahme des Beryllium.
Kann Ihnen dienen: Kohlenstoff AlotropesPostübergreifende Metalle
Sie sind Metalle des sogenannten P -Blocks zwischen Übergangsmetallen und Metalloiden in der Periodenzüchttabelle.
Die Elemente der Gruppe 3 haben Oxidationszustände +1 und +3 als die häufigsten, obwohl Aluminium nur den Oxidationszustand +3 darstellt. Es ist auch Teil der post -transitionalen Metalle in den Gruppen 14 und 15.
Übergangsmetalle d
Sie bilden eine Gruppe zwischen den basenbildenden Elementen und Säureformatoren. Atom -Orbitale D und F sind unvollständig und werden gefüllt. Obwohl der Begriff Übergangsmetalle auf Übergangsmetalle d bezieht.
Übergangsmetalle haben mehr als einen Oxidationszustand. Sie haben Fusions- und Siedepunkte, die höher sind als andere Metallgruppen. Übergangsmetalle sind eine sehr heterogene Metallgruppe, die unter anderem Eisen, Chrom, Silber usw. umfasst.
Seltene Erden
 Seltenerd Mineral
Seltenerd Mineral Diese Gruppe von Metallen besteht aus den Elementen Scandio und Ititrio und den Elementen der Reihe von Lantaniden und Aktiniden. Der Begriff "Seltener Erde" bezieht sich auf die Tatsache, dass sie in reinen Zuständen nicht in der Natur gefunden werden und durch Säuren befestigt werden können.
Verwendet/Anwendungen von Metallen
Alkali Metalle
Lithium wird bei einigen Kernreaktoren als Wärmeübertragungsmittel verwendet. Es wird in einigen trockenen Batterien und Akkumulatoren mit wenig Gewicht verwendet. Chlorid und Lithiumbromid sind hygroskopische Verbindungen, die bei industriellen Trocknungs- und Klimaanlagenverfahren verwendet werden.
Natrium wird in Metallmetallurgie wie Titan und Zirkonium verwendet. Es wird in der öffentlichen Beleuchtung in Natriumbogenlampen verwendet. Natriumchlorid (NaCl) wird als Lebensmittelgeschmack und Fleischkonservierung verwendet.
Alkalineter -Metalle
Magnesium wurde in der Fotografie als Blitzlicht und Feuerwerk verwendet. Barium ist ein Bestandteil von Legierungen, die in Zündkerzen verwendet werden. Bariumsalze werden verwendet, um die durch X -Strahlen in Magen -Darm -Traktaten verursachten Schäden zu begrenzen.
Calcium wird verwendet, um die in geschmolzenen Metallen gelösten Verunreinigungen und bei der Eliminierung von Restgasen in Vakuumröhrchen zu beseitigen. Es ist Teil des Gips, Material, das bei der Konstruktion und bei der Behandlung von Knochenbrüchen verwendet wird.
Postübergreifende Metalle
Aluminium, weil es ein Leichtmetall ist, wird beim Bau von Flugzeugen und Gefäßen verwendet. Es wird auch zur Ausarbeitung zahlreicher Küchenutensilien verwendet. Es wird als Rohstoff bei der Herstellung von Deodorants verwendet, die das Schwitzen einschränken.
Kann Ihnen dienen: prozentuale LösungenGallium wird bei Transistoren und Thermometern für hohe Temperaturen verwendet. Das Isotop 67GA wird in der Medizin bei der Behandlung einiger Melanome eingesetzt. Blei wird beim Bau von Batterien und beim Schutz vor ionisierender Strahlung verwendet.
Übergangsmetalle
Kupfer wird in Wasserversorgungsrohren, in Kühlschränken und Klimaanlagen verwendet. Es wird auch als Teil des Computermechanismus des Computers Wärme verwendet. Es wird bei der Leitung von elektrischem Strom, in Elektromagneten und in der Färbung von Glas verwendet.
Der Nickel wird bei der Ausarbeitung von Edelstahl sowie Gitarrenstrings und wiederaufladbaren Batterien verwendet. Es wird auch in der Galvanoplastik beim Metallschutz verwendet. Es wird in Legierungen verwendet, die in Teilen von Fahrzeugen wie Ventilen, Lager und Bremsen enthalten sind.
Der Nickel wird seit langem bei der Ausarbeitung von Münzen verwendet.
Zink wird im Korrosionsmetallschutz verwendet, in der Messingproduktion. Zinkoxid und Zinksulfat werden zur Herstellung von Platten verwendet.
Chrom wird im Metallkorrosionsschutz verwendet und liefert Glanz. Es wird als Katalysator in der Ammoniaksynthesereaktion (NH3). Chromoxid wird im Holzschutz verwendet.
Seltene Erden
Der Skandio wird in Aluminiumaluminium für Luft- und Raumfahrtkomponenten verwendet. Es ist ein Additiv in Quecksilberdampflampen.
Der Lantano wird in hoher Brechung und Alkalis -resistentes Glas verwendet. Darüber hinaus wird es zur Herstellung von Kameraslinsen und als katalytische Katalysatorflüssigkeit für Ölraffinerien verwendet.
Cerio wird als chemischer Mittel verwendet. Darüber hinaus wird es für die Versorgung einer gelben Glas- und Keramikfärbung sowie für den Katalysator für selbstbeschäftigte Öfen verwendet.
Beispiele für Metallelemente
Alkalisch
Natrium (Na), Kalium (K), Cesio (CS), Lithium (Li) und Rubidium (Ru).
Alkaline-Terreos
Beryllium (BE), Magnesium (Mg), Calcium (CA), Strontium (MR), Barium (BA) und Radio (RA).
Posttrangieren
Aluminium (Al), Gallium (GA), Inder (IN), Talio (TL), Tin (SN) und Blei (PB).
Übergang
Titan (Ti), Vanadium (V), Chrom (CR), Mangan (Mn), Eisen (Glaube), Cobalt (CO), Nickel (Ni), Kupfer (Cuinc), Zink (Zn), Zirkonium (ZR), Niobio (NB), Molybdän (MO), Paladio (PD), Silber (AG), Volframium (W), Renio (RE), Osmio (OS), Iridido (Ir),
Platin (Pt), Gold (Au) und Quecksilber (Hg).
Seltene Erden
Scandio (SC), Itrio (Y), Lantano (LA), Cerio (CE), Praseodimio (PR), Neodym (ND), Samarium (SM), Europio (EU), Gadolinio (GD), Holmio (HO), HO Erbio (ER), Tulio (TM), Iterbio (YB) und Luthacio (Lu).
Verweise
- Whitten, Davis, Peck & Stanley. (2008). Chemie. (8. Aufl.). Cengage Lernen.
- Shiver & Atkins. (2008). Anorganische Chemie. (Vierte Edition). Mc Graw Hill.
- Helmestine, Anne Marie, ph.D. (5. Oktober 2019). Metalle gegen Nichtmetalle. Erholt von: thoughtco.com
- Metalle und ihre Eigenschaften-physikalisch und chemisch. [PDF]. Erholt von: csun.Edu
- Jonathan Meister. (2019). 18 verschiedene Arten von Metall (Fakten und Verwendungszwecke). Erholt von: makeitfrommetal.com

