Myosineigenschaften, Struktur, Typen und Funktionen
- 5045
- 514
- Nick Laurén
Der Myosin Es ist ein molekularer Motor aus Protein Natur, der sich im Cytosol auf Aktinfilamente bewegen kann. Die Energie, die die Verschiebung von Myosin antreibt, stammt aus der ATP -Hydrolyse. Aus diesem Grund wird Myosin normalerweise als Mecanochemistry -Enzym definiert.
In Eukaryoten ist Myosin ein sehr häufiges Protein. Es gibt verschiedene Arten von Myosin, die von einer Familie von Genen kodiert werden. In Hefen werden 5 Klassen unterschieden, während Dutzende bei Säugetieren beschrieben wurden.
 Quelle: David Richfield (Benutzer: Slashme) Wenn dieses Bild in externen Werken verwendet wird, kann es wie folgt zitiert werden: Richfield, David (2014). "Medizingalerie von David Richfield". Wikijournal of Medicine 1 (2). Doi: 10.15347/WJM/2014.009. ISSN 2002-4436. [CC BY-SA 3.0 (http: // creativecommons.Org/lizenzen/by-sa/3.0/]]
Quelle: David Richfield (Benutzer: Slashme) Wenn dieses Bild in externen Werken verwendet wird, kann es wie folgt zitiert werden: Richfield, David (2014). "Medizingalerie von David Richfield". Wikijournal of Medicine 1 (2). Doi: 10.15347/WJM/2014.009. ISSN 2002-4436. [CC BY-SA 3.0 (http: // creativecommons.Org/lizenzen/by-sa/3.0/]] Myosin hat eine Vielzahl von Funktionen. Myosin I. neben Actin nimmt an der Bewegung von Keratozyten teil.
Myosin II bietet Steifheit der Plasmamembran und beteiligt sich an der Zytokinese und der Muskelkontraktion. Beide, Myosinas I und II, arbeiten mit der Zellmigration zusammen. Myosinas I und V führen den Transport von Vesikeln entlang der Aktinfilamente durch.
[TOC]
Struktur
In elektronischen mikroskopischen Aufnahmen hat die typische Myosin -Isoformstruktur drei Domänen: Kopf, Hals und Schwanz. Durch Hydrolyse mit Chimotripsin wird ein Segment aus Kopf und Hals, das als schweres Meromiosin (HMM) bezeichnet wird, und ein Schwanzsegment, das als leichte Meromiosin (LMM) bezeichnet wird, erhalten.
Die Beherrschung des Kopfes ist das N-terminale Ende der schweren Kette, und die Domäne des Schwanzes ist das C-terminale Ende der leichten Kette.
Myosinklassen können durch die Anzahl der polypeptischen Ketten differenziert werden.
Myosin Ich habe eine Polypeptidkette, die einen Kopf bildet, und sein Schwanz fehlt Alpha -Helizidregionen. Während Myosinas I und V zwei Polypeptidketten und dort haben.
Myosinas I und V haben Gewerkschaftsstandorte nach Calmodulin, die reguliert und behebt CA+2, In leichten Ketten. Die Myosina, die ich korrigierte, ca+2 In leichten Ketten, aber so unterschiedlich als Calmodulin.
Eigenschaften
Auf mechanischer Ebene haben Myosinas drei Eigenschaften, nämlich:
- Der Kopf von Myosin ist die motorische Domäne, die durch diskrete Schritte voranschreitet: die Vereinigung des Myosin -Kopfes zu einem Aktin -Filament, seiner Neigung und der anschließenden Trennung erzeugt die Bewegung von Myosin. Dieser Prozess ist zyklisch und hängt von ATP ab.
- Konformationsänderungen: Die Hydrolyse eines ATP -Moleküls wird bei jedem Schritt eines Myosinmolekül. Dies impliziert große Konformationsänderungen von Myosin.
Kann Ihnen dienen: radiale SymmetrieDie erste Amplifikationsstufe erzeugt sich durch den Verlust der Gamma-Phosphat-Gruppe des ATP, wodurch eine Umstrukturierung der Strukturelemente am Standort der ATP Union ermöglicht wird. Diese Reorganisation ist mit strukturellen Veränderungen an der Gewerkschaftsstelle zu Actin koordiniert.
Die zweite Amplifikationsstufe impliziert die Kommunikation der Konformationsänderung im aktiven Zentrum zu strukturellen Komponenten des Terminalscarboxyls.
- Richtungslosigkeit: Es wurde festgestellt. Diese Schlussfolgerung stammt aus den Leveling -Experimenten des Actin -Filaments unter Verwendung des optischen Fluoreszenzmikroskops.
Funktionen
Myosin neben Actin nimmt an Muskelkontraktion, zellulärer Adhäsion, Zytokinese, der Steifheit der kortikalen Membranen und der Verschiebung einiger Vesikel beteiligt, unter anderem Steifheit.
Myosin -Defekte können pathologische Bedingungen erzeugen. Zum Beispiel sind Defekte in Myosinas I und V mit Myopathien von Myosin- und Pigmentierungsstörungen verwandt (Griselli -Syndrom). Während die Erkrankungen in Myosin -Isoformen VI verursachen.
Muskelkontraktion
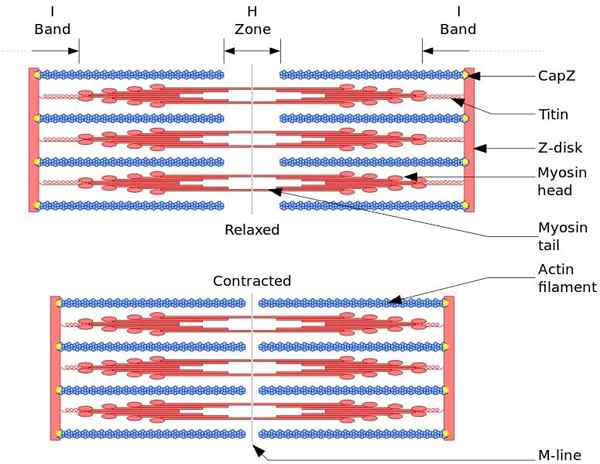
Die funktionelle und strukturelle Einheit des Skelettmuskels ist Sarkom. Während der Muskelkontraktion erreicht die Länge des Sarkomers 30% seiner ursprünglichen Länge.
Sarkomere bestehen aus dicker, Myosin- und dünner Aktinfilamenten, die auf komplexe Weise organisiert sind. Im Allgemeinen befinden sich Myosinköpfe an den distalen Enden des Filaments und seiner Schwänze in Richtung der Mitte des Sarkomeros, und die Organisation ist bipolar.
Um Muskelkontraktion zu machen, müssen Myosinköpfe der entgegengesetzten Enden zur Z -CD oder zum Ende (+) des Filaments bewegen. Da die Organisation dicker Filamente bipolar ist, tritt das Gleiten dünner Filamente auf dicke Filamente auf, die durch ATP angetrieben werden.
Die Verschiebungskraft tritt auf, weil Hunderte von Myosinköpfen eines dicken Filaments mit einem dünnen Filament interagieren.
Cytocinese
Während der Mitose bilden Actin und Myosin II, wenn die Mikrotubuli der Spindelpolen getrennt sind, in der Zelle der Zelle einen kontraktilen Ring. Dieser Ring bezieht seinen Durchmesser und teilt die Zelle in zwei Teile ein.
Erteilung der Steifheit für kortikale Membranen
In mutierten Zellen, denen Myosin II fehlt, ist die Plasmamembran leicht zu verformen, wenn eine externe Kraft angewendet wird. Dies geschieht, weil Myosin II den Plasmamembranproteinen Aggregationskraft liefert.
Kann Ihnen dienen: Morphologische AnpassungZelluläre Adhäsion
Im epithelialen Gewebe befinden sich die kontraktilen Aktin- und Myosin -II -Strahlen in den Nachbarschaften der Plasmamembran und bilden einen kreisförmigen Gürtel, der die Zellzelloberfläche umgibt. Dieser kreisförmige Gürtel bestimmt die Form der Zelle und behält die Vereinigung zwischen den Zellen bei.
Der Kontakt zwischen Zellen erfolgt durch die kreisförmige Gürteleinstellung zu Zelladhäsionsmolekülen unter Verwendung von Bindungsproteinen.
Verschiebung einiger Vesikel
Experimentelle Beweise zeigen, dass Myosin V den Membrantransport vom Golgi -Apparat bis zur Peripherie der Zelle durchführt. Einige Beweise sind:
- In nervösen Gewebezellen wurde durch Immunfluoreszenz von Astrozyten festgestellt, dass sich Myosin V neben Golgi befindet.
- In Hefen unterbricht Mutationen im Myosin -V -Gen die Proteinsekretion und folglich akkumulieren Proteine im Cytosol.
- Myosin I Isoformen sind für den Transport von Vakuolen in die Zellmembran verantwortlich. Unter Verwendung spezifischer Antikörper gegen Myosin I -Isoformen wurde festgestellt, dass sich diese Isoformen in verschiedenen Teilen der Zelle befinden.
Wenn beispielsweise ein lebender Amöbe mit einem Antikörper gegen Myosins markiert ist, wird der Transport der Vakuole in die Membran festgenommen. Aus diesem Grund dehnt sich die Vakuole aus und die Zelle explodiert.
Myosin -bezogene Krankheiten
Myosinas und Ohrverlust
Es gibt zahlreiche Gene und Mutationen, die den Ohrverlust erzeugen. Diese Krankheit ist häufig monogenetisch .
Mutationen in unkonventionellen Myosinas mit einem oder zwei Köpfen Myosin beeinflussen die Funktionsweise des inneren Ohrs. Einige der mutierten Myosin -Isaformen sind Myosin IIIa, Myosin VIIA und Myosin XVA. Vor kurzem wurden in Myosin VI zwei Mutationen entdeckt.
Die Mutationen in Myosin VI sind c.897g> t und p.926Q. Die erste Mutation wirkt sich auf einen Bereich aus, der mit dem aktiv gelegenen aktiven Switch I interagiert. Homozygot für die frühe Mutation zeigen den Phänotyp und verursachen schwerwiegende Wirkungen.
Die zweite Mutation beeinflusst einen Lastbereich mit Last in einem Alpha -Propeller im Schwanz von Myosin VI. Diese Region ist wichtig für die proximale Dimerisierung des Motors und beeinflusst die Stereo-Chart-Funktion von Myosin VI.
Es kann Ihnen dienen: Hilfswissenschaften der BiologieEine andere Mutation ist p.ASN207ser, der einen Motor erzeugt, der keine Kraft erzeugen kann. Dies liegt daran.
Die Mutation p.Arg657TRP erzeugt den Verlust der Myosin VI -Funktion. Der Arg -Rückstand ist an den Konformationsänderungen beteiligt, die Hydrolyse an die Myosinbewegung verbinden.
Myosin X und Krebs
Myosina X (MYO10) ist ein unkonventionelles Myosin, das im Gehirn, Endothelios und viele Epithele exprimiert wird. Myo10 und drei Arten von Actin -basierten Projektionen (Philopoden, Rechnungen und Projektionen ähnlich wie die Philopodianer) während der Krebsmetastasierung.
Invasive Krebszellen haben eine große Anzahl von Philopoden und exprimieren ein hohes Maß an Fascin. Dieses Protein führt Kreuzungen zwischen Aktinfilamenten durch. Um dem Primärtumor zu entkommen.
Sobald die Zellen die extrazelluläre Matrix erreicht haben. Hohe Myo10 -Werte deuten auf eine hohe Aggressivität und Metastasierung bei Brustkrebs hin.
Die Stummschaltung von Myox erzeugt den Verlust des metastasierten Charakters von Zellen, die keine Aktin -basierten Projektionen bilden können. Alle diese Projektionen haben eine Verständnis -Basis -Adhäsionen, die von MY1010 innerhalb des Philopodiums transportiert werden.
Myox ist an der Bildung der Zentren beteiligt. Das Fehlen von Myox begünstigt die Bildung multipolarer Spikes. Myox ist auch an der Signalübertragung in Krebszellen beteiligt. Zum Beispiel wird myox durch 3,4,5, -inositol trifosphat (PIP3) aktiviert.
Verweise
- Alberts, geb., Johnson, a., Lewis, J., und Kohl. 2007. Biologie des Zellmolekulares. Garlandwissenschaft, New York.
- Brownstein, Z., Abu-Rayyan, a., Karfunkel-don, d., Sirigu, s., Davido, geb., Shohat, m., Frydman, m., Houdusse, a., Kanaan, m., Avraham, k. 2014. Neuartige Myosinmutationen für erblicher Hörverlust, die durch gezielte genomische Einfassung und massiv parallele Sequenzierung schwelfte. European Journal of Human Genetics, 22: 768-775.
- Courson, d.S. und Cheney, r.UND. 2015. Myosin-X und Krankheit. Experimentelle Zellforschung, 334: 10-15.
- Lodisch, h., Berk, a., Zipurski, s.L., Matsudaria, p., Baltimore, d., Darnell, J. 2003. Zell- und Molekularbiologie. Editorial Medica Panamericana, Buenos Aires, Bogotá, Caracas, Madrid, Mexiko, Sāo Paulo.
- Schliwa, m. und Weehlke, G. 2003. Molekulare Motoren. Nature, 422: 759 - 765.
- Wert sein.D. 2003. Die molekulare Werkzeugkiste für intazelluläre Transport. Zelle, 112: 467-480.
- « Exonuklease -Eigenschaften, Struktur und Funktionen
- Bromo -Geschichte, Struktur, elektronische Konfiguration, Eigenschaften, verwendet »

