Heisenberg Atomic Model
- 2216
- 630
- Tizian Liebich
Was ist Heisenbergs Atommodell?
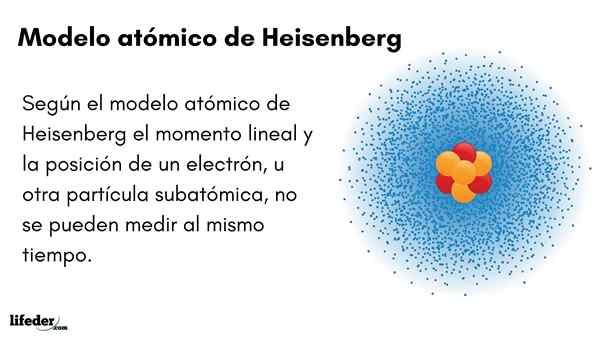
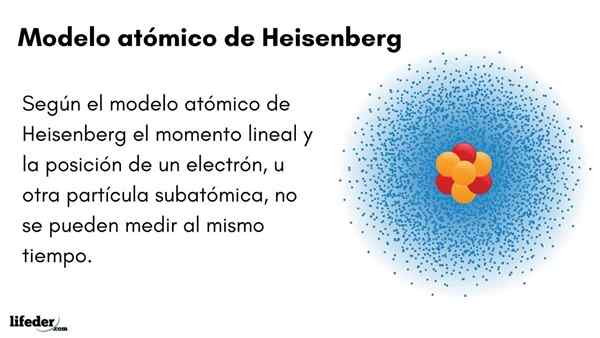
Er Heisenberg Atomic Model (1927) führt das Unsicherheitsprinzip in Elektronenorbitalen ein, die den Atomkern umgeben. Der herausragende deutsche Physiker stellte die Grundlagen der Quantenmechanik fest, um das Verhalten von subatomaren Partikeln abzuschätzen, aus denen ein Atom besteht.
Das Unsicherheitsprinzip von Werner Heisenberg zeigt an, dass es nicht möglich ist, die lineare Position eines Elektrons gleichzeitig mit Sicherheit zu kennen. Das gleiche Prinzip gilt für Zeit- und Energievariablen; Das heißt, wenn wir einen Hinweis auf die Position des Elektrons haben, werden wir den linearen Moment des Elektrons ignorieren und umgekehrt.
Kurz gesagt, es ist nicht möglich, den Wert beider Variablen gleichzeitig vorherzusagen. Die oben genannte bedeutet nicht, dass eine der zuvor erwähnten Größen nicht mit Präzision bekannt sein kann. Wann immer es getrennt ist, gibt es kein Hindernis, den Wert von Interesse zu erhalten.
Unsicherheit findet jedoch statt.
Dieses Prinzip entsteht aufgrund streng theoretischer Argumentation als einzig praktikable Erklärung, um Grund für wissenschaftliche Beobachtungen zu geben.
Eigenschaften des Heisenberg -Atommodells
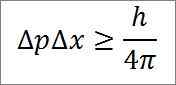 Werner Heisenberg
Werner Heisenberg Im März 1927 veröffentlichte Heisenberg seine Arbeiten Über den Wahrnehmungsinhalt von Kinos- und Quantenmechanik, wo er das Prinzip der Unsicherheit oder Unbestimmtheit beschrieben hat.
Dieses Prinzip, das im von Heisenberg vorgeschlagenen Atommodell von grundlegender Bedeutung ist, ist durch Folgendes gekennzeichnet:
- Das Unsicherheitsprinzip entsteht als Erklärung, die die neuen Atomtheorien über das Elektronenverhalten ergänzt. Trotz der Verwendung von Messinstrumenten mit hoher Präzision und Empfindlichkeit ist in jeder experimentellen Studie noch unbestimmt vorhanden.
- Aufgrund des Unsicherheitsprinzips erhöht sich bei der Analyse von zwei verwandten Variablen, wenn Sie eine genaue Kenntnis eines davon haben.
- Das lineare Moment und die Position eines Elektrons oder eines anderen subatomaren Teilchens können nicht gleichzeitig gemessen werden.
- Die Beziehung zwischen beiden Variablen wird durch eine Ungleichheit angegeben. Laut Heisenberg das Produkt der Variationen des linearen Moments -3. 4 Jules x Sekunden) und 4π, wie im folgenden mathematischen Ausdruck beschrieben:
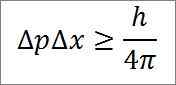
Die Legende, die diesem Ausdruck entspricht, lautet wie folgt:
∆P: Unbestimmung des linearen Moments.
∆x: Unbestimmung der Position.
H: Plankenkonstante.
π: PI 3.14 Zahl.
- In Anbetracht der oben genannten ist das Produkt der Unsicherheiten als niedrigere Beziehung die Beziehung h/4π, was ein konstanter Wert ist. Wenn eine der Größen zu Null kommt, muss der andere im gleichen Anteil zunehmen.
- Diese Beziehung gilt für alle Paare konjugierter kanonischer Größen. Zum Beispiel: Heisenbergs Unsicherheitsprinzip ist perfekt für das Energy-Time-Duo anwendbar, wie unten beschrieben:
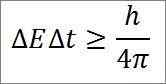
In diesem Ausdruck:
∆E: Energieunwirklichkeit.
∆t: Unbestimmtheit der Zeit.
H: Plankenkonstante.
π: PI 3.14 Zahl.
- Aus diesem Modell folgt, dass der absolute kausale Determinismus in konjugierten kanonischen Variablen unmöglich ist, da die Kenntnis der ursprünglichen Werte der Studienvariablen festgelegt werden sollte, um diese Beziehung herzustellen.
- Folglich basiert das Heisenberg -Modell aufgrund der Zufälligkeit, die zwischen den Variablen und subatomarer Ebene besteht.
Experimentelle Tests
Das Unsicherheitsprinzip von Heisenberg entsteht die einzige mögliche Erklärung für die experimentellen Tests, die in den ersten drei Jahrzehnten des 21. Jahrhunderts stattgefunden haben.
Bevor Heisenberg das Unsicherheitsprinzip aussprach, schlugen die in Kraft gewellten Vorschriften bis dahin vor.
Dies bedeutete, dass sie so behandelt wurden, als wären sie klassische Physik; Das heißt, ein Anfangswert wurde gemessen und der Endwert wurde nach dem vorabgestellten Verfahren geschätzt.
Kann Ihnen dienen: VektorgrößeDas obige bedeutete das Definieren eines Referenzsystems für Messungen, das Messinstrument und die Form der Verwendung des Instruments gemäß der wissenschaftlichen Methode.
Danach mussten sich die von subatomaren Partikeln beschriebenen Variablen deterministisch verhalten. Das heißt, sein Verhalten sollte genau und genau vorhergesagt werden.
Jedes Mal, wenn ein Aufsatz dieser Art durchgeführt wurde, war es unmöglich, den geschätzten Wert theoretisch in der Messung zu erhalten.
Die Maßnahmen wurden aufgrund der natürlichen Bedingungen des Experiments falsch dargestellt, und das erzielte Ergebnis war nicht nützlich, um die Atomtheorie zu bereichern.
Beispiel
Zum Beispiel: Wenn es darum geht, die Geschwindigkeit und Position eines Elektrons zu messen, muss die Montage des Experiments den Zusammenstoß eines Lichtphotons mit dem Elektron in Betracht ziehen.
Diese Kollision induziert eine Variation der intrinsischen Geschwindigkeit und Position des Elektrons, so dass das Objekt der Messung durch experimentelle Bedingungen verändert wird.
Daher fördert der Forscher das Auftreten eines unvermeidlichen experimentellen Fehlers trotz der Genauigkeit und Präzision der verwendeten Instrumente.
Quantenmechanik als klassische Mechanik
Zusätzlich zu dem oben genannten ist das Heisenberg -Unbestimmtheitsprinzip festgestellt, dass die Quantenmechanik per Definition in Bezug auf die klassische Mechanik anders funktioniert.
Infolgedessen wird angenommen, dass die genaue Kenntnis der subatomarischen Maßnahmen durch die dünne Linie begrenzt wird, die die klassische und die Quantenmechanik trennt.
Heisenberg Modellbeschränkungen
Obwohl Heisenbergs Atommodell die Unbestimmtheit von subatomaren Partikeln erklärt und die Unterschiede zwischen der klassischen und der Quantenmechanik sitzt.
Kann Ihnen dienen: Gravitationsenergie: Formeln, Eigenschaften, Anwendungen, ÜbungenDarüber hinaus impliziert die Tatsache, dass die Beziehung durch eine Ungleichheit hergestellt wird. Folglich ist die Unsicherheit, die den subatomischen Prozessen innewohnt, signifikant.
Artikel von Interesse
Schrödinger Atommodell.
Broglie Atomic Model.
Chadwick Atomic Model.
Perrin Atommodell.
Thomson Atomic Model.
Dalton Atomic Model.
Dirac Jordan Atomic Model.
Democritus Atomic Model.
Leucipo -Atommodell.
BOHR -Atommodell.
Sommerfeld Atommodell.
Aktuelles Atommodell.
Verweise
- Beyler, r. (1998). Werner Heisenberg. Encyclopædia Britannica, Inc. Erholt von: Britannica.com
- Heisenbergs Unsicherheitsprinzip (s).F.). Erholt von: Hiru.EUS
- Garcia, J. (2012). Heisenberg Unsicherheitsprinzip. Erholt von: Hiberus.com
- Atommodelle (s).F.). Nationale autonome Universität von Mexiko. Mexiko-Stadt, Mexiko. Erholt von: Beratung.Cuautitlan2.Unam.mx
- Werner Heisenberg (s.F.).Abgerufen von: The History-Off-the-Atom.Wikispaces.com
- Wikipedia, Free Encyclopedia (2018). Plankenkonstante. Geborgen von: ist.Wikipedia.Org
- Wikipedia, Free Encyclopedia (2018). Heisenberg Unbestimmtes Beziehung. Geborgen von: ist.Wikipedia.Org

