Carnot -Maschine
- 4063
- 996
- Luca Holdt
Was ist die Carnot -Maschine??
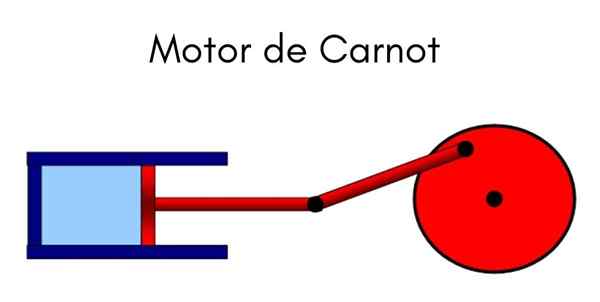
Der Carnot -Maschine Es ist ein ideales zyklisches Modell, bei dem Wärme verwendet wird, um einen Job zu machen. Das System kann als Kolben verstanden werden, der sich in einem Zylinder bewegt, der ein Gas komprimiert. Der ausgeübte Zyklus ist der von Carnot, der vom Vater der Thermodynamik, dem französischen Physiker und Ingenieur Nicolas Leonard Sadi Carnot, erklärt wird.
Carnot gab diesen Zyklus im frühen neunzehnten Jahrhundert an. Die Maschine wird vier staatlichen Variationen unterzogen, wechselende Bedingungen wie konstanter Temperatur und Druck, wobei eine Variation des Volumens bei der Komprimierung und Ausdehnung von Gas belegt wird.
Formeln
Laut Carnot können die ideale Maschine Temperatur- und Druckschwankungen ausgesetzt werden, es ist möglich, die erhaltene Leistung zu maximieren.
Der Carnot -Zyklus muss in jeder seiner vier Phasen getrennt analysiert werden.
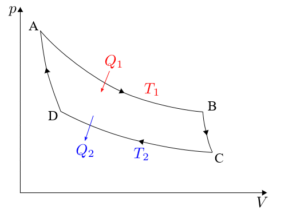
Die mit jeder der auf der Carnot -Maschine ausgeübten Zyklus ausgeübten Formeln sind nachstehend detailliert.
Isothermische Ausdehnung (a → B)
Die Räumlichkeiten dieser Phase sind die folgenden:
- Gasvolumen: Es geht vom Mindestvolumen auf ein durchschnittliches Volumen aus.
- Maschinentemperatur: konstante Temperatur T1, hoher Wert (T1> T2).
- Maschinendruck: Steigen von P1 nach P2 ab.
Der isotherme Prozess impliziert, dass die Temperatur T1 in dieser Phase nicht variiert. Wärmeübertragung induziert eine Gasausdehnung, die Bewegung auf dem Kolben induziert und mechanische Arbeit erzeugt.
Bei der Erweiterung stellt das Gas eine gewisse Abkühlen vor. Es absorbiert jedoch die von der Temperaturquelle emittierte Wärme und bei der Ausdehnung die konstante Temperatur beibehält.
Kann Ihnen dienen: Was ist die lineare Geschwindigkeit?? (Mit gelösten Übungen)Da die Temperatur während dieses Prozesses konstant bleibt, ändert sich die innere Energie des Gases nicht und die gesamte vom Gas absorbierte Wärme wird effektiv in die Arbeit umgewandelt. So:
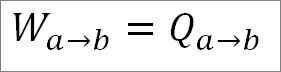
Andererseits ist es am Ende dieser Phase des Zyklus auch möglich, den Druckwert unter Verwendung der idealen Gasgleichung dafür zu erhalten. Auf diese Weise haben Sie Folgendes:
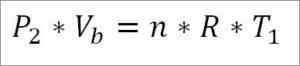
In diesem Ausdruck:
- P2: Druck am Ende der Phase.
- VB: Volumen an Punkt B.
- N: Anzahl der Gasmolen.
- A: Universelle Konstante ideale Gase. R = 0,082 (atm*liter)/(moles*k).
- T1: Absolute Anfangstemperatur, Kelvin -Grad.
Adiabatische Expansion (B → C)
Während dieser Phase des Prozesses wird die Gasausdehnung durchgeführt, ohne den Wärme auszutauschen. Auf diese Weise sind die Räumlichkeiten unten detailliert:
- Gasvolumen: Es geht vom durchschnittlichen Volumen auf ein maximales Volumen aus.
- Maschinentemperatur: Steigen von t1 nach t2 ab.
- Maschinendruck: Konstante P2 -Druck.
Der adiabatische Prozess impliziert, dass der P2 -Druck während dieser Phase nicht variiert. Die Temperatur nimmt ab und das Gas erweitert sich weiter, bis es das Maximum seines Volumens erreicht. Das heißt, der Kolben erreicht die Spitze.
In diesem Fall stammt die geleistete Arbeit aus der inneren Energie des Gases und sein Wert ist negativ, da die Energie während dieses Prozesses abnimmt.
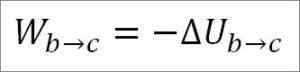
Angenommen, es ist ein ideales Gas, wird die Theorie behauptet, dass Gasmoleküle nur kinetische Energie haben. Nach den Prinzipien der Thermodynamik kann dies durch die folgende Formel abgeleitet werden:
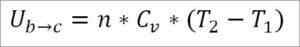
In dieser Formel:
- ∆UB → c: Interne Energievariation des idealen Gases zwischen den Punkten B und C.
- N: Anzahl der Gasmolen.
- Lebenslauf: Gasmolarwärmekapazität.
- T1: Absolute Anfangstemperatur, Kelvin -Grad.
- T2: Absolute Endtemperatur, Kelvin Grad.
Isotermische Kompression (C → D)
In dieser Phase beginnt die Kompression von Gas; Das heißt, der Kolben wird in den Zylinder mobilisiert, mit dem das Gas seinen Volumen zusammenbringt.
Die in diesem Prozess innewohnenden Bedingungen sind nachstehend detailliert:
- Gasvolumen: Es verläuft vom maximalen Volumen zu einem Zwischenvolumen.
- Maschinentemperatur: konstante Temperatur T2, reduzierter Wert (T2 < T1).
- Maschinendruck: Erhöhen Sie von P2 auf P1.
Hier nimmt der Druck auf das Gas zu, so beginnt es zu komprimieren. Die Temperatur bleibt jedoch konstant und daher ist die interne Energieschwankung des Gases Null.
Analog zur isothermen Expansion, die durchgeführte Arbeit ist gleich der Hitze des Systems. So:
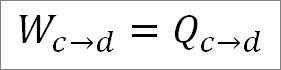
Es ist auch machbar, den Druck an diesem Punkt unter Verwendung der idealen Gasgleichung zu finden.
Adiabatische Komprimierung (D → A)
Dies ist die letzte Phase des Prozesses, in der das System zu seinen Anfangsbedingungen zurückkehrt. Dazu werden die folgenden Bedingungen berücksichtigt:
- Gasvolumen: Es geht von einem Zwischenvolumen zu einem Mindestvolumen.
- Maschinentemperatur: Erhöhen Sie von T2 auf T1.
- Maschinendruck: konstanter Druck P1.
Die in die vorherige Phase in das System eingebaute Wärmequelle wird entfernt, sodass das ideale Gas seine Temperatur in der Zwischenzeit erhöht. Der Druck bleibt konstant.
Das Gas kehrt zu den Anfangstemperaturbedingungen (T1) und in seinem Volumen zurück (minimal). Wieder einmal stammt die Arbeit aus der inneren Energie des Gases, sodass Sie:
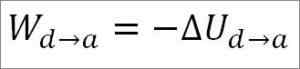
Ähnlich wie bei adiabatischer Expansion ist es möglich, die Variation der Gasenergie durch den folgenden mathematischen Ausdruck zu erhalten:
Kann Ihnen dienen: Calciumfluorid (CAF2): Struktur, Eigenschaften, verwendet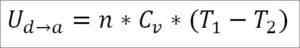
Wie funktioniert die Carnot -Maschine??
Die Carnot -Maschine arbeitet als Motor, bei dem die Leistung durch Variation isothermischer und adiabatischer Prozesse maximiert wird, wobei die Ausdehnungsphasen und das Verständnis eines idealen Gases abwechseln.
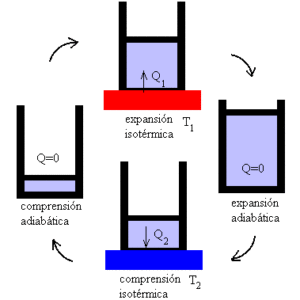
Der Mechanismus kann als ideales Gerät verstanden werden, das einen Job ausübt.
Im ersten Fokus ist das System einer T1 -Temperatur ausgesetzt. Es ist eine hohe Temperatur, die das System zur Spannung unterwirft und Gasausdehnung erzeugt.
Dies führt wiederum in der Ausführung einer mechanischen Arbeit, die die Mobilisierung des Kolbens aus dem Zylinder ermöglicht und deren Grenze nur durch adiabatische Expansion möglich ist.
Dann kommt der zweite Fokus, in dem das System einer T2 -Temperatur weniger als T1 ausgesetzt ist. Das heißt, der Mechanismus unterliegt der Kühlung.
Dies induziert Wärmeextraktion und Gasquetikan.
Anwendungen
Die Carnot -Maschine wurde aufgrund ihres Beitrags zum Verständnis der wichtigsten Aspekte der Thermodynamik häufig verwendet.
Mit diesem Modell können Sie die Variationen der idealen Gase klar verstehen, die Temperatur- und Druckänderungen unterliegen, was eine Referenzmethode ist.