Methoden zur Trennung homogener Gemische
- 1731
- 78
- Said Ganzmann
Der Methoden zur Trennung homogener Gemische Sie sind alle, die ohne chemische Reaktionen die Komponenten oder gelöste Stoffe ermöglichen, die dieselbe Phase integrieren. das heißt, von Flüssigkeit, Feststoff oder Gas.
Solche homogenen Gemische bestehen aus Lösungen, bei denen gelöste Partikel zu klein sind, um sie mit bloßem Auge zu unterscheiden. Sie sind so klein, dass es keine schmalen oder selektiven Filter gibt, die sie beibehalten, während die Lösung sie überträgt. Auch Techniken wie Zentrifugation oder Magnetisierung helfen Ihrer Trennung auch nicht.
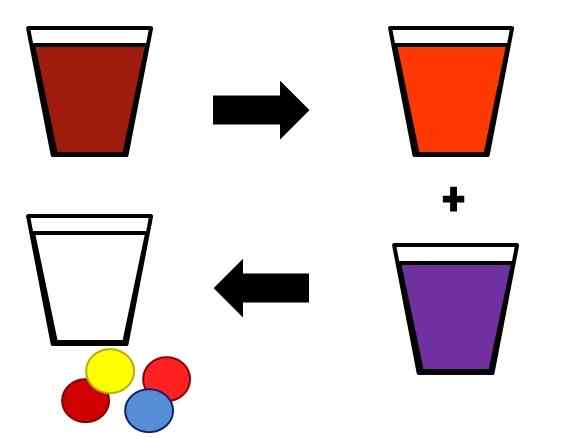 Illustratives Beispiel dafür, wie sich homogene Gemische in Stufen trennen können. Quelle: Gabriel Bolívar.
Illustratives Beispiel dafür, wie sich homogene Gemische in Stufen trennen können. Quelle: Gabriel Bolívar. Ein Beispiel dafür, wie Lösungen in ihren Komponenten getrennt sind. Die anfängliche Mischung (braun) wird in zwei Komponenten unterteilt, gleichermaßen homogen (orange und lila). Schließlich werden aus den beiden resultierenden Gemischen, das Lösungsmittel (weiß) und die vier jeweiligen Paare von gelösten Stoff (rot-gelb und rotblau) erhalten.
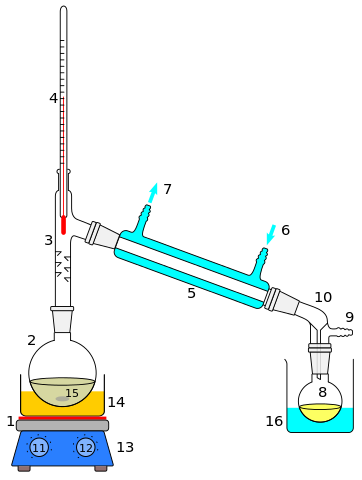
Unter den Methoden oder Techniken der Trennung von Lösungen werden wir Verdunstung, Destillation, Chromatographie und fraktionierte Kristallisation vornehmen. Abhängig von der Komplexität der Mischung sollten mehr als eine dieser Methoden angewendet werden, bis sie die Homogenität bricht.
[TOC]
Die Hauptmethoden zur Trennung von Gemischen
- Verdunstung
 Verdunstung ist die einfachste Methode, um homogene Gemische von einem einzelnen gelösten Stoff zu trennen.
Verdunstung ist die einfachste Methode, um homogene Gemische von einem einzelnen gelösten Stoff zu trennen. Die einfachsten homogenen Gemische sind die Lösungen, bei denen ein einzelner gelöster Stoff aufgelöst wurde. Zum Beispiel gibt es im überlegenen Bild eine farbenfrohe Lösung aufgrund der Absorption und Reflexion von sichtbarem Licht mit den Partikeln seines gelösten Stoffes.
Wenn es während seiner Vorbereitung gut gerührt hat, gibt es keine klareren oder dunklen Regionen als andere; Sie sind alle gleich, Uniformen. Solche farbenfrohen Partikel können nicht durch eine mechanische Methode vom Lösungsmittel getrennt werden, sodass Sie Energie im Wärme (roter Dreieck) benötigen, um dies zu erreichen.
Es kann Ihnen dienen: Kohlenstoffdisulfid (CS2): Struktur, Eigenschaften, Verwendungen, RisikenSomit wird die farbenfrohe Lösung offen erhitzt, um zu beschleunigen und die Verdunstung des Lösungsmittels außerhalb seines Behälters zu ermöglichen. Damit nimmt das Volumen, das die gelösten Partikel trennt.
Das Endergebnis ist, dass der farbenfrohe gelöste Stoff am unteren Rand des Behälters bleibt und das Lösungsmittel vollständig verdunstet ist.
Die Unannehmlichkeit bei der Verdunstung ist, dass sein Ziel, das Lösungsmittel zu beseitigen, anstatt die gelösten Stoffe zu trennen, indem er es auf seinen Siedepunkt erhitzt. Der verbleibende Feststoff kann aus mehr als einem gelösten gelösten Stoff bestehen und wird daher von anderen Trennungsmethoden benötigt, um ihn in seinen isolierten Komponenten zu definieren.
- Destillation
 Destillation
Destillation Destillation ist möglicherweise die Methode zur Trennung homogener Lösungen oder Gemische. Die Verwendung erstreckt sich bis zu geschmolzenen Salzen oder Metallen, kondensierten Gasen, Lösungsmittelmischungen oder organischen Extrakten. Der gelöste gelöste ist die meiste Zeit eine Flüssigkeit, deren Siedepunkt in mehreren Grad in Bezug auf das Lösungsmittel unterscheidet.
Wenn der Unterschied zwischen solchen Siedepunkten hoch ist (mehr als 70 ºC), wird eine einfache Destillation verwendet; Und wenn nicht, dann wird eine fraktionale Destillation durchgeführt. Beide Destillationen haben mehrere Ansammlungen oder Konstruktionen sowie eine andere Methodik für Gemische unterschiedlicher chemischer Natur (flüchtig, reaktiv, polar, apolar usw.).
Bei der Destillation bleiben sowohl Lösungsmittel als auch gelöste Stoffe erhalten, und dies ist einer der Hauptunterschiede in Bezug auf die Verdunstung.
Die Rotaevaporation kombiniert jedoch diese beiden Aspekte: ein flüssiges oder flüssiges Flüssigkeitsmisch Öl bleibt im anfänglichen Behälter.
Kann Ihnen dienen: Periodenzüchter, wofür ist esLuftdestillation
Kondensatluft wird einer kryogenen fraktionalen Destillation ausgesetzt, um Sauerstoff, Stickstoff, Argon, Neon usw. zu trennen. Die Luft, eine homogene gasförmige Mischung, wird in eine Flüssigkeit verwandelt, in der Stickstoff, da es sich um die Mehrheitsbaut handelt, theoretisch als Lösungsmittel wirkt; Und die anderen Gase, ebenfalls kondensiert, als flüssige gelöste gelöste.
- Chromatographie
Die Chromatographie kann im Gegensatz zu anderen Techniken keine Erträge oder ähnliche Ausbilder liefern. Das heißt, es ist nicht nützlich, eine ganze Mischung zu verarbeiten, sondern einen unbedeutenden Teil desselben. Die von ihnen bereitgestellten Informationen sind jedoch analytisch wertvoll, da sie Gemische anhand seiner Zusammensetzung identifiziert und klassifiziert.
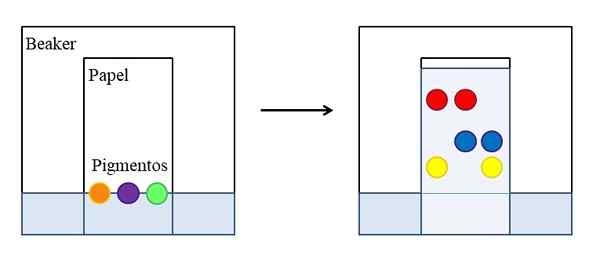 Papier- oder Feinschichtschromatographie. Quelle: Gabriel Bolívar.
Papier- oder Feinschichtschromatographie. Quelle: Gabriel Bolívar. Es gibt verschiedene Arten von Chromatographien, aber die einfachste, die in den Schulen oder Kursen vor der Universität erklärt wird, ist das des Papier ).
Das obere Bild zeigt, dass in einem Becher mit Wasser oder einem bestimmten Lösungsmittel ein Papier platziert wird, das als Referenzlinie mit Tropfen oder Punkten von drei ausgewählten Pigmenten (orange, lila und grün) gekennzeichnet wurde. Der Becher bleibt geschlossen, damit der Druck konstant ist und vor den Lösungsmitteldämpfern gesättigt ist.
Dann beginnt die Flüssigkeit am Papier aufzusteigen und die Pigmente zu ziehen. Die Wechselwirkungen zwischen Pigmentabsen sind nicht alle gleich: Einige sind stärker und andere schwächer. Je mehr Affinität das Pigment für das Papier empfindet, desto weniger wird es in Bezug auf die ursprünglich gekennzeichnete Linie durch das Papier aufsteigen.
Kann Ihnen dienen: GeschwindigkeitskonstanteZum Beispiel: Das rote Pigment ist dasjenige, das sich weniger Affinität zum Lösungsmittel anfühlt, während das Gelb kaum aufstieg, weil das Papier es mehr behält. Es wird dann gesagt, dass das Lösungsmittel die mobile Phase und das Papier der stationären Phase ist.
- Bruchkristallisation
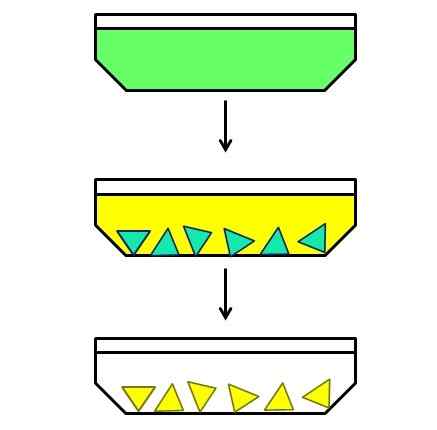 Illustratives Beispiel für die fraktionierte Kristallisation. Quelle: Gabriel Bolívar.
Illustratives Beispiel für die fraktionierte Kristallisation. Quelle: Gabriel Bolívar. Und schließlich haben Sie fraktionale Kristallisation. Diese Methode könnte vielleicht wie ein Hybrid katalogisieren, da sie von einer homogenen Mischung aus beginnt, um eine Heterogen zu beenden. Nehmen wir beispielsweise an, dass es eine Lösung gibt, in der ein grünes Feststoff aufgelöst wurde (überlegenes Bild).
Grüne Partikel sind zu klein, um manuell oder mechanisch zu trennen. Es ist auch so, dass der grüne Feststoff eine Mischung aus zwei Komponenten und keine einzelne Verbindung dieser Farbe ist.
Dann ist eine Lösung davon erhitzt und während des Abkühlens in Ruhe gelassen. Es stellt sich heraus, dass die beiden Komponenten, obwohl sie sehr miteinander verwandt sind, ihr Lösungsmittellösungsmittel leicht unterschiedlich sind. Daher beginnt einer der beiden zuerst und dann der andere, zuerst zu kristallisieren.
Die grün-blaue Komponente (in der Mitte des Bildes) ist die erste, die sich kristallisiert, während die gelbe Komponente noch gelöst ist. Da sie grün-blaue Kristalle sind, sind sie heiß, bevor gelbe Kristalle auftreten. Dann kristallisiert das Lösungsmittel etwas mehr, und eine weitere Filtration wird gemacht.
Themen von Interesse
Mischungsgetrennmethoden.
Methoden zur Trennung heterogener Gemische.
Mischungen: Komponenten und Typen.
Homogene Gemische.
Heterogene Gemische.
Verweise
- Whitten, Davis, Peck & Stanley. (2008). Chemie. (8. Aufl.). Cengage Lernen.
- Chelsea Schuyler. (2019). Chromatographie, Distillion und Filterion: Methoden zur Trennung von Gemischen. Lernen. Erholt von: Studium.com
- CK-12 Foundation. (16. Oktober 2019). Methoden zum Trennen von Gemischen. Chemistry Librettexts. Erholt von: Chem.Librettexts.Org
- Gute Wissenschaft. (2019). Trennung von Gemischen. Erholt von: GoodScience.com.Au
- Clark Jim. (2007). Dünnschichtchromatographie. Erholt von: Chemguide.CO.Vereinigtes Königreich
- « Versprochene (PM) Struktur, Eigenschaften, erhalten, verwendet, verwendet
- Metallinguistische Funktionseigenschaften, Funktionen und Beispiele »

