Pencanona Chemische Struktur, Eigenschaften, Synthese, verwendet
- 2450
- 605
- Medine Kedzierski
Der Pentanona Es ist eine organische Verbindung, die zur Familie der Ketone gehört, deren chemische Formel C ist5H10ENTWEDER. Es bleibt eines der einfachsten Ketone und besteht aus einer farblosen Flüssigkeit mit einem Aroma ähnlich wie Aceton. Von nun an präsentieren die Ketone in Bezug auf die Kohlenstoff Anzahl ihres Skeletts Isomer Position.
Wenn Sie über Position sprechen, bezieht sich Isomeria darauf, wo sich die Carbonylgruppe befindet, c = o. Somit besteht Puntanona tatsächlich aus zwei Verbindungen mit physikalischen Eigenschaften, die kaum voneinander unterscheiden: 2-Penon und 3-Penon (niedrigeres Bild). Beide sind flüssig, aber ihre Siedepunkte sind gleich, daher können sie nicht durch Destillation getrennt werden.
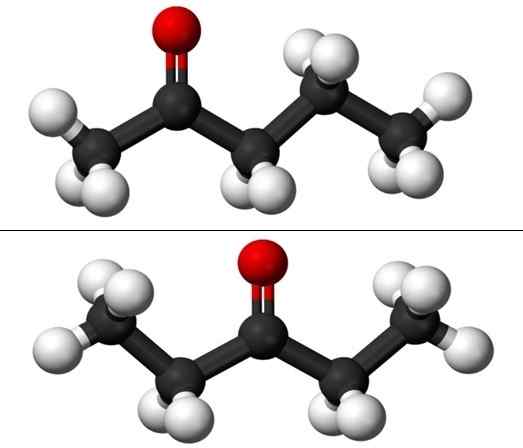
 Moleküle der Positionisomere für Pentanona. Quelle: Jynto & Ben Mills über Wikipedia.
Moleküle der Positionisomere für Pentanona. Quelle: Jynto & Ben Mills über Wikipedia. Jedes der beiden Pentanone hat jedoch eine eigene Syntheseroute, daher ist es unwahrscheinlich, dass es eine Mischung aus ihnen gibt. Mischung, die durch Einfrieren machbar sein kann.
Seine Verwendungen sind eingeschränkt, insbesondere als organische Lösungsmittel. Alternativen zu Aceton in Medien, bei denen Sie mit einer Temperatur über dem niedrigen Siedepunkt arbeiten. Sie sind auch Ausgangsmaterialien für andere organische Synthese, da ihre Gruppe C = o nucleophile Zugabe reduzieren oder leiden kann.
[TOC]
Chemische Struktur
Isomere positionieren
Im Bild haben wir die molekularen Strukturen der beiden Positions -Isomere für das Puntanona, die durch ein Modell von Kugeln und Stäben dargestellt werden. Die schwarzen Kugeln entsprechen kohlensäurehaltige Skelette, weiße bis Wasserstoffatome und roten Sauerstoffatomen in Gruppe C = o.
2-Pintanon
Das 2-Ponanona (oben) hat Gruppe C = oder im zweiten Kohlenstoff, was gleich ist, wenn es im Raum war; Das heißt, das 2-Ponanona und das 4-Pantanona sind gleichwertig, da es ausreicht, um sie 180º zu drehen, damit ihre Strukturen gleich sind.
Kann Ihnen dienen: Kohlenstofftetrachlor (CCL4)Links von C = O haben Sie einen Methylradikal, Cho3-, Und zu seiner Rechten ein radikaler Propil. Aus diesem Grund erhält diese Cetona auch den Namen (weniger verwendet) von Metil Propil Cetona (MPK in Englisch). Sie können die Asymmetrie dieser Struktur auf den ersten Blick sehen.
3-Penon
Das 3-Péntanona (unten) hat Gruppe C = O im dritten Kohlenstoff. Beachten Sie, dass dieses Isomer eine größere Version von Aceton ist und dass es auch sehr symmetrisch ist; Die beiden Radikale an den Seiten der Gruppe C = O sind gleich: zwei Ethylradikale, CH3CH2-. Deshalb heißt das 3-Pananona auch Cetona Deriestil (oder Dimethylaceton).
Intermolekulare Wechselwirkungen
Das Vorhandensein der Carbonylgruppe, sowohl im 2-Pantanon als auch im 3-Penona, verleiht dem Molekül Polarität.
Daher können beide Pentanona-Isomere über Dipol-Dipol miteinander interagieren.
Ebenso intervenieren die Londoner -Dispersionskräfte zwischen Kohlenstoff und hydrierten Skeletten in geringerem Maße.
Durch das Puntanona, ein größerer molekularer Bereich und eine größere Masse im Vergleich zu denen des Aceton, trägt dieser Beitrag zu seinem Dipolmoment bei und ermöglicht einen höheren Siedepunkt (102 ° C> 56 ° C), um einen höheren Siedepunkt zu besitzen). Tatsächlich verdampfen die beiden Isomere bei 102 ºC; während sie bei verschiedenen Temperaturen einfrieren.
Kristalle
Wahrscheinlich spielen die Symmetrien in der Kristallisierung eine wichtige Rolle. Zum Beispiel beträgt der Fusionspunkt des 2 -Pantanonas -78 ºC, während der 3 -Péntanona, -39 ºC.
Kann Ihnen dienen: Avogadro -GesetzDies bedeutet, dass 3-Pantanona-Kristalle gegen die Temperatur stabiler sind; Seine Moleküle sind kohärsiver und erfordern mehr Wärme, um sich in der flüssigen Phase zu trennen.
Wenn es eine Mischung aus beiden Isomeren gäbe, wäre der 3-Penon der erste, der sich kristallisierte und schließlich der 2-Pananona bei einer niedrigeren Temperatur ist. Die symmetrischeren 3-Pantanon-Moleküle des 3-Pantanons sind leichter ausgerichtet als die von 2-Ponanona: asymmetrisch und gleichzeitig dynamischer.
Eigenschaften
Aussehen
Farblose Flüssigkeiten mit einem Aroma ähnlich dem von Aceton.
Molmasse
86,13 g/mol
Dichte
0,81 g/ml (3-Ponanona)
0,809 g/ml (2-Ponanona)
Schmelzpunkt
-78 ºC (2-Ponanona)
-39 ºC (3-Ponanona)
Siedepunkt
102 ºC (für beide Isomere)
Wasserlöslichkeit
35 g/l (3-Ponenona)
60 g/l (2-Ponenona)
Dampfdruck
35 mmHg (3-Ponenona)
270 mmHg (2-Pantanon) bei 20 ºC
Diese Werte sind nicht nützlich, um den Dampfdruck beider Isomere direkt zu vergleichen.
Flammpunkt
12,78 ºC (3-Ponanona)
10 ºC (2-Ponanona)
Stabilität
Die beiden Pentanona -Isomere sind extrem brennbar, daher müssen sie so weit von jeder Wärmequelle entfernt bleiben. Blitzpunkte zeigen, dass eine Flamme die Dämpfe beider Pentanas auch bei einer Temperatur von 10 ° C einstellen kann.
Synthese
Obwohl die beiden Pentanona -Isomere physisch und chemisch sehr ähnlich sind, sind ihre synthetischen Routen unabhängig vom anderen, daher ist es unwahrscheinlich, dass beide in derselben Synthese erhalten werden.
2-Pintanon
Ausgehend von dem 2-Penol. Oxidation wäre:
Es kann Ihnen dienen: keine Elektrolyte: Eigenschaften und Beispiele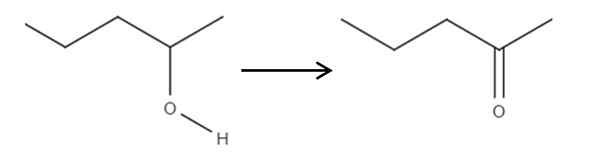 Oxidation von 2-Pantanol in 2-Pantanona. Quelle: Gabriel Bolívar.
Oxidation von 2-Pantanol in 2-Pantanona. Quelle: Gabriel Bolívar. Einfach der C-OH-Link wird c = o. Es gibt andere Methoden, um die 2-Penona zu synthetisieren, aber dies ist am einfachsten zu verstehen.
3-Penon
Der 3-Pintanon kann mittels synthetisiert werden3CH2Cooh. Diese synthetische Route erzeugt symmetrische Ketone und ist ein Cho -Molekül3COOH wird die Cooh -Gruppe in Form von CO verlieren2, Während die andere Ihre Gruppe oh in Form von H2ENTWEDER:
2ch3CH2Cooh => ch3CH2Coch2CH3 + CO2 + H2ENTWEDER
Eine weitere etwas komplexere Route besteht darin, eine Mischung aus Ethylen direkt zu reagieren, Cho2= Ch2, CO2 und h2 Die 3-Ponanona bilden.
Anwendungen
Sofern die Anwendung nicht sehr streng ist, handelt es sich um eine spezifische Synthese, oder dass es auch gezeigt wurde Verwendet.
Das heißt, "Es spielt keine Rolle", wenn Sie das 2-Ponanona oder 3-Penona als Lösungsmittel für Gemälde oder Harze oder als elendes verwenden möchten, da die wichtigsten Kriterien zu seinem Preis und zur Verfügbarkeit werden. Der 3-Penon wird in der Automobilindustrie verwendet, um das Verhalten von Gasen in internen Verbrennungsmotoren zu untersuchen.
Verweise
- Morrison, r. T. und Boyd, r, n. (1987). Organische Chemie. 5. Ausgabe. Editorial Addison-Wesley Interamerikaner.
- Carey f. (2008). Organische Chemie. (Sechste Ausgabe). Mc Graw Hill.
- Graham Solomons t.W., Craig b. Braten. (2011). Organische Chemie. Amine. (10. Ausgabe.). Wiley Plus.
- Wikipedia. (2019). 3-Pain. Abgerufen von: in.Wikipedia.Org
- Nationales Zentrum für Biotechnologie Information. (2019). 2-Pontenon. Pubchem -Datenbank. CID = 7895. Erholt von: Pubchem.NCBI.NLM.NIH.Regierung
- Royal Society of Chemistry. (2019). 3-Pain. Erholt von: Chemspider.com
- Professor t. Nalli. (2013). Oxidation von 2-Pintanol und Destillation des Produkts. Erholt von: Kurs1.Winona.Edu
- « Paraguay Flagge Geschichte und Bedeutung
- Geschichte und Bedeutung der Vereinigten Königreichs Flagge »

