Äquivalentes Gewicht
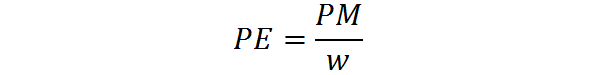
- 1037
- 50
- Ibrahim Steuk
Was ist das äquivalente Gewicht?
Er Äquivalentes Gewicht Es ist das Gewicht oder die Masse eines Substanzäquivalents. Das heißt, es ist das Gewicht oder die Masse eines Substanz.
Die normale Substanz, die als Referenz genommen wird. Normale Verbindungen reagieren immer mit Stöchiometrie 1: 1 miteinander.
Wenn wir beispielsweise über eine Säure-/Basenreaktion sprechen, wäre das äquivalente Gewicht einer Säure das Gewicht des zusammenhängenden zusammengesetzten Zusammenlebens zu 1 Mol einer normalen Säure, die ein einzelnes ionisierbares Proton hat.
Bevor bekannt war, dass Materie durch Atome und Moleküle gebildet wurde, war bereits eine Reihe von Gesetzen festgestellt.
Diese Gesetze bildeten die Grundlagen stöchiometrischer Berechnungen während der Anfänge der Chemie als Wissenschaft.
Das Konzept des Äquivalentgewichts hängt mit dieser frühen Phase der Entwicklung der Chemie zusammen. Als nächstes werden wir diskutieren, wie es berechnet wird, wofür es ist und einige gemeinsame Beispiele für Ihre Berechnung.
Formel und äquivalente Gewichtseinheiten
Das äquivalente Gewicht wird aus dem Molekulargewicht einer Substanz mittels der folgenden Formel berechnet:
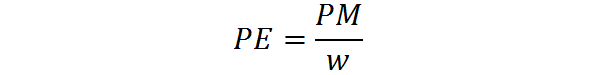
Wenn PE das äquivalente Gewicht ist, ist PM das Molekulargewicht oder die Molmasse der Substanz, und W repräsentiert die Anzahl der Äquivalente pro Mol.
Letzteres besteht immer aus einer Ganzzahl gleich oder größer als 1. Es repräsentiert die Anzahl der Moleküle eines „normalen“ Reagens, zu dem jedes Substanzmolekül äquivalent ist. Daher hängt es von der Art des fraglichen Reagenziens und der Art der chemischen Reaktion ab.
Kann Ihnen dienen: Dihydroxyaceton: Struktur, Eigenschaften, erhalten, verwendet, verwendetEs kann auch aus dem Teig, m und der Anzahl der Äquivalent berechnet werden:
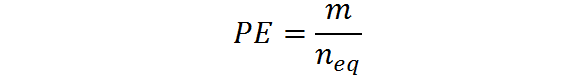
Äquivalente Gewichtseinheiten
Wie aus der vorherigen Formel ersichtlich ist, wird das äquivalente Gewicht in Masseneinheiten (normalerweise Gramm) zur Anzahl der Äquivalent ausgedrückt. Das heißt, die Einheiten sind g/EQ.
Der Wert von W In der ersten früheren Formel wird es in äquivalenten Einheiten auf Mol (Gl/Mol) exprimiert, während die Molmasse in Gramm über Mol (g/mol) exprimiert wird.
Was ist das äquivalente Gewicht für?
Der Hauptnutzen des äquivalenten Gewichts besteht darin, dass es die stöchiometrischen Berechnungen vereinfacht. Das äquivalente Gewicht einer Substanz entspricht einer anderen Substanz desselben Typs und für dieselbe Art der chemischen Reaktion. In der Tat erhält er von dort aus seinen Namen.
Auf diese Weise können wir stöchiometrische Berechnungen auf sehr einfache Weise und ohne die Notwendigkeit chemischer Gleichungen durchführen.
Wie wird das äquivalente Gewicht berechnet??
Wie wir bereits gesehen haben, wird das äquivalente Gewicht aus dem Molekulargewicht und der Anzahl der Äquivalente pro Mol oder W berechnet.
Berechnung des Molekulargewichts
Das Molekulargewicht einer Substanz wird durch Hinzufügen des Atomgewichts aller Atome bestimmt, die es ausmachen. Diese Atomgewichte befinden sich in der Periodenzüchtertabelle.
Bestimmung von W
Der Wert von W Für eine Substanz hängt es von der Art der Reaktion ab, an der sie beteiligt sind. Das heißt, es hängt von der Art des fraglichen Reagenzie ab. Für jede Art von Substanz gibt es eine andere Art der Bestimmung W.
Die folgende Tabelle zeigt, wie es bestimmt wird W Für verschiedene Fälle.
Es kann Ihnen dienen: Calciumhypochlorit (CA (CLO) 2)| Art des Reagens | Wert von W |
| Säuren | Anzahl der ionisierbaren Hydrogene für jedes Säuremolekül. |
| Basen | Anzahl der Protonen, die jedes Basenmolekül erfassen oder neutralisieren können oder neutralisieren können. |
| Oxidationsmittel | Anzahl der Elektronen, die jeden Mol Oxidationsmittel bei der Halbpause der Reduktion erfassen. |
| Reduzierende Agenten | Anzahl der Elektronen, die jedes Maulwurf reduzierender Mittel in der Oxidationssemi -Retaktion freigesetzt haben. |
| Du gehst raus | Gesamtzahl der positiven oder negativen Ladungen, die beim Salz erzeugt werden. |
| Neutrale Substanzen | 1 |
Es ist zu beachten, dass eine Substanz, wenn sie an mehr als einer Art chemischer Reaktion teilnehmen kann, mehr als einen Wert von haben kann W Und daher mehr als ein gleichwertiges Gewicht.
Bedeutung und Anwendungen des äquivalenten Gewichts
Das äquivalente Gewicht wird verwendet, um die Anzahl der Äquivalente einer Chemikalie zu berechnen. Diese Anzahl der Äquivalente entspricht immer der Anzahl der Äquivalente einer anderen Substanz, mit der sie reagiert.
Dies wird hauptsächlich in zwei verschiedenen Bereichen verwendet:
In der analytischen Chemie
Die Äquivalente werden häufig verwendet, um stöchiometrische Berechnungen in der analytischen Chemie zu erleichtern. Dies gilt insbesondere bei der volumetrischen und gravimetrischen Analyse.
Das Wissen über das Volumen des Grades am Punkt der Äquivalenz und der Konzentration des Titelartikels sowie des äquivalenten Gewichts des berechtigten Anspruch.
In der Elektrolyse
Im Bereich der Elektrolyse repräsentiert das äquivalente Gewicht das Gewicht eines Metalls oder einer anderen Substanz, die bei 96 auftreten kann.500 ° C Belastung durch elektrolytische Zelle. Dies erleichtert stöchiometrische und wirtschaftliche Berechnungen des Elektrolyseprozesses.
Kann Ihnen dienen: Quecksilberoxid (HG2O)Beispiele für die äquivalente Gewichtsberechnung
Kalzium
Das Atomgewicht von Kalzium beträgt 40 und dieses Metall bildet Kationen mit Valencia +2, so.
Schwefelsäure (h2SW4)
Das Molekulargewicht dieser Verbindung ist 98 und ist eine diprotische Säure so W = 2. Daher beträgt das äquivalente Gewicht PE: 98/2 = 49 g/gl/EQ.
Aluminiumhydroxid (AL (OH)3)
Aluminiumhydroxid (PM = 78) ist eine Amphoterverbindung, die als Säure und als Basis wirken kann.
Wenn Sie als Basis fungieren, indem Sie Ihre drei Hydroxide veröffentlichen, dann dann W = 3, Also PE: 78/3 = 26 g/Gl/EQ. Andererseits fängt es ein Wassermolekül ein und fördert ein Proton, W = 1 und pe = 78 g/gl/EQ.
Calciumphosphat (CA)3(Po4)2)
Calciumphosphat ist ein Salz, das beim Dissoziieren 3 CA -Ionen erzeugt2+ und 2 Ionen po43-.
In jedem Fall beträgt die Anzahl der Lasten des gleichen Vorzeichens, das jede Calciumphosphateinheit erzeugt W = 6 und pe = 310/6 = 51,67 g/gl/EQ.
Verweise
- Universelle Enzyklopädie (s). F.). Äquivalentes Gewicht. Entnommen von Encyclopedia_universal.ES-Academic.com.
- Chemie, anorganische Chemie (s). F.). Äquivalentes Gewicht. Entnommen von Fullquimica.com.
- Chemie.Es ist s. F.). Gleichwertig. Aus der Chemie entnommen.Ist.
- Spiegato (2021). Was ist das äquivalente Gewicht? Von Spiegato genommen.com.

