Thermodynamische Prozesse
- 2287
- 308
- Joy Hort
Wir erklären, was die thermodynamischen Prozesse sind, welche Typen existieren und mehrere Beispiele geben
Was sind die thermodynamischen Prozesse??
Der Thermodynamische Prozesse Sie sind Prozesse, bei denen ein untersuchtes thermodynamisches System einen Zustandswechsel unterzieht. Während dieser Zustandsänderung tritt eine Energiebewegung entweder innerhalb des Systems oder zwischen dem System und der Umgebung auf. In der Tat ist dies der Grund, warum sie genannt werden Thermodynamische Prozesse, Angesichts dessen Thermosflasche- Es bezieht sich auf Wärme (eine Form der Energie) und -dynamisch Bezieht sich auf Bewegung.
Durch die Änderung des Zustands wird es nicht unbedingt von fest zu Flüssigkeit oder Gasflüssigkeit bezeichnet (obwohl dies auch thermodynamische Prozesse sind), sondern zu einer Änderung der Zustandsfunktionen, dh in den Variablen, die den Zustand der definieren Systemzustand wie Temperatur, Volumen und Druck.
Die thermodynamischen Prozesse treten überall auf. Tatsächlich kann praktisch jeder Änderungsprozess, für den ein System definiert werden kann, als thermodynamischer Prozess angesehen werden. Von einem Eiscreme bis zum Betrieb eines Verbrennungsmotors oder dem Betrieb eines Mixers.
Arten von thermodynamischen Prozessen
Es gibt eine Vielzahl von thermodynamischen Prozessen, daher ist es erforderlich, diese zu klassifizieren, um ihre Studie zu erleichtern. Die Hauptkriterien zur Klassifizierung der thermodynamischen Prozesse sind:
- Nach dem Wechselkurs im System
- Nach der Zustandsfunktion, die konstant bleibt
- Nach dem zweiten Gesetz der Thermodynamik
1. Arten von thermodynamischen Prozessen gemäß dem Wechselkurs
-
Systemänderungen
Diese Art des thermodynamischen Prozesses ist durch die Passage des Systems von einem Anfangszustand zu einem endgültigen gekennzeichnet, das beide durch eine angemessene Anzahl von Zustandsvariablen definiert ist. In dieser Art von Prozessen befindet sich das System im thermodynamischen Gleichgewicht sowohl im Anfangszustand als auch im endgültigen Zustand, und die Änderung wird durch ein externes Mittel verursacht.
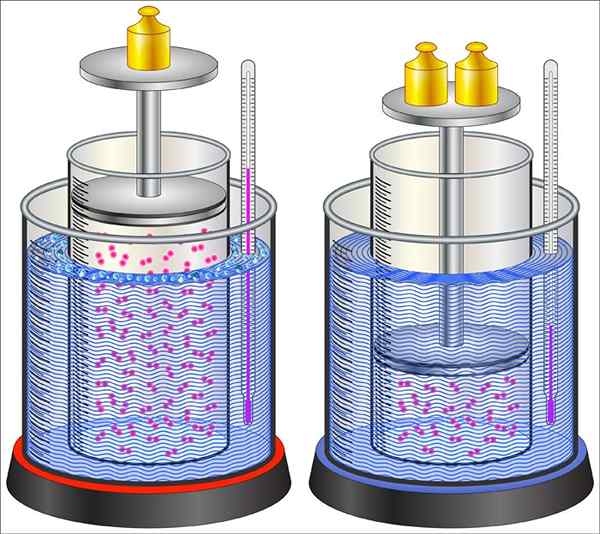
Kann Ihnen dienen: Petrischbox: charakteristisch, Funktionen, Beispiele verwenden Beispiel für den Veränderungsprozess im System, in diesem Fall tritt eine Zustandsänderung im Gas auf, das sich innerhalb des Zylinders befindet
Beispiel für den Veränderungsprozess im System, in diesem Fall tritt eine Zustandsänderung im Gas auf, das sich innerhalb des Zylinders befindet Das thermodynamische Gleichgewicht ist eine makroskopische Erkrankung, die impliziert, dass das System keine Zeitänderung unterzogen wird, es sei denn. Dies kann aus dem Beitrag der Energie in Form von Wärme und Arbeit bestehen, unter anderem.
Es ist zu beachten, dass beim Studium der Veränderungsprozesse im System viele Male (wenn auch nicht immer) der Prozess selbst nicht von Bedeutung ist, sondern nur der Ausgangszustand und der endgültige Zustand.
-
Zyklische Prozesse
In vielen Situationen, insbesondere beim Bau von Maschinen, die auf thermodynamischen Prozessen basieren, wird das System an eine Reihe von Zustandsänderungsprozessen unterzogen, die von einem Anfangszustand ausgehen, eine Reihe von Zwischenzuständen durchlaufen und erneut in derselben ursprünglichen State -Anfangsanfangszeit enden. somit einen Zyklus abschließen.
 Die Prozesse innerhalb des Zylinders eines Verbrennungsmotors sind zyklische Prozesse, die kontinuierlich wiederholt werden, um den Motor am Laufen zu halten
Die Prozesse innerhalb des Zylinders eines Verbrennungsmotors sind zyklische Prozesse, die kontinuierlich wiederholt werden, um den Motor am Laufen zu halten Zyklische Prozesse erzeugen keine Nettoänderung im Zustand des Systems (da sie im selben Zustand beginnen und enden), aber je nachdem, wie der Zyklus ausgeführt wird ein anderer oder zwischen zwei anderen getrennten Systemen.
Ein Beispiel für zyklische Prozesse ist das, was in den Kolben eines internen Verbrennungsmotors sowie der Satz von Prozessen, die innerhalb des Kühlsystemkompressors auftreten, geschieht.
-
Flussprozesse
Die Flussprozesse unterscheiden sich von den beiden anderen Arten von Prozessen, in denen das System aus der Materie besteht.
Kann Ihnen dienen: Ethylenglykol: Eigenschaften, chemische Struktur, verwendet Rohre in einer Fabrik, in der Strömungsprozesse auftreten
Rohre in einer Fabrik, in der Strömungsprozesse auftreten Diese Arten von thermodynamischen Prozessen werden häufig im Engineering verwendet, und die interessierenden Eigenschaften sind im Allgemeinen die Energieeintritts- und Ausstiegsraten zum und vom Behälter, da sie durch die Angelegenheit gekreuzt wird, die eine reine Flüssigkeit, eine Lösung, a Reaktantische Mischung usw.
2. Arten von thermodynamischen Prozessen gemäß der Zustandsfunktion, die konstant bleibt
Um ihre Analyse und Interpretation zu erleichtern, werden viele thermodynamische Prozesse durchgeführt, um eine oder mehrere konstante Variablen beizubehalten. Auf diese Weise können die Auswirkungen auf das Änderungssystem einer kleinen Anzahl von Variablen ermittelt werden. Dadurch kann verschiedene Arten von thermodynamischen Systemen definiert werden, nachdem die Variable konstant bleibt. Diese sind:
-
Isotherme Prozesse (t = CTTE)
Sind die Prozesse, bei denen die Temperatur konstant bleibt. Trotz nicht intuitiver Tatsache, dass sich die Temperatur nicht ändert. Während dieser Prozesse ändert sich die interne Energie des Systems nicht.
-
Isocorische Prozesse (V = CTTE)
Sind die Prozesse, die ohne Volumenänderung auftreten. Im Allgemeinen treten sie in geschlossenen Systemen mit starren Wänden auf (die nicht verformt werden können). Sie werden auch isovolumetrisch und isometrisch bezeichnet. Sie sind gekennzeichnet, indem sie keine Expansionsarbeit p-V einbeziehen.
-
Isobarische Prozesse (P = CTTE)
Es ist vielleicht die häufigste Art des thermodynamischen Prozesses, mit dem wir in unserem täglichen Leben getroffen haben. Sie sind durch konstante Druck gekennzeichnet.
-
Adiabatische Prozesse (q = 0)
Dies sind die Prozesse, die ohne Wärmeübertragung auftreten. Sie sind normalerweise mit isothermen Prozessen verwechselt, da viele annehmen, da keine Wärmeübertragung vorliegt, dass es keine Temperaturänderung gibt. Dies ist jedoch nicht so.
-
Isoentropische Prozesse (S = CTTE)
Sie sind Prozesse, bei denen die Entropie des Systems konstant bleibt.
-
Isoalpische Prozesse (H = CTTE)
Sie sind die Prozesse, bei denen die Enthalpie des Systems konstant bleibt.
Kann Ihnen dienen: Natriumthiosulfat (Na2s2o3)3. Arten von thermodynamischen Prozessen gemäß dem zweiten Thermodynamikgesetz
Das zweite Gesetz wird verwendet, um die Spontanität thermodynamischer Prozesse vorherzusagen. Basierend darauf können die folgenden Arten von Prozessen unterschieden werden:
-
Spontane Prozesse
Sie sind diejenigen, die eine Erhöhung der Entropie des Universums implizieren und daher spontan (natürlich) auftreten (natürlich).
-
Reversible Prozesse
Diese Art von Prozessen beinhaltet keine Veränderung der Entropie des Universums und ist daher im Gleichgewicht. Sie sind reversible Prozesse, die in beide Richtungen auftreten können.
-
Irreversible Prozesse
Sie sind solche, die eine Abnahme der Entropie des Universums implizieren und daher nicht natürlich vom Anfangszustand bis zum Ende, sondern in die entgegengesetzte Richtung auftreten.
Beispiele für thermodynamische Prozesse
- Carnots Zyklus ist a Zyklischer Prozess von 4 Stufen, auf denen Kühlsysteme wie Referenzen basieren.
- Die Verdunstung einer Wasserpfütze ist ein Beispiel für a Irreversibler thermodynamischer Prozess.
- Frostbildung in einem Gefrierschrank ist a Irreversibler Prozess.
- Die Kühlung eines Gas, das durch die Flucht aus der Flasche unter Druck gesetzt wird, ist ein Beispiel für a Ungefähr adiabatischer Prozess.
- Die Verbrennung des Küchengase isobarischer Prozess.
- Wasserheizung in einer Gasheizung ist a Flussprozess, Da das Wasser eingeht und das Rohr mit einer konstanten Geschwindigkeit verlässt, während die Wärme von der Gasverbrennung absorbiert wird.

