Proteinase K -Eigenschaften, enzymatische Aktivität, Anwendungen
- 1560
- 459
- Jasmine Kupprion
Der Proteina k Es handelt. Dieses Enzym gehört wiederum zur Familie von Subtilisin -Proteinen (Peptidase S8).
Die K -Proteinase hat ein Molekulargewicht (PM) von 28.900 Daltons und wurde zuerst in 1 isoliert.974 in Pilzauszügen Engyodontium Album, zuvor als Name von bekannt Tritirachium Album Limber.
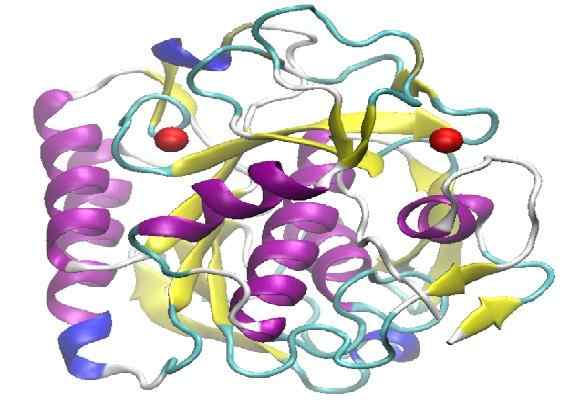
 Molekülstruktur der K -Proteinase. Quelle: Lykchiniadis [CC BY-SA 4.0 (https: // creativecommons.Org/lizenzen/by-sa/4.0)]]
Molekülstruktur der K -Proteinase. Quelle: Lykchiniadis [CC BY-SA 4.0 (https: // creativecommons.Org/lizenzen/by-sa/4.0)]] Es präsentiert eine hohe proteolytische Kapazität, die durch die Abbau des im Haar vorhandenen Keratins nachgewiesen wird. Das Wort Keratin auf Englisch ist "Keratin" geschrieben, von dort aus, dass es "Proteinsa K" genannt wurde.
Aufgrund seiner hohen Kraft, native Proteine zu teilen, ist dieses Enzym in verschiedenen Techniken der Molekülbiologie nützlich. Hauptsächlich verwendet, um Nukleinsäuren mit hohem Molekulargewicht zu isolieren und herzustellen (PM).
Die K -Proteinase wirkt durch die Freisetzung der Kern -DNA, gleich.
Andererseits wurde festgestellt, dass K -Proteinase einige denaturierte native Proteine hydrolysieren kann, was das Interesse der Forscher für die Verwendung in der Untersuchung von Prion -Proteinen (PRPC) geweckt hat.
Trotz seiner hohen proteolytischen Leistung gibt es jedoch Proteine, die gegen die Wirkung von K -Protein resistent sind. Unter ihnen gibt es einige anomale Proteine, die PRPRION (PRPSC) genannt werden, die mit übertragbaren Spongiform -Enzephalopathien assoziiert sind.
[TOC]
Eigenschaften der Proteinase K
Die K -Proteinase hat eine tertiäre Struktur aus drei Schichten mit einem β -Blatt von sieben medizinischen Ketten zwischen zwei Schichten von Propellern. Für die Zugehörigkeit zur Familie von Peptidasen wird S8 durch die Präsentation einer katalytischen Triade in ihrem aktiven Zentrum gekennzeichnet, dessen sequentielle Reihenfolge (ASP, sein und Sein) ist, was sie von anderen Peptidase -Familien unterscheidet.
Es kann Ihnen dienen: Protein AminosäurenDieses Enzym der Serinprotease -Gruppe ist durch hydrolyse Peptidbindungen in der Nähe der Carboxylgruppe aliphatischer und aromatischer Aminosäuren gekennzeichnet.
Andererseits ist es in der Lage, in Gegenwart bestimmter ätzender Substanzen wie Natriumdodecilsulfat (SDS), Tris-HCl und EDTA zu wirken.
Dies ist ein früherer Schritt bei der Herstellung von Proteinen für die Elektrophorese -Technik. Der pH -Bereich, an den die K Proteinsa wirkt, ist ziemlich breit (2.0 bis 12.0) mit einem optimalen pH zwischen 7.5 bis 12.0, und sein isoelektrischer Punkt beträgt 8.9. Wie zu sehen ist, ist es gegen eine sehr breite Palette von pH aktiv.
Ein weiteres Merkmal, das in der K -Proteinase auffällt, ist die Stabilität in Gegenwart hoher Temperaturen (50 - 60 ° C).
Enzymatische Aktivität
Die K Proteinsa benötigt das Vorhandensein von Kalziumion, obwohl es seine Aktivität nicht beeinflusst, wenn es wichtig ist, seine Stabilität aufrechtzuerhalten.
Damit die K -Proteinsa die vollständige Verdauung des Substrats durchführen können, ist eine ungefähre Kontaktzeit zwischen 5 Minuten und 2 Stunden erforderlich.
In diesem Sinne verglichen Daza und Mitarbeiter jedoch die Reinheit der DNA, die zu mehreren Expositionszeiten gegen die K -Proteinase erhalten wurde.
In Bezug auf die Konzentration des K -Proteinase -Enzyms in den verschiedenen Protokollen kann nun gesagt werden, dass es sehr unterschiedlich ist.
Es kann aus sehr niedrigen Konzentrationen (5 µg/ml) bis 500 µg/ml Konzentrationen verwendet werden. Die häufigsten Arbeitskonzentrationen liegen jedoch zwischen 50 und 100 μg /ml, insbesondere für Proteinverdauungen und Nucleas. Obwohl für die Gewebebehandlung eine Konzentration von 2 mg/ml erforderlich ist.
Kann Ihnen dienen: Easmotherium Sibiricum: Eigenschaften, Lebensraum, FossilienAnwendungen
Ihre Anwendungen sind sehr breit und können im Folgenden zusammengefasst werden:
-Es wird in der Proteinverdauung und der DNA-Extraktion mit verschiedenen Methoden verwendet: Saloting, PK-SDS, Cethyl-Tritylammonium (CTAB), modifiziertes Kaliumacetat und Natriumiodid-Extraktion Acetat.
-Inaktivierung von Nukleas (RNASAs und DNASAS).
-In der Hybridisierungstechnik Vor Ort (His), um die Freisetzung von Nukleinsäure zu unterstützen, zusätzlich zur Beseitigung unerwünschter Proteine.
-Proteinmodifikation.
-Auf Forschungsebene in verschiedenen Studien.
Vorteile von K Proteinase
Es wurden verschiedene vergleichende Studien zwischen DNA -Extraktionstechniken durchgeführt, die K -Proteinase verwenden, mit anderen, die sie nicht verwenden, und alle schließen, dass es größere Vorteile gibt, wenn das Enzym verwendet wird. Unter den Vorteilen kann Folgendes erwähnt werden:
-Hochmolekulare, hohe Qualität und Reinheit DNA wird erhalten.
-Die extrahierte DNA ist bis zu 3 Monate stabil.
DNA Extrahierte kann in den folgenden Techniken verwendet werden: Southern Blot, Polymerase -Kettenreaktion (PCR), Elektrophorese unter anderem.
Proteinase -resistente K -Proteine
Verschiedene Untersuchungen haben zu dem Schluss geführt.
Andere Autoren haben beschrieben, dass in der Struktur von PRPSC empfindliche Teile und andere gegen die K -Proteinase resistent sind. Beide Parteien sind jedoch gleichermaßen giftig und ansteckend.
Auf der anderen Seite isolierte Bastian und Mitarbeiter im Jahr 1987 4 Proteine von 28, 30, 66 und 76 kDa von einer Art von einer Art von einer Art von Spiroplasma Mirum. Alle stellten sich als resistent gegen die Wirkung der K -Proteinase und hatten auch eine Kreuzreaktion mit einigen Prionen.
Kann Ihnen dienen: ChemotoxisEs ist bekannt, dass diese Spezies wichtige Katarakte und neurologische Schäden verursachen kann, und aufgrund der wissenschaftlichen Befunde des Bastianers hat sie unter anderem versucht, sich auf diesen Mikroorganismus mit übertragbarer spongiformer Enzephalopathien zu beziehen, die übertragbar sind.
Die Ätiologie dieser degenerativen neurologischen Pathologie bleibt jedoch derzeit Prionen zugeschrieben.
In diesem Sinne identifizierte und kennzeichnete Butler und Mitarbeiter im Jahr 1991 eine Klasse von 40 kDa KDA -Proteinase -resistent aus zwei Stämmen aus zwei Stämmen von Mycoplasma Hyorhinis. Dieser Erreger betrifft Schweine und infiziert ihr Gewebe, aber in diesem Fall gab es keine Kreuzreaktion mit den getesteten Gefängnissen.
Weitere Forschungen sind in dieser Hinsicht erforderlich, um viele Unbekannte aufzuklären.
Verweise
- Bastian F, Jennings R und Gardner W. 1987. Antiserum-zu-Scrapie-Asociated Fibrillenprotein-Kreuzreaktionen mit Spiroplasma MiruM Fibrillenproteine. J. Klinik. Mikrobiol. 25: 2430-2431.
- Daza C, Guillen J, König J, Ruiz V. Bewertung einer DNA -Extraktions- und Reinigungsmethode aus Muskelgewebe, die im Formaldehyd nicht identifizierter Leichen fixiert ist. Med, 2014; 22 (1): 42-49,
- Butler G, Kotani H, Kong L, Frick M, Evancho S, Stanbridge E und McGarrity G. Identifizierung und Charakterisierung von Protein-K-resistenten Proteinen in Mitgliedern der Klassenmollicutes. Infektion und Immunität, 1991, 59 (3): 1037-1042
- López M., Rivera M., Viettri M., Lares M., Marcoima A., Herrera L. et al. Vergleich von zwei DNA -Extraktionsprotokollen von Trypanosoma Cruzi kultiviert in Axhenic Medium. Rev. Peru. Med. Exp. Gesundheitswesen 2014; 31 (2): 222-227. Erhältlich bei: Scielo.Org
- Jiménez G, Villalobos M, Jiménez E und Palma W. Bestimmung der Wirksamkeit von fünf DNA -Extraktionsprotokollen aus parafiniertem Material für molekulare Untersuchungen. Rev Méd Medic Costa Rica. 2007; 1 (1): 10-19.
- « Flora und Fauna von Santiago Del Estero Hauptart
- Programmierte Veralterung Geschichte, Typen, Konsequenzen »

