Dreifacher Punkt
- 1405
- 118
- Luca Holdt
Was ist der dreifache Punkt??
Er Dreifacher Punkt Es ist ein Begriff im Bereich der Thermodynamik, der sich auf die Temperatur und den Druck bezieht, bei dem es gleichzeitig drei Substanzphasen in einem thermodynamischen Gleichgewichtszustand gibt. Dieser Punkt existiert für alle Substanzen, obwohl die Bedingungen, unter denen sie erreicht werden.
Ein dreifacher Punkt kann auch mehr als eine Phase des gleichen Typs für eine bestimmte Substanz beinhalten. Das heißt, zwei verschiedene Feststoff-, Flüssigkeits- oder Gasphasen werden beobachtet. Das Helium, insbesondere sein Helio-4-Isotop, ist ein gutes Beispiel für einen dreifachen Punkt, an dem zwei individuelle Flüssigkeitsphasen beteiligt sind: normale und überflüssige Flüssigkeit.
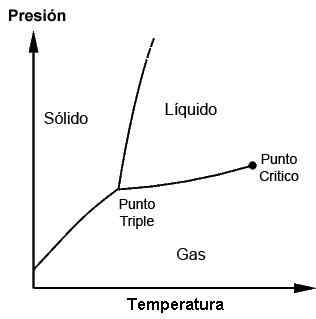
 Phasendiagramm, das den dreifachen Punkt und den kritischen Punkt zeigt
Phasendiagramm, das den dreifachen Punkt und den kritischen Punkt zeigt Wofür ist es und wenn der dreifache Punkt verwendet wird?
Der dreifache Wasserpunkt wird verwendet, um das Kelvin, die thermodynamische Temperaturbasiseinheit im Internationalen Einheiten -System (SI), zu definieren. Dieser Wert wird per Definition statt messen festgelegt.
Die dreifachen Punkte jeder Substanz können mit der Verwendung von Phasendiagrammen beobachtet werden, bei denen Diagramme aufgetragen wurden Temperatur, Druck und/oder Löslichkeit.
In seinem Schmelzpunkt befindet sich eine Substanz, in der der Feststoff der Flüssigkeit trifft; Es kann auch an seinem Siedepunkt gefunden werden, an dem die Flüssigkeit das Gas trifft. Es liegt jedoch an dem dreifachen Punkt, an dem die drei Phasen erreicht werden. Diese Diagramme sind für jede Substanz unterschiedlich, wie später zu sehen ist.
Kann Ihnen dienen: API -Schwerkraft: Skalierung und Klassifizierung von RohölDer dreifache Punkt kann effektiv bei der Kalibrierung von Thermometern unter Verwendung von Dreipunktzellen verwendet werden.
Dies sind Proben von Substanzen unter isolierten Bedingungen (innerhalb von "Zellen" von Glas), die sich an ihrem dreifachen Punkt mit bekannten Temperatur- und Druckbedingungen befinden, und erleichtern somit die Untersuchung der Genauigkeit der Thermometermessungen.
Die Untersuchung dieses Konzepts bei der Erforschung des Planeten Mars wurde ebenfalls verwendet, bei dem der Meeresspiegel während der Missionen versucht wurde, die in den 1970er Jahren durchgeführt wurden.
Dreifaches Wasser
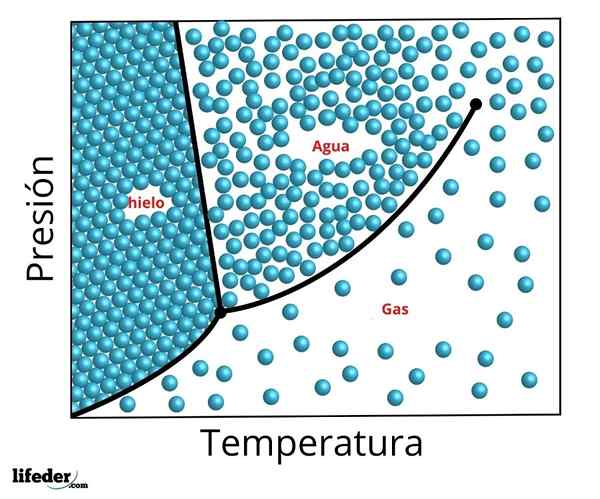 Phasendiagramm des dreifachen Wasserpunkts. Der dreifache Punkt ist der untere Punkt und der Kritiker der obere Punkt
Phasendiagramm des dreifachen Wasserpunkts. Der dreifache Punkt ist der untere Punkt und der Kritiker der obere Punkt Die genauen Druck- und Temperaturbedingungen, bei denen Wasser in seinen drei Phasen im Gleichgewicht - flüssiges Wasser, Eis und Dampf - bei einer Temperatur von genau 273,16 K (0,01 ºC) und einem Teildruck des Dampfs 611.656 Pascals (0,00603659 atm (0,00603659) auftreten ).
Zu diesem Zeitpunkt ist es möglich, die Substanz mit minimalen Temperaturveränderungen in eine der drei Phasen umzuwandeln. Auch wenn sich der Gesamtsystemdruck über dem für den Dreipunkt erforderlichen Punkt befinden kann, erreicht das System, wenn der teilweise Dampfdruck bei 611.656 PA liegt.
Es ist möglich, in der vorherigen Abbildung die Darstellung des dreifachen Punkts zu beobachten (oder Dreifacher Punkt, in englischer Sprache) einer Substanz, deren Diagramm dem von Wasser ähnlich ist, entsprechend der Temperatur und dem Druck, der erforderlich ist, um diesen Wert zu erreichen.
Bei Wasser entspricht dieser Punkt dem Mindestdruck, bei dem flüssiges Wasser existieren kann. Um unter diesem dreifachen Punkt gering zu drücken (z. B. in einem Vakuum), und wenn ein konstanter Druckheizung verwendet wird, wandelt sich feste Eis direkt in Wasserdampf um, ohne durch Flüssigkeit zu gehen. Dies ist ein Prozess namens Sublimation.
Es kann Ihnen dienen: Theorie des Urknalls: Merkmale, Stufen, Beweise, ProblemeÜber diesen Mindestdruck hinaus (p)Tp), das Eis schmilzt zuerst, um flüssiges Wasser zu bilden, und nur dort verdunstet es oder kochen, um Dampf zu bilden.
Für viele Substanzen ist der Temperaturwert an seinem dreifachen Punkt die minimale Temperatur, bei der die flüssige Phase existieren kann, dies geschieht jedoch bei Wasser nicht. Für Wasser geschieht dies nicht, da der Eisschmelzpunkt auf der Grundlage des Drucks abnimmt, wie bei der grün gepunkteten Linie der vorherigen Abbildung gezeigt.
In Hochdruckphasen weist Wasser ein recht komplexes Phasendiagramm auf, das fünfzehn bekannte Eisphasen (bei unterschiedlichen Temperaturen und Drücken) zeigt, zusätzlich zu zehn verschiedenen dreifachen Punkten, die in der folgenden Abbildung angezeigt werden:
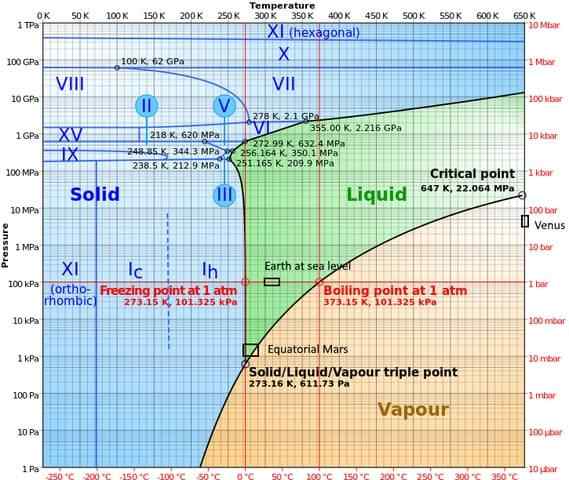
Es kann angemerkt werden, dass Eis bei hohen Druckbedingungen im Gleichgewicht mit der Flüssigkeit bestehen kann; Das Diagramm zeigt, dass die Fusionspunkte mit dem Druck zunehmen. Bei niedrigen konstanten Temperaturen und zunehmendem Druck kann Dampf direkt in Eis transformiert werden, ohne die flüssige Phase zu durchlaufen.
Die verschiedenen Bedingungen, die auf den Planeten auftreten, wo der dreifache Punkt (Land auf See und im Äquatorbereich des Mars) auch in diesem Diagramm dargestellt werden).
Das Diagramm macht deutlich, dass der dreifache Punkt aus Druck und Atmosphärentemperatur und nicht nur von Experimentatorinterventionen vom Standort abhängt.
Dreifachpunkt von Cyclohexan
Der Cyclohexan ist ein Cyclocano mit der molekularen Formel von C6H12. Diese Substanz hat die Besonderheit, drei Punkte zu haben, die leicht reproduziert werden können, wie im Fall von Wasser, da sich dieser Punkt bei einer Temperatur von 279,47 K und einem Druck von 5.388 kPa befindet.
Es kann Ihnen dienen: Live -Gebühren: Konzept, Merkmale, BeispieleUnter diesen Bedingungen wurde die Hirarverbindung beobachtet.
Dreifacher Benzolpunkt
In einem ähnlichen Fall wie Cyclohexan Benzol (organische Verbindung mit chemischer Formel C6H6) hat in einem Labor leicht dreifache Dreipunktbedingungen reproduzierbar.
Die Werte betragen 278,5 K und 4,83 kPa, daher ist das Experimentieren mit dieser Anfängerebene ebenfalls häufig.
Verweise
- Wikipedia. (S.F.). Wikipedia. Erhalten von in.Wikipedia.Org
- Britannica, e. (1998). Britannica Encyclopedia. Aus Britannica erhalten.com
- Macht, n. (S.F.). Macht nuklear. Aus Kernkraft erhalten.Netz
- Wagner, w., Saul, a., & Prub, zu. (1992). Internationale Gleichungen für den Druck entlang des Schmelzens und entlang der Sublimationskurve des normalen Wassers. Bochum.
- Penoncello, s. G., Jacobsen, r. T., & Goodwin, a. R. (1995). Zur thermodynamischen Eigenschaftsformulierung für Cyclohexan.

