Grignard Reaktive Vorbereitung, Anwendungen, Beispiele
- 1088
- 79
- Nick Laurén
Er Grignard -Reagenz Es ist eine Familie von organometallischen Verbindungen, die als allgemeine Formel aufweist, wobei R ein radikales Kohlenwasserstoff darstellt: eine Alkylgruppe, Aryl, Vinyl usw. In der Zwischenzeit repräsentiert X ein Halogen: Jod, Brom oder Chlor. Fluor wird in Grignards Reagenz nicht verwendet.
Das Reagenz verdient seinen Namen seinem Schöpfer, dem französischen Chemiker Victor Grignard im Jahr 1900, und verdient den Nobelpreis 1912 für seine Arbeit. Es wird durch Reaktion eines Organhalogen mit Magnesium hergestellt, vorzugsweise in einer Atmosphäre von Stickstoff.
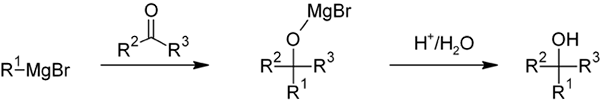 Allgemeines Schema der Reaktion von Grignard auf die BR
Allgemeines Schema der Reaktion von Grignard auf die BR In dieser Reaktion wird der Dietyl Ether oder Tetrahydrofurano (THF) normalerweise als Lösungsmittel (THF) verwendet. In der Zwischenzeit sollte Wasser vermieden werden, da es stark mit Grignards Reagenz reagiert. Dieses Reagenz ist eine starke Basis und ein Nucleophil, das heißt, wenn er reagiert, gibt er ein paar Elektronen auf.
Grignards Reagenzien reagieren mit fast allen organischen Verbindungen, mit Ausnahme von Kohlenwasserstoffen, Ether und tertiären Aminen. Die Reaktionen von Grignard zielen auf die Synthese neuer Verbindungen ab, indem neue Kohlenstoffkohlenstoffbindungen erzeugt werden.
Sie reagieren auch mit den halogenierten Verbindungen bestimmter Metalle, um ihre Alkalderivate zu bilden.
[TOC]
Grignard -Reagenzierung Vorbereitung
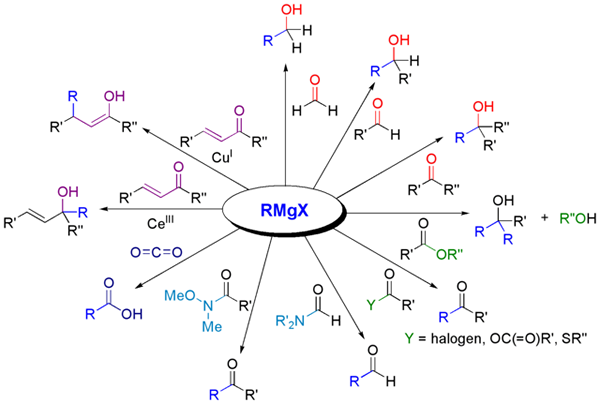 Grignards Reagenz und seine Reaktionen mit mehreren Carbonylverbindungen. Quelle: Calvero über Wikipedia.
Grignards Reagenz und seine Reaktionen mit mehreren Carbonylverbindungen. Quelle: Calvero über Wikipedia. Reagenzien
Die Reagenzien von Grignard werden hergestellt, indem die Organohalogene (RX), kleine Magnesiumstücke. Magnesium muss zuvor aktiviert werden, da es normalerweise in Form von Bändern mit Magnesiumoxid dargestellt wird, was es unfähig macht, in der Reaktion von Grignard verwendet zu werden.
Lösungsmittel und Gleichung
Die Herstellung wird in einem Kolben mit Dietyl Ether oder Tetrahydrofurano als Lösungsmittel mit Organhalogen (RX) und Magnesium durchgeführt. Der Kolben ist mit einem Refluxkondensator ausgestattet, um den Verlust des Lösungsmittels aufgrund der Verdunstung zu verringern.
Kann Ihnen dienen: Magnetische TrennungDie Komponenten der Mischung werden 20 oder 30 Minuten in einem Wasserbad erhitzt, wobei die folgende Reaktion auftritt:
Rx +mg → rmgx
Gebrauchte Lösungsmittel müssen signiert werden, dh ohne saure Hydrogene. Wasser und Alkohole sollten vermieden werden, da sie das Reagenz von Grignard protonieren und seine Zerstörung verursachen:
Rmgx +h2O → rh +mg (oh) x
Dies geschieht, weil Grignards Reagenzkohlenstoff sehr nukleophil ist, was zur Bildung eines Kohlenwasserstoffs führt. Es wird auch empfohlen, die Reaktion in einer Atmosphäre von Stickstoff auszuführen, um die Wirkung von Sauerstoff zu vermeiden.
Grignards Reagenz ist empfindlich gegenüber Feuchtigkeit und Sauerstoff, daher werden Tests seines guten Zustands durchgeführt, wobei Indikatoren dafür verwendet werden, wie Menthol, Fenantrolin oder 2,2'-Biperidin.
Anwendungen
Die wichtigste synthetische Anwendung von Grignards Reagenz ist seine Reaktion mit Verbindungen mit Carbonylgruppen für die Alkoholproduktion. Die Bildung von Kohlenstoffkohlenstoffbindungen ist schnell und exotherm.
Grignard -reaktive Reaktion mit dem Formaldehyd
Der Formaldehyd reagiert mit Grignards Reagenz, um einen primären Alkohol zu entstehen. Diese Reaktion tritt in zwei Stufen auf.
In der ersten Stufe reagiert das Formaldehyd mit Grignards Reagenz in Gegenwart des Ätherlösungsmittel.
In einer zweiten Stufe wird die Hydrolyse des vorderen Komplexes durch die Wirkung von verdünnte Schwefelsäure (H) erzeugt3ENTWEDER+), produzieren einen primären Alkohol.
Es kann Ihnen dienen: Anisol: Struktur, Eigenschaften, Nomenklatur, Risiken und VerwendungUm die Darstellung des globalen Prozesses zu vereinfachen, werden die beiden Stufen in einem so synthetisiert, als ob der primäre Alkoholbildungsprozess in einer einzelnen Stufe aufgetreten wäre:
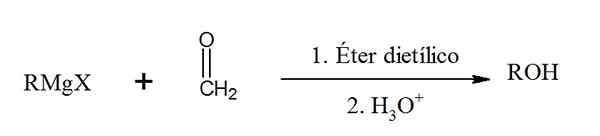 Reaktion zwischen dem Formaldehyd und einem Reagenz der Grignard. Quelle: Gabriel Bolívar über Chemsketch.
Reaktion zwischen dem Formaldehyd und einem Reagenz der Grignard. Quelle: Gabriel Bolívar über Chemsketch. Grignardreaktionsreaktion mit einem Aldehyd
Die Aldehyde, wenn sie mit Grignards Reagenz reagieren, entstehen einen sekundären Alkohol. Die Gleichung ist ähnlich wie oben, mit dem Unterschied, dass die resultierende Alkoholformel r ist2Choh.
Reagenzierung der Grignard -Reagenz mit einer Cetona
Grignards Reagenz bei der Reaktion mit einem Keton stammt aus einem tertiären Alkohol:
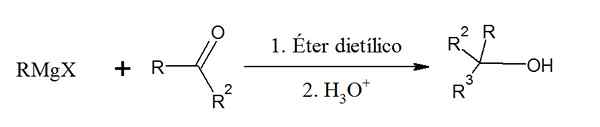 Reagenzierung der Grignard -Reagenz mit einer Cetona. Quelle: Gabriel Bolívar über Chemsketch.
Reagenzierung der Grignard -Reagenz mit einer Cetona. Quelle: Gabriel Bolívar über Chemsketch. Beachten Sie, wie dieses Reagenz verwendet wird, um Alkohole mit der höchsten Anzahl von Kohlenstoffen zu erhalten.
Grignard -Reagenz -Reaktion mit einem Ester
In dieser Synthesereaktion werden Methylester und Ethylester häufiger verwendet. Zwei Mol Grignard -Reagenz sind durch Mol des Esters erforderlich. Grignards erster Maulwurfsreaktionen mit dem Ester und bilden ein Keton- und Metaximagnesio -Halogenid (CH2Omgx):
Rmgx +r' -c (o) -Ooch3 → r' -c (o) -r +ch2Omgx
In der Zwischenzeit reagiert Grignards zweiter Maulwurf mit dem Keton auf einen tertiären Alkohol. Diese Reaktion wurde bereits im vorherigen Bild dargestellt.
Grignard -Reagenz -Reaktion mit Epoxid
In dieser Reaktion wird ein primärer Alkohol gebildet:
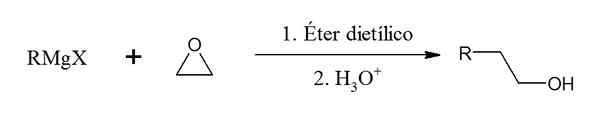 Reaktion zwischen Grignards Reagenz und Epoxid. Quelle: Gabriel Bolívar über Chemsketch.
Reaktion zwischen Grignards Reagenz und Epoxid. Quelle: Gabriel Bolívar über Chemsketch. Reagenzierung der Grignard -Reagenz mit Kohlendioxid
Wenn Grignards Reagenzs mit Carboxylsäuredioxid reagiert.
Kann Ihnen dienen: AyaroínaEinige der hier genannten Anwendungen waren im ersten Bild.
Beispiele
Beispiel 1
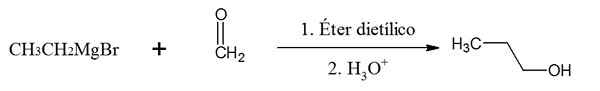 Ethylmagnesiumbromidreaktion mit dem Formaldehyd. Quelle: Gabriel Bolívar über Chemsketch.
Ethylmagnesiumbromidreaktion mit dem Formaldehyd. Quelle: Gabriel Bolívar über Chemsketch. Beachten Sie, dass das Ethylsegment an die CHO -Gruppe bindet2 der Formaldehyd zur Bildung des 1-Propanols, einem primären Alkohol.
Beispiel 2
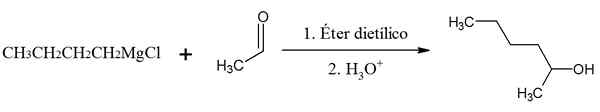 Butilmagnesium -Chloridreaktion mit Ethanal. Quelle: Gabriel Bolívar über Chemsketch.
Butilmagnesium -Chloridreaktion mit Ethanal. Quelle: Gabriel Bolívar über Chemsketch. In dieser Reaktion wird ein sekundärer Alkohol hergestellt: 2-Hexanol.
Beispiel 3
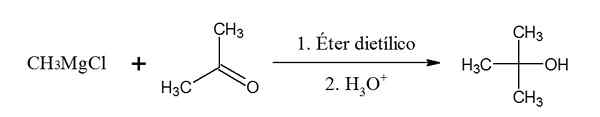 Methylmagnesium -Chlorid -Reaktion mit Propanona (Cetona). Quelle: Gabriel Bolívar über Chemsketch.
Methylmagnesium -Chlorid -Reaktion mit Propanona (Cetona). Quelle: Gabriel Bolívar über Chemsketch. In diesem Beispiel verwandelt sich Propanon, da es sich um ein Keton handelt.
Beispiel 4
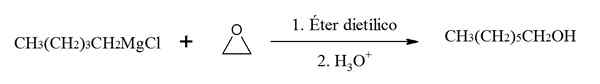 Pentilmagnesiumbromidreaktion mit Ethylenoxid (Epoxid). Quelle: Gabriel Bolívar über Chemsketch.
Pentilmagnesiumbromidreaktion mit Ethylenoxid (Epoxid). Quelle: Gabriel Bolívar über Chemsketch. In diesem Beispiel reagiert Ethylenoxid mit Pentilmagnesiumchlorid zu Alkohol 1-Heptanol.
Andere Beispiele für Grignard -Reagenz -Reaktionen
Das Arilmagnesium -Bromid und der Dietyl -Ether reagieren mit einem Vinylhalogenid, RCH = CHX oder r2C = CHX, um die Dehnung zu synthetisieren. Diese Verbindung wird zur Herstellung von Gummi, Kunststoffen, Isoliermaterialien, Rohren, Lebensmittelbehältern, Autoteilen usw. verwendet.
Gardards Reagenz wird bei der Herstellung von Tamoxifen verwendet, das Medikament bei der Behandlung von Brustkrebs eingesetzt wird.
Verweise
- Morrison, r. T. und Boyd, r, n. (1987). Organische Chemie. 5. Ausgabe. Editorial Addison-Wesley Interamerikaner.
- Carey f. (2008). Organische Chemie. (Sechste Ausgabe). Mc Graw Hill.
- Graham Solomons t.W., Craig b. Braten. (2011). Organische Chemie. (10. Ausgabe.). Wiley Plus.
- Wikipedia. (2020). Grignard -Reagenz. Abgerufen von: in.Wikipedia.Org
- Clark Jim. (2015). Eine Einführung in Grignard -Reagenzien. Erholt von: Chemguide.CO.Vereinigtes Königreich
- Sudha Korwar. (7. September 2017). Die Anwendung einer kontinuierlichen Grignardreaktion bei der Herstellung von Fluconazol. Chemie Europa. doi.org/10.1002/ejoc.201701002
- Seyferth Dietmar. (16. März 2009). Die Grignardreagenzien. Organometallikale , 28, 6, 1598-1605. doi.org/10.1021/om900088z. American Chemical Society.
- « Die 7 Bräuche und Traditionen des wichtigsten Yaquis
- Regionalisierungsmerkmale, Typen, Wichtigkeit, Beispiele »

